Clear Sky Science · pl
Metabolit jelitowy indol-3-octowy nasila neuropsychiatryczną postać toczeń przez szlak AHR/STAT3 w mikrogleju
Jak bakterie jelitowe mogą wpływać na umysł
U osób z toczniem, chorobą autoimmunologiczną, czasami pojawiają się poważne zaburzenia myślenia, nastroju i pamięci — stan określany jako neuropsychiatryczny toczeń. Objawy związane z mózgiem mogą być wyniszczające, a lekarze wciąż mają trudności z wyjaśnieniem, dlaczego występują i jak je leczyć. To badanie wskazuje niespodziewanego winowajcę: niektóre bakterie jelitowe i związane z nimi związki chemiczne, które mogą przemieszczać się z jelit do mózgu i podsycać tam stan zapalny.
Od mikrobioty jelitowej do zaburzeń zachowania
Naukowcy zaczęli od pytania, czy mikroby jelitowe od pacjentów z neuropsychiatrycznym toczniem różnią się pod względem efektów od mikrobioty pacjentów z toczniem bez objawów mózgowych. Przeniesiono bakterie ze stolca każdej z grup pacjentów do zdrowych myszy, którym wcześniej usunięto własną mikroflorę jelitową. Myszy otrzymujące mikroby od pacjentów z neuropsychiatrycznym toczniem wykazały więcej zachowań przypominających lęk, objawów depresyjnych oraz problemy z uczeniem się i pamięcią niż myszy, które otrzymały mikrobiotę od pozostałych pacjentów z toczniem. W ich mózgach zaobserwowano większą aktywację mikrogleju — komórek odpornościowych mózgu — oraz wyższe poziomy molekuł zapalnych. Ochronna bariera wokół mózgu, znana jako bariera krew–mózg, była także bardziej przepuszczalna u tych zwierząt, co sugeruje, że coś w przeszczepionej mikrobiocie uszkadza ten kluczowy element ochronny.
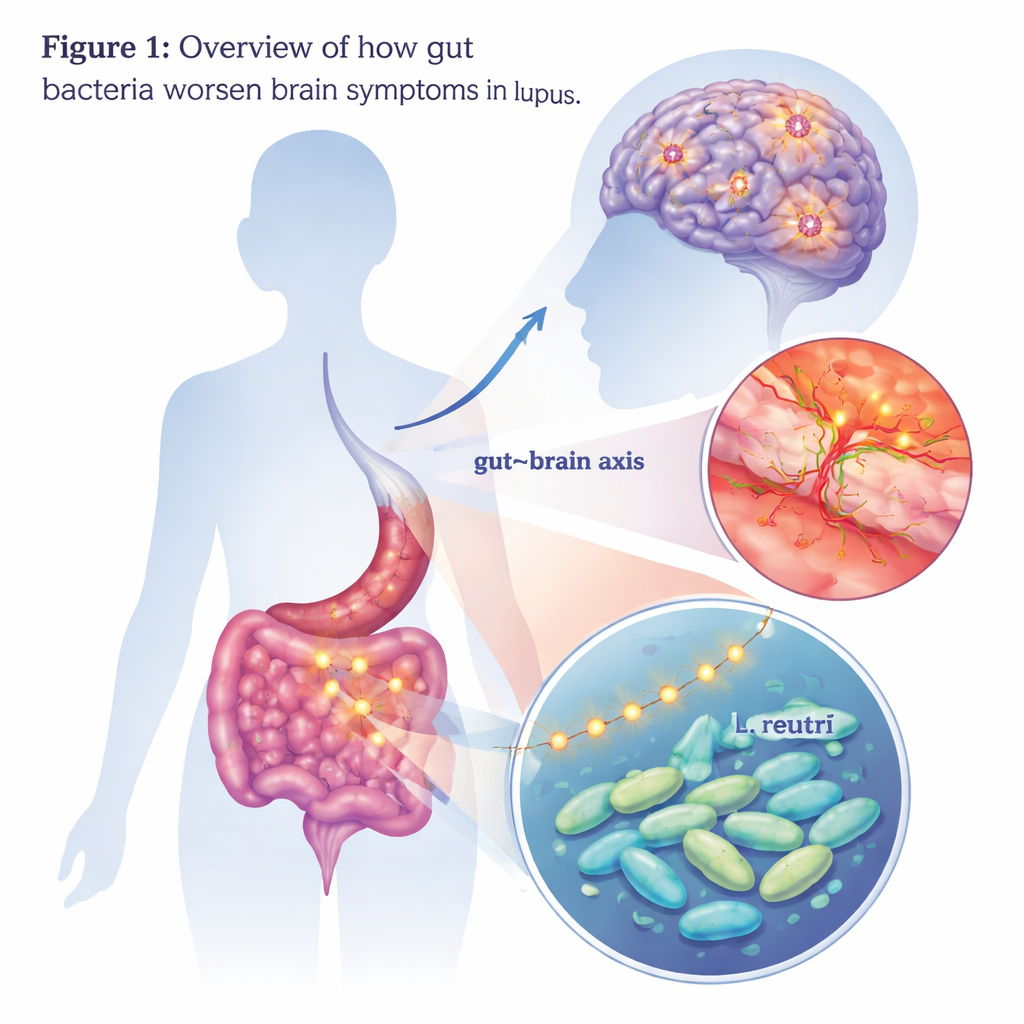
Skupiając się na jednym bakterium
Aby ustalić, które mikroby mogą być odpowiedzialne, zespół porównał składy bakterii jelitowych pacjentów i myszy. Jedna grupa wyróżniała się wyraźnie: rodzaj Lactobacillus, a w szczególności gatunek Lactobacillus reuteri, był liczniejszy u pacjentów z neuropsychiatrycznym toczniem i u myszy wykazujących zmiany mózgowe. Gdy naukowcy karmili jedynie L. reuteri myszy predysponowane do tocznia, zwierzęta rozwinęły silniejsze zachowania lękowo- i depresjopodobne oraz radziły sobie gorzej w testach pamięci. W ich mózgach obserwowano większą aktywację mikrogleju, większą utratę neuronów i dalsze zaburzenie bariery krew–mózg. Wyniki te sugerują, że przynajmniej w kontekście tocznia ten zwykle postrzegany jako probiotyczny gatunek bakterii może przyjąć bardziej szkodliwą rolę.
Mała cząsteczka o dużych efektach
L. reuteri jest znany z wytwarzania związku chemicznego zwanego indol‑3‑octowym (IAA) z tryptofanu pokarmowego. Przy użyciu czułych testów chemicznych zespół stwierdził wyższe poziomy IAA w kale pacjentów z neuropsychiatrycznym toczniem niż u innych pacjentów z toczniem oraz potwierdził, że hodowle L. reuteri wytwarzają znacznie więcej IAA niż powszechne bakterie jelitowe, takie jak Escherichia coli. U pacjentów z neuropsychiatrycznym toczniem stężenia IAA w płynie otaczającym mózg i rdzeń kręgowy korelowały z wyższymi poziomami cytokin zapalnych, co sugeruje, że ta cząsteczka może docierać do ośrodkowego układu nerwowego i wzbudzać stan zapalny. U myszy predysponowanych do tocznia karmienie L. reuteri podnosiło poziomy IAA w jelicie, krwi i mózgu. Podawanie samego IAA tym myszom odtworzyło wiele tych samych zmian: nieprawidłowe zachowania, aktywację mikrogleju, wyższe sygnaly zapalne oraz osłabienie bariery krew–mózg i bariery jelitowej.
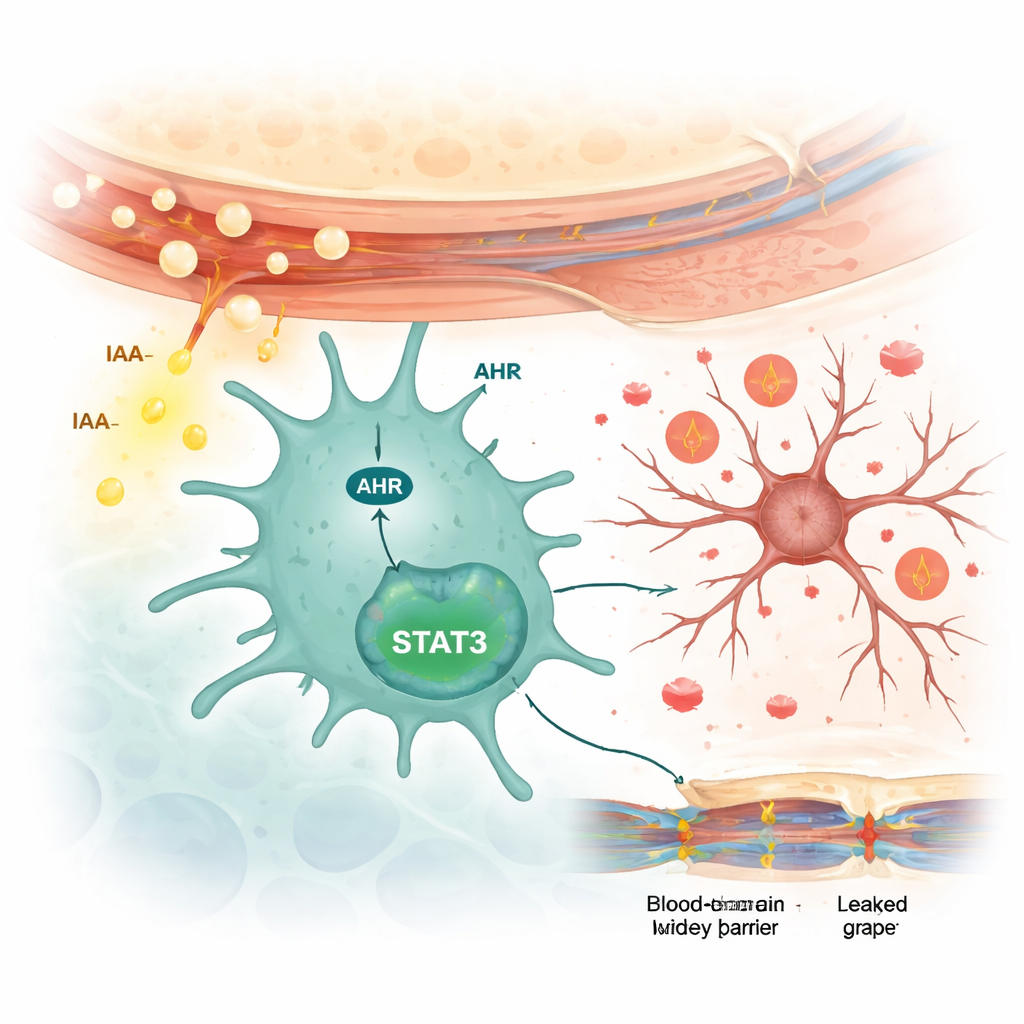
Jak komórki odpornościowe mózgu zostają włączone
Naukowcy następnie zbadali, w jaki sposób IAA komunikuje się z komórkami mózgu. Stwierdzili, że IAA zwiększa aktywność białka-sensora zwanego receptorem arylowegohydrokarbonowego (AHR) specyficznie w mikrogleju, a nie w neuronach ani w astrocytach — gwiaździstych komórkach podporowych. W hodowanych komórkach mikrogleju IAA podnosiło poziomy AHR i uruchamiało białko sygnałowe położone niżej w kaskadzie, zwane STAT3, które z kolei napędzało produkcję cytokin zapalnych. Zablokowanie AHR za pomocą leku uniemożliwiało aktywację STAT3 i ograniczało uwalnianie tych sygnałów zapalnych. Gdy myszy predysponowane do tocznia leczono lekiem blokującym AHR, ich zachowania lękowo- i depresjopodobne uległy poprawie, aktywacja mikrogleju zmalała, spadły molekuły zapalne, a bariera krew–mózg stała się mniej przepuszczalna.
Co to oznacza dla pacjentów
Łącznie badanie przedstawia łańcuch zdarzeń łączących jelito z mózgiem w neuropsychiatrycznym toczniu. Nadmiar L. reuteri w jelicie prowadzi do wytwarzania dodatkowego IAA, które osłabia barierę jelitową i przedostaje się do krwiobiegu. IAA dociera następnie do mózgu, gdzie uruchamia sygnalizację AHR i STAT3 w mikrogleju, wywołując stan zapalny, który uszkadza neurony i rozluźnia barierę krew–mózg. Dla pacjentów wyniki te sugerują, że modyfikacja mikrobioty jelitowej, zmniejszenie szkodliwych metabolitów takich jak IAA lub zablokowanie szlaku AHR/STAT3 w mikrogleju może w przyszłości pomóc chronić mózg przed wyniszczającymi skutkami neuropsychiatrycznego tocznia.
Cytowanie: Feng, Y., Zheng, L., Tang, W. et al. Gut metabolite indole-3-acetic acid aggravates neuropsychiatric lupus via the AHR/STAT3 pathway in microglia. Commun Biol 9, 281 (2026). https://doi.org/10.1038/s42003-026-09561-7
Słowa kluczowe: neuropsychiatryczny toczeń, mikrobiota jelitowa, Lactobacillus reuteri, zapalanie mikrogleju, bariera krew–mózg