Clear Sky Science · pl
Dynamiczna terapia stymulowana radionuklidami indukuje komplementarne immunogenne drogi śmierci komórkowej — nekroptozę i apoptozę w komórkach nowotworowych
Wykorzystując sztuczki raka przeciwko niemu samemu
Rak jest znany z omijania naszych najlepszych terapii, zwłaszcza w przypadku agresywnych guzów piersi, które szerzą się po całym organizmie. W tym badaniu zbadano pomysłową metodę nazwaną dynamiczną terapią stymulowaną radionuklidami (RaST), która wykorzystuje markery obrazowe i światłoczułe nanomateriały do zabijania komórek nowotworowych w sposób jednocześnie pobudzający układ odpornościowy. Dla czytelników ta praca ma znaczenie, ponieważ sugeruje, że istniejące narzędzia obrazowania i inteligentne materiały mogą zostać wykorzystane na nowo, by wywołać dłużej trwającą, napędzaną przez odporność kontrolę nowotworu, zamiast jedynie przejściowego zmniejszenia guza.
Nowy sposób na rozświetlenie guzów od wewnątrz
Tradycyjne terapie światłem działają tylko tam, gdzie może dotrzeć zewnętrzna wiązka, na przykład na skórze lub płytkich guzach. RaST omija to ograniczenie, używając radioaktywnego cukru, podobnego do markera stosowanego już w skanach PET, który naturalnie gromadzi się w szybko rosnących komórkach nowotworowych. Gdy ten znacznik przemieszcza się przez guz, emituje słabe niebieskawe światło zwane promieniowaniem Czerenkowa. Naukowcy zaprojektowali maleńkie nanocząstki dwutlenku tytanu pokryte białkiem ukierunkowującym je na nowotwór, dzięki czemu również kumulują się w guzie. Gdy znacznik i nanocząstki spotykają się, wewnętrzne światło uruchamia cząstki, które z kolei generują impulsy reaktywnych form tlenu — wysoce reaktywnych molekuł uszkadzających komórki nowotworowe od środka.
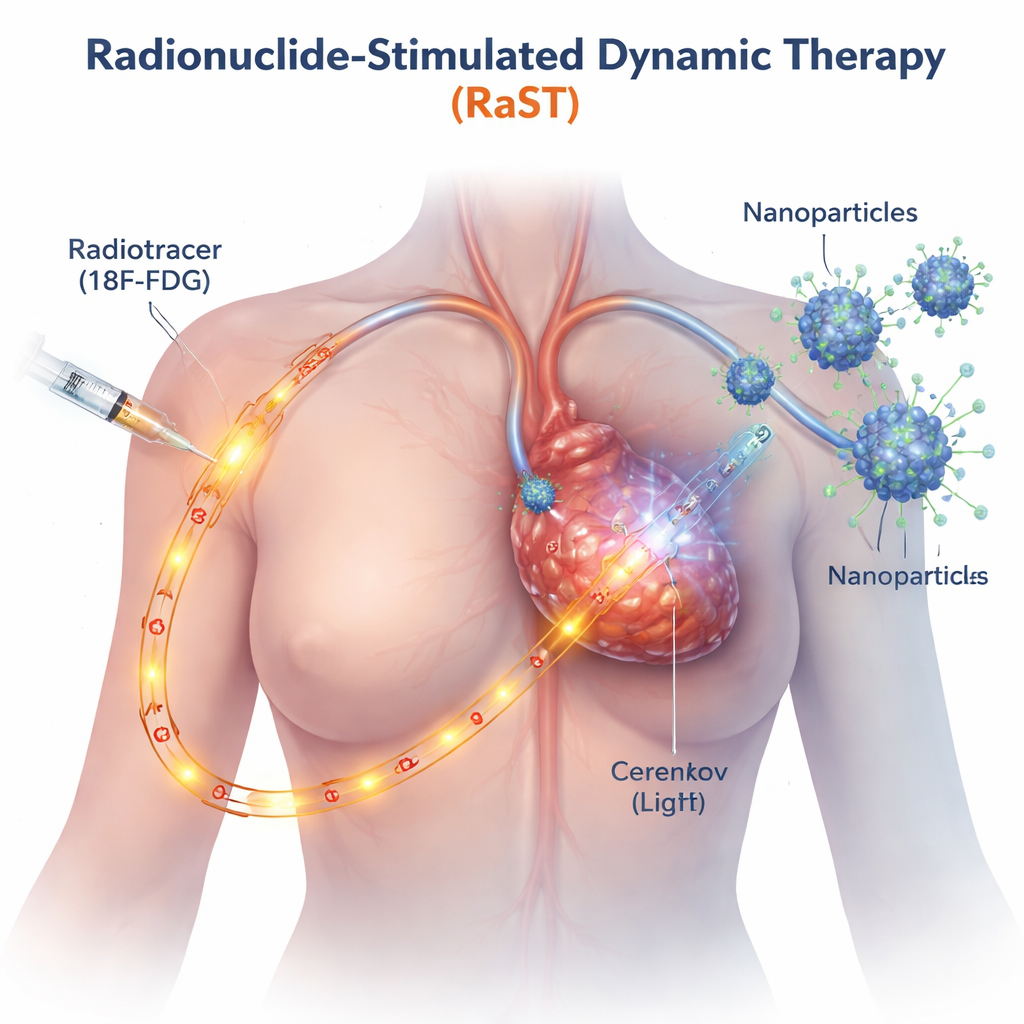
Uaktywnienie dwóch odmiennych ścieżek prowadzących do śmierci komórki
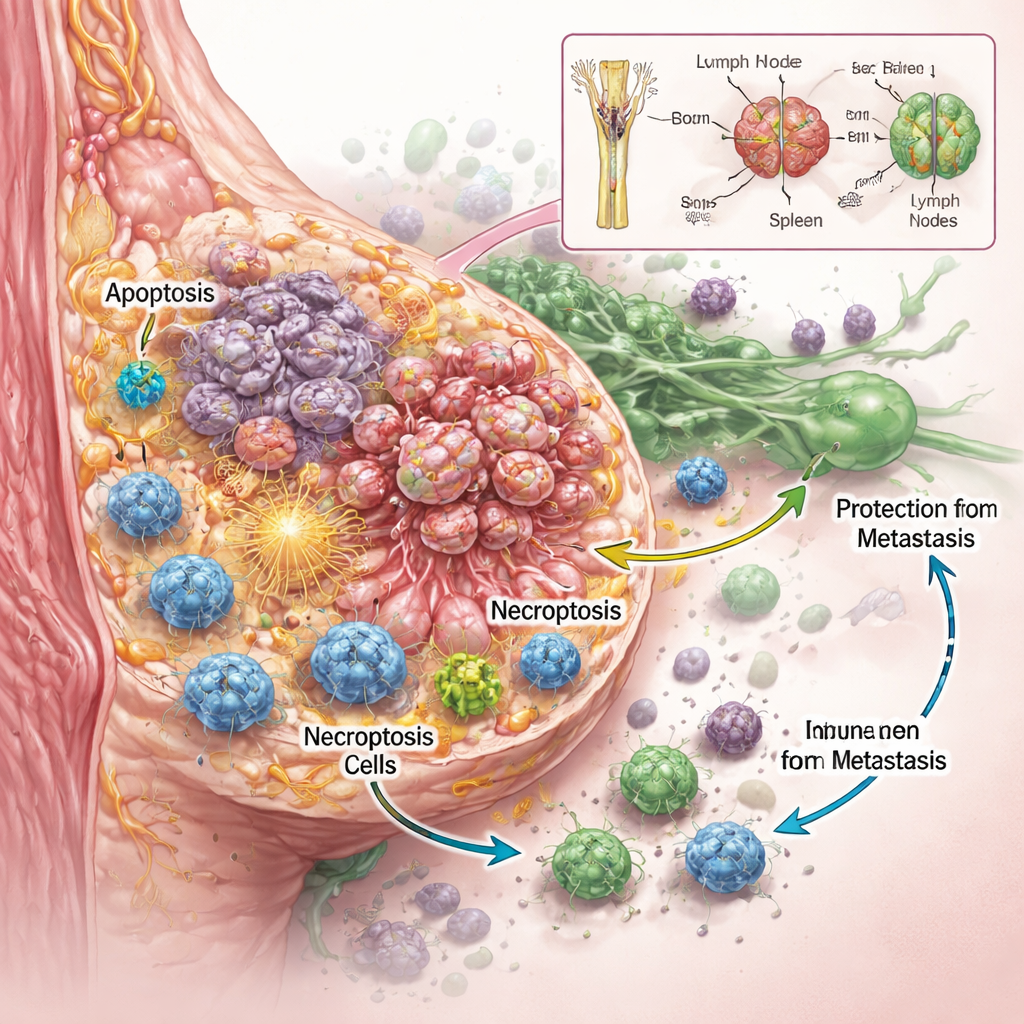
Zespół chciał wiedzieć nie tylko, czy RaST zabija komórki nowotworowe, ale także jak to robi. Używając kilku agresywnych linii komórek raka piersi w warunkach laboratoryjnych, odkryli, że precyzyjnie dobrane dawki markera radioaktywnego i nanocząstek działały razem, uszkadzając komórki guza skuteczniej niż każdy ze składników osobno, nawet w typach znanych z oporności na standardową chemioterapię. Szczegółowe obrazowanie i pomiary białek wykazały, że RaST jednocześnie aktywował dwa uregulowane programy śmierci komórki. Jeden z nich to apoptoza, często opisywana jako „samobójstwo” komórkowe, w którym komórki uporządkowanie się demontują. Drugi to nekroptoza, bardziej eksplodująca forma śmierci komórki, w której komórki pęcznieją, pękają i uwalniają molekularne sygnały alarmowe do otoczenia. Sygnały te, znane jako molekuły związane z uszkodzeniem i cytokiny zapalne, mogą działać jak race przyciągające i aktywujące komórki odpornościowe.
Angażowanie układu odpornościowego dla trwałej kontroli
Aby sprawdzić, czy ten zapalny sposób zabijania guza ma znaczenie in vivo, badacze przetestowali RaST na modelach mysich raka piersi. U myszy pozbawionych kluczowych mechanizmów odpornościowych RaST niewiele pomagał w zatrzymaniu wzrostu guza czy rozsiewu do płuc, mimo że powodował znaczne miejscowe obumieranie komórek. Jednak u myszy z nienaruszonym układem odpornościowym to samo leczenie wywołało częściowe i całkowite regresje guzów oraz zapobiegało przerzutom do płuc. Guzy wystawione na RaST wypełniły się komórkami odpornościowymi — zwłaszcza komórkami mieloidalnymi, takimi jak makrofagi i komórki dendrytyczne — które potrafią pochłaniać martwą tkankę i prezentować fragmenty nowotworu limfocytom T. Badania krwi wykazały fale sygnałów stymulujących i regulujących odporność w czasie, sugerując, że RaST najpierw uruchamia atak na nowotwór, a później przesuwa układ odpornościowy w stronę bardziej zrównoważonego stanu w miarę kurczenia się lub stabilizowania guzów.
Polowanie na ukryte resztki i ochrona przed nawrotem
Nawet u myszy, u których guzy wydawały się całkowicie wyleczone przez RaST, bardzo czuła barwnikowa metoda obrazowania wykryła później drobne ogniska resztkowych komórek nowotworowych ukryte w węzłach chłonnych. Co znamienne, zwierzęta te mimo to nie rozwinęły nowych guzów ani odległych przerzutów przez wiele miesięcy. Analizy chemiczne wykazały, że nanocząstki dwutlenku tytanu, początkowo obficie obecne w kościach i wątrobie, stopniowo przemieszczały się do śledziony i węzłów chłonnych — dokładnie tam, gdzie patrolują komórki odpornościowe. To powolne przemieszczanie się prawdopodobnie zapewnia lokalne źródło reaktywnych form tlenu dostępne dla komórek odpornościowych, pomagając im rozpoznawać i kontrolować te ukryte resztki nowotworu, zanim ponownie wzrosną lub się rozsieją.
Co to może oznaczać dla przyszłej opieki nad pacjentami z rakiem
Mówiąc prosto, praca ta pokazuje, że RaST to coś więcej niż tylko kolejny sposób zatruwania komórek guza. Łącząc radioaktywne markery, światłoczułe nanocząstki i własne mechanizmy obronne organizmu, metoda ta kieruje komórki nowotworowe na dwie formy zaprogramowanej śmierci, które głośno alarmują układ odpornościowy. U zwierząt z zachowaną odpornością prowadzi to do długotrwałej kontroli agresywnych guzów piersi i blokuje przerzuty, nawet gdy kilka komórek nowotworowych pozostaje w węzłach chłonnych. Choć przed szerokim zastosowaniem u ludzi pozostaje jeszcze wiele do zrobienia, badanie to wskazuje drogę ku terapiom, które nie tylko dążą do zmniejszenia guzów, lecz także przekształcają relację między nowotworem, śmiercią komórkową i odpornością, tak by organizm mógł pomagać w utrzymaniu choroby pod kontrolą w długim okresie.
Cytowanie: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
Słowa kluczowe: rak piersi, nanocząstki, immunoterapia, terapia radionuklidowa, nekroptoza