Clear Sky Science · pl
Reorganizacja epigenetyczna i metaboliczna w przerzutujących pheochromocytomach i paragangliomach spowodowana mutacjami SDHB
Dlaczego te rzadkie guzy mają znaczenie
Pheochromocytomy i paragangliomy to rzadkie nowotwory rozwijające się z komórek nerwowych produkujących hormony, często w pobliżu nadnerczy. Większość rośnie powoli i można je wyleczyć chirurgicznie, ale około jedna na pięć ostatecznie rozsiewa się do innych narządów, stając się zagrożeniem dla życia. To badanie stawia proste, lecz kluczowe pytanie: co sprawia, że niektóre z tych guzów stają się niebezpieczne? Analizując dogłębnie, jak nowotwory te włączają i wyłączają geny oraz jak się zasilają, badacze odkrywają ukrytą słabość, którą być może dałoby się kiedyś wykorzystać terapeutycznie.
Od łagodnego wzrostu do śmiertelnego rozsiewu
Zespół skupił się na guzach niosących zmiany w genie SDHB. SDHB pomaga mitochondriom — elektrowniom komórkowym — w przebiegu części cyklu Krebsa, kluczowej ścieżki wytwarzania energii. Gdy SDHB jest uszkodzony, gromadzi się związek zwany sukcynianem, a komórki zaczynają zachowywać się, jakby żyły w warunkach niskiego tlenu, nawet gdy tak nie jest. Badacze przeanalizowali tkanki od 34 pacjentów, porównując guzy ograniczone miejscowo z tymi, które już się rozsiewały. Wykorzystując wysokorozdzielczą mapę metylacji DNA, pokazującą, jak chemiczne znaczniki regulują aktywność genów, stwierdzili, że guzy przerzutujące mają silniejszy wzór wyciszania genów niż łagodne, szczególnie gdy występuje mutacja SDHB.
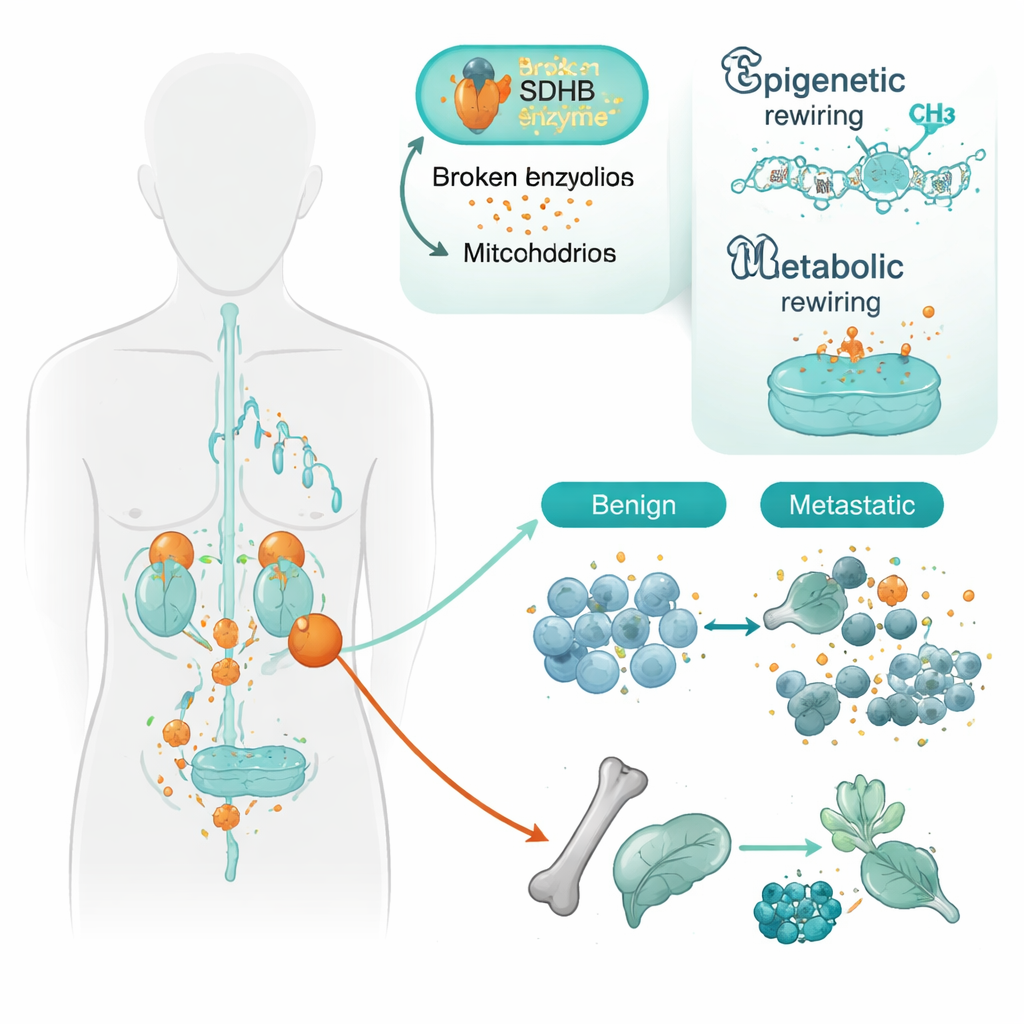
Przeprogramowanie tożsamości komórek
Wiele genów wyciszonych w agresywnych guzach to te, które pomagają komórkom nerwopodobnym dojrzewać i utrzymywać swoją wyspecjalizowaną tożsamość. Należą do nich rodziny genów kierujących przyleganiem komórek, organizacją chromatyny i decyzjami dotyczącymi losu komórkowego. Wyraźnym przykładem był gen przylegania komórkowego PCDHGC3. Nawet w nieresztujących nowotworach z mutacją SDHB region kontrolny tego genu był już częściowo wyłączony; w nowotworach przerzutujących wyciszenie było jeszcze silniejsze. Inny gen, SATB2, zaangażowany w organizację dużych odcinków DNA, był wyciszony tylko w guzach przerzutujących, niezależnie od statusu SDHB. Te wzorce sugerują, że utrata SDHB „primuje” komórki do mniej dojrzałego, bardziej ruchliwego stanu, a kolejne zmiany epigenetyczne ułatwiają im oderwanie się i rozsiewanie.
Przestrojenie sposobu, w jaki guzy „jedzą” cukry
Co zaskakujące, nie wszystkie zmiany polegały na wyciszaniu genów. Mniejsza grupa genów stała się mniej metylowana i bardziej aktywna, a były to głównie geny zaangażowane w transport cukrów do komórek. Wśród nich wyróżniał się gen transportera fruktozy SLC2A5. Jego produkt, znany jako GLUT5, przemieszcza fruktozę — cukier powszechny w owocach i wielu przetworzonych produktach — do wnętrza komórek. W modelach komórkowych przypominających guzy, eksponowanych na niskie stężenie tlenu, SLC2A5 stopniowo się włączał, podczas gdy inne transportery cukrów reagowały mniej konsekwentnie. Autorzy utworzyli następnie hodowle komórek pochodzące od pacjentów z guzami PPGL i pokazali, że gdy glukoza była ograniczona, dodanie fruktozy pomagało tym komórkom nadal się dzielić, szczególnie w warunkach o niskim poziomie tlenu, które przypominają mikrośrodowisko guza.
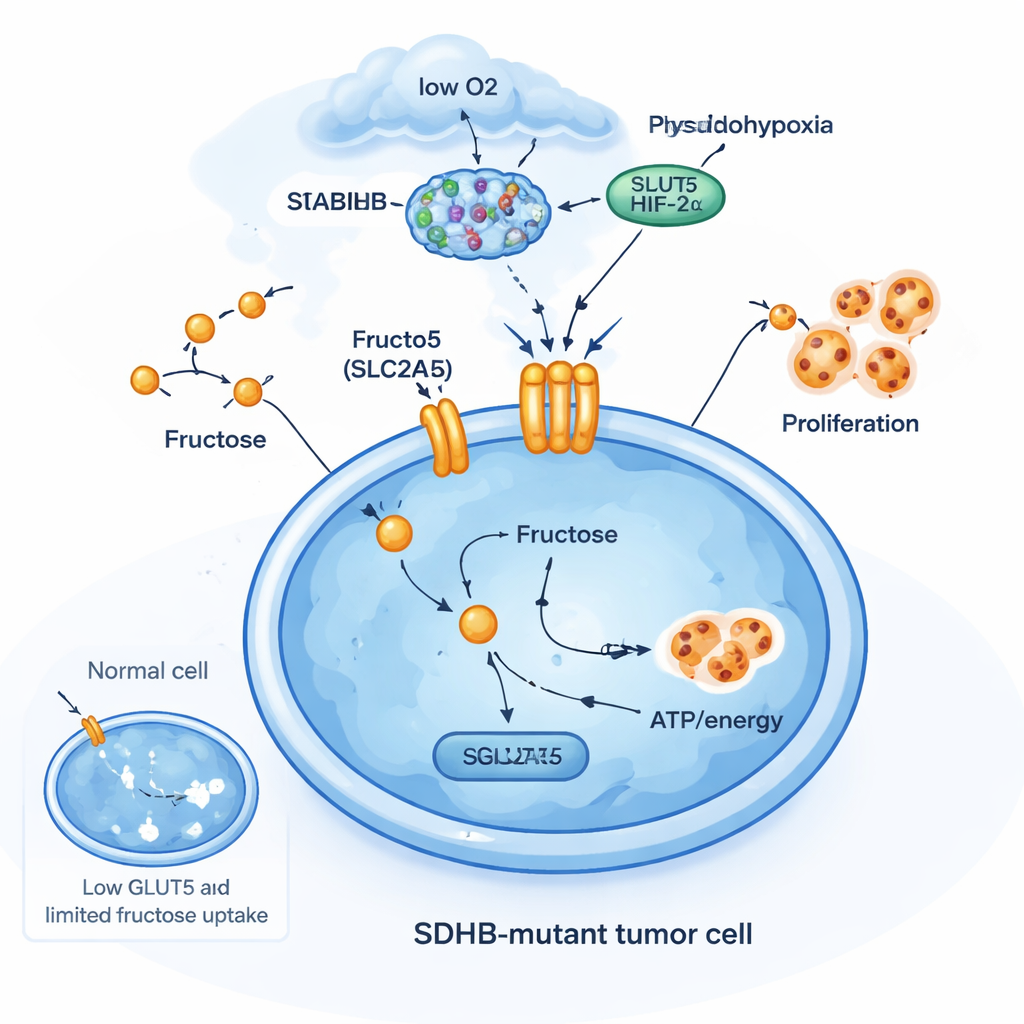
Trik przetrwania napędzany fruktozą
Aby zrozumieć, dlaczego mutacje SDHB mają tutaj znaczenie, zespół edytował kilka typów komórek, usuwając SDHB. W komórkach chromafinopodobnych z nadnercza i w linii raka nerek z konstytutywną aktywacją czynnika wykrywania niskiego tlenu HIF2α utrata SDHB zwiększała poziomy SLC2A5. Jednak w bardziej typowych liniach nowotworowych, które nie miały cech neuroendokrynnych ani aktywności HIF2α, to samo wyłączenie SDHB nie uruchamiało SLC2A5. Pokazuje to, że transporter fruktozy nie jest elementem ogólnej odpowiedzi na stres; to wysoce specyficzna adaptacja w niektórych typach komórek, które już funkcjonują w stanie „pseudo‑hipoksji”. W tych komórkach utrata SDHB, nagromadzenie sukcynianu i aktywność HIF2α współdziałają, otwierając nowe metaboliczne drzwi: pobieranie fruktozy, by zasilać wzrost, gdy tlen i glukoza są ograniczone.
Co to oznacza dla pacjentów
W skrócie, badanie ujawnia podwójną zmianę w przerzutujących PPGL z mutacją SDHB. Po pierwsze, system kontroli DNA zostaje przestrojony tak, że popycha komórki w kierunku mniej wyspecjalizowanego, bardziej plastycznego stanu sprzyjającego inwazji. Po drugie, ich system energetyczny zostaje przeprogramowany, by sięgać po fruktozę jako alternatywne paliwo w surowych, ubogich w tlen i glukozę niszach. Identyfikacja transportera fruktozy SLC2A5/GLUT5 jako kluczowego elementu tego procesu wskazuje potencjalne piętno Achillesowe: blokowanie pobierania lub metabolizmu fruktozy mogłoby selektywnie głodzić te guzy, oszczędzając większość tkanek normalnych. Chociaż takie terapie nie są jeszcze dostępne, odwzorowanie tego epigenetycznego i metabolicznego krajobrazu jest istotnym krokiem w kierunku bardziej precyzyjnych, ukierunkowanych na metabolizm terapii dla pacjentów z wysokim ryzykiem SDHB‑mutantnych PPGL.
Cytowanie: Cubiella, T., Alba-Linares, J.J., San-Juan-Guardado, J. et al. Epigenetic and metabolic rewiring in metastatic pheochromocytomas and paragangliomas driven by SDHB mutations. Commun Biol 9, 266 (2026). https://doi.org/10.1038/s42003-026-09543-9
Słowa kluczowe: pheochromocytoma, paraganglioma, mutacja SDHB, epigenetyka, metabolizm fruktozy