Clear Sky Science · pl
Analiza multi-omiczna ludzkich sieci sygnalizacyjnych PHACTR1
Dlaczego ten gen naczyń krwionośnych ma znaczenie dla ciebie
Zawały serca, udary i nadciśnienie mają swoje źródło w stanie naszych naczyń krwionośnych. Pojedynczy gen o nazwie PHACTR1 pojawia się wielokrotnie w dużych badaniach genetycznych tych schorzeń, ale naukowcy nie rozumieli, dlaczego. To badanie zastosowało szerokie, „wszystopoziomowe” spojrzenie wewnątrz ludzkich komórek, aby namapować, co PHACTR1 faktycznie robi, ujawniając, jak może wpływać na wzrost komórek, wykorzystanie energii i gospodarkę żelazem — procesy, które ostatecznie kształtują zdrowie tętnic.
Skanowanie komórek w dużej skali
Zamiast skupiać się na pojedynczych molekułach, badacze zastosowali strategię zwaną multi-omiką — jednoczesne pomiary tysięcy RNA, białek, małych metabolitów i lipidów w komórkach. Zmodyfikowali ludzkie komórki tak, by albo produkowały dodatkowe PHACTR1, albo miały zredukowaną ekspresję tego genu, naśladując naturalne różnice genetyczne występujące u ludzi. Porównując te zmienione komórki z kontrolami na czterech poziomach molekularnych, a następnie analizując dane za pomocą zaawansowanego oprogramowania do ścieżek metabolicznych, stworzyli globalną mapę tego, jak zmiana PHACTR1 rozchodzi się po wewnętrznej maszynerii komórki. 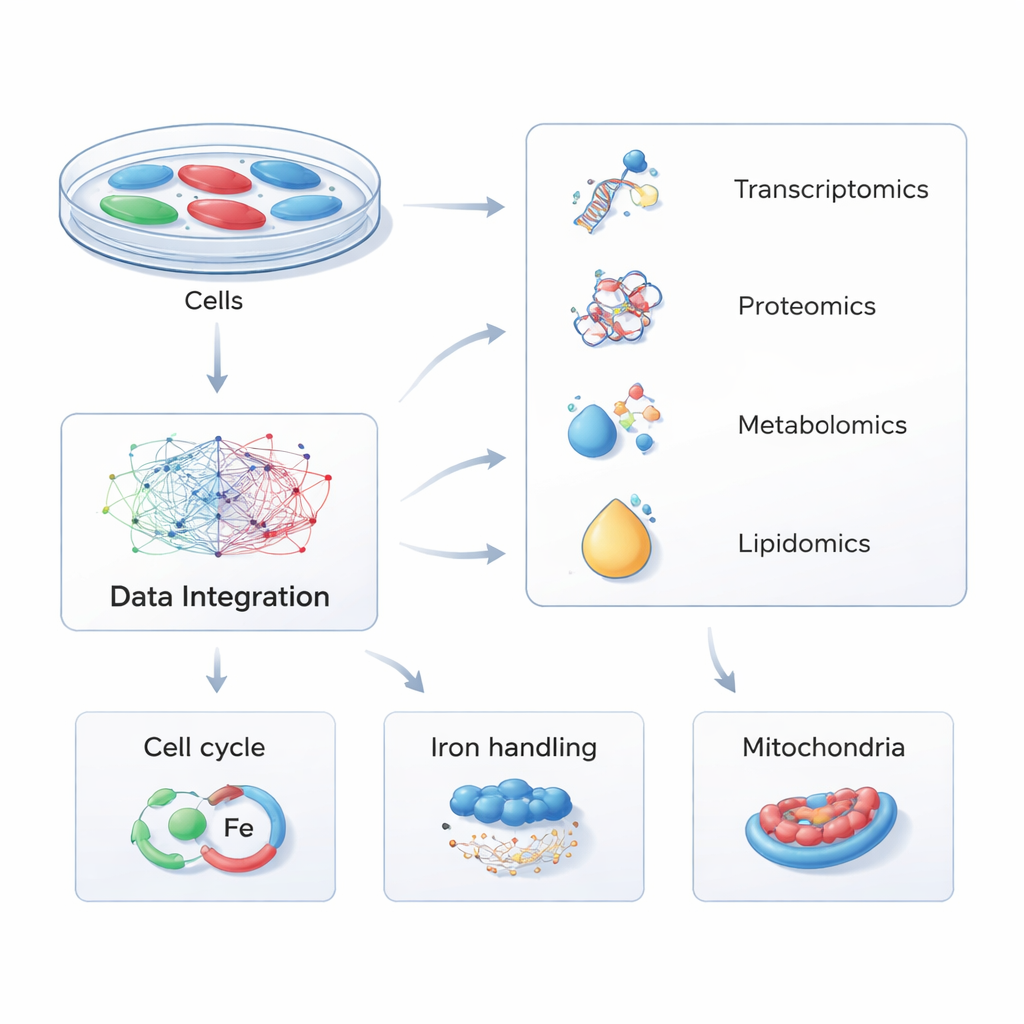
Ponad szkieletem komórkowym: kontrola cyklu komórkowego
PHACTR1 była dotychczas kojarzona głównie z organizacją wewnętrznego szkieletu komórkowego zbudowanego z filamentów aktynowych. Nowe dane wykazały, że ma też istotny wpływ na kontrolę cyklu komórkowego — choreografię, w której komórki kopiują DNA i dzielą się. Komórki z nadmiarem PHACTR1 przemieszczały się z fazy spoczynkowej G1 i kumulowały się w fazach kopiowania DNA i przygotowania do podziału, przy czym mniejsza liczba komórek prawidłowo wchodziła w pełną mitozę. Zmienione były kluczowe regulatory takie jak cyklina B1, Cdt1 oraz inne białka cyklu komórkowego. Gdy zespół powtórzył eksperymenty w pierwotnych ludzkich komórkach śródbłonka — komórkach wyściełających naczynia — ponownie zaobserwowano zmiany w podstawowych regulatorach cyklu komórkowego. Sugeruje to, że PHACTR1 pomaga decydować, kiedy komórki naczyniowe odpoczywają, dzielą się lub zatrzymują, co jest kluczową równowagą zarówno przy naprawie ścian naczyń, jak i przy powstawaniu niebezpiecznych przerostów tkankowych.
Zarządzanie żelazem i ochrona przed uszkodzeniami
Integracja multi-omiki wskazała także na ścieżki związane z żelazem i specjalistyczną formą śmierci komórkowej napędzaną żelazem, zwaną ferroptozą. Chociaż komórki nie umierały aktywnie przez ferroptozę, zwiększenie poziomu PHACTR1 obniżyło poziomy głównych białek zajmujących się żelazem, w tym łańcucha ciężkiego ferrytyny (głównej powłoki do przechowywania żelaza) oraz oksygenazy hemowej 1 (która odzyskuje żelazo z hemu). W pierwotnych komórkach śródbłonka PHACTR1 podobnie zmieniał te białka i kluczowe mechanizmy obronne przeciwko uszkodzeniom oksydacyjnym. Ponieważ nieprawidłowa gospodarka żelazem może napędzać zapalenie, stres oksydacyjny i niestabilne blaszki miażdżycowe, wyniki te sugerują, że PHACTR1 może modulować sposób, w jaki komórki naczyniowe przechowują i detoksyfikują żelazo, co potencjalnie wpływa na podatność na pewne choroby naczyń.
Mitochondria, energia i zdrowie tętnic
Kolejnym zaskoczeniem była rola PHACTR1 w mitochondriach, elektrowniach komórkowych. Zespół wykrył białko PHACTR1 w wyizolowanych mitochondriach i zaobserwował, że zmiana jego poziomów przeobraża sieć mitochondrialną. Przy wysokim PHACTR1 mitochondria były bardziej wydłużone, a białko Drp1 ulegało modyfikacji chemicznej w miejscu, które zmniejsza podział mitochondriów. Poziomy białka szkieletowego AKAP1, które pomaga organizować sygnalizację na powierzchni mitochondriów, wzrastały i spadały równolegle z PHACTR1. Zmiany strukturalne odpowiadały zmianom w produkcji energii: wysoki PHACTR1 zmniejszał mitochondrialną produkcję ATP i wiązał się z nagromadzeniem pewnych cząsteczek pochodnych kwasów tłuszczowych, które sygnalizują wolniejsze spalanie tłuszczów, podczas gdy niski PHACTR1 skłaniał komórki do większego polegania na glikolizie, czyli spalaniu cukru. Analizy próbek ludzkich tętnic wykazały, że PHACTR1 i AKAP1 mają tendencję do współaktywacji, łącząc ten mitochondrialny obwód kontroli bezpośrednio z rzeczywistymi naczyniami krwionośnymi. 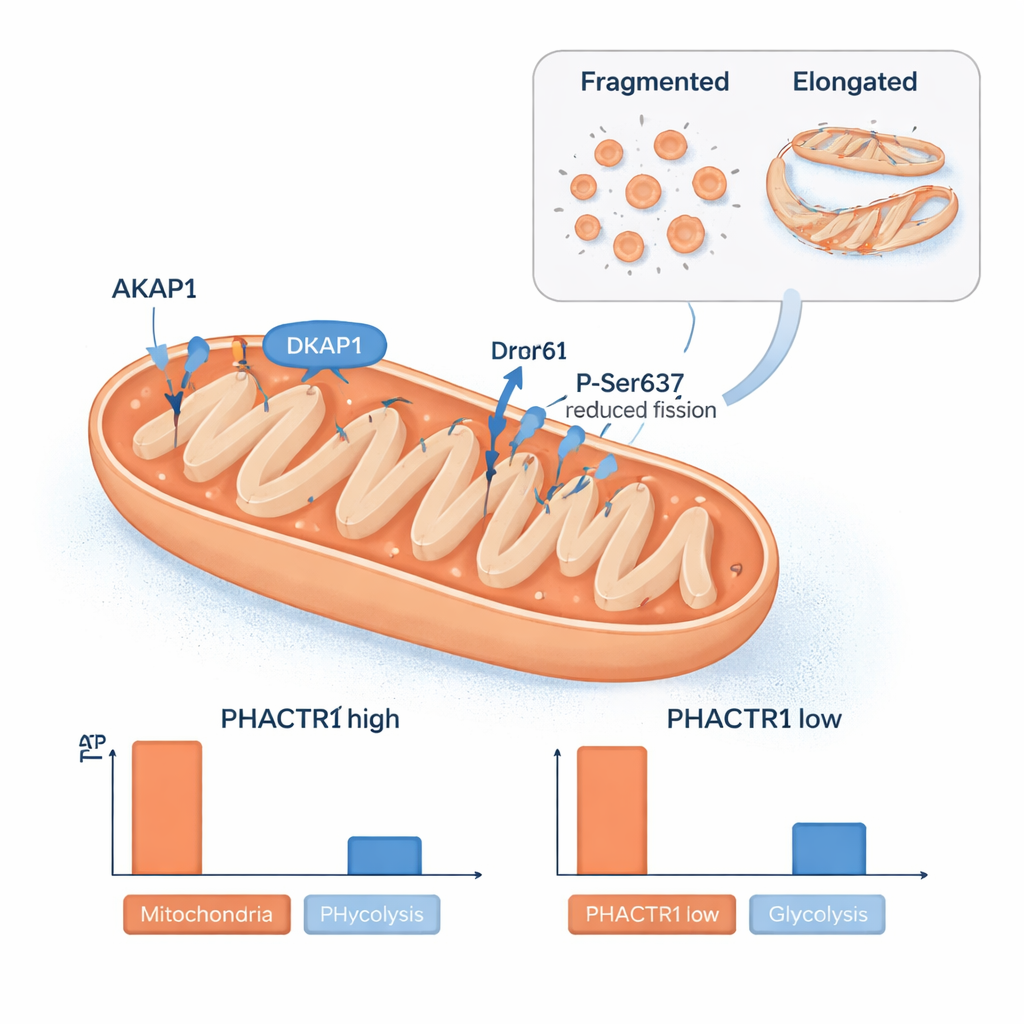
Co to wszystko oznacza dla naczyń krwionośnych
Podsumowując, praca ta pokazuje, że PHACTR1 nie jest genem o jednej funkcji, lecz mistrzowskim koordynatorem wpływającym na to, jak komórki naczyniowe dzielą się, przechowują żelazo i uzyskują energię. Mapując te powiązania wśród tysięcy cząsteczek, badanie pomaga wyjaśnić, dlaczego naturalne różnice w PHACTR1 łączą się z tak szerokim spektrum chorób naczyniowych — od choroby wieńcowej po samoistne rozdarcia tętnic i migrenę. Dla osób niebędących specjalistami przekaz jest taki, że gen wskazany przez genetykę populacyjną jest teraz śledzony aż do konkretnych zachowań komórkowych, które wpływają na wzrost blaszki, stabilność naczyń i równowagę energetyczną. W dłuższej perspektywie zrozumienie sieci kontrolowanych przez PHACTR1 może otworzyć drogę do bardziej precyzyjnych terapii, które delikatnie skorygują cykl komórkowy, gospodarkę żelazem lub funkcję mitochondrialną w kierunku zdrowszego stanu u osób zagrożonych chorobami sercowo-naczyniowymi.
Cytowanie: Wolhuter, K., Ma, L., Bryce, N.S. et al. Multi-omic analysis of human PHACTR1 signaling networks. Commun Biol 9, 265 (2026). https://doi.org/10.1038/s42003-026-09542-w
Słowa kluczowe: PHACTR1, choroby naczyń, multi-omika, mitochondria, metabolizm żelaza