Clear Sky Science · pl
Celowanie w PAK4 nasila gemcytabinowy pyroptoza w raku trzustki poprzez oś NLRP1/kaspaza-3/GSDME
Dlaczego zabijanie komórek nowotworowych „ognistym” sposobem może mieć znaczenie
Rak trzustki należy do najbardziej śmiertelnych nowotworów, a nawet najlepsze leki chemioterapeutyczne często przestają działać, gdy guzy stają się oporne. W tym badaniu zbadano zaskakujący zwrot akcji: ten sam lek, gemcytabina, może zabijać komórki nowotworowe w bardziej wybuchowy, zapalny sposób zwany pyroptozą — jeśli wyłączony zostanie kluczowy molekularny „hamulec” nazywany PAK4. Zrozumienie i celowanie w ten hamulec może sprawić, że istniejące terapie będą skuteczniejsze u wielu pacjentów.
Uparcie oporny nowotwór, który lekceważy leczenie
Ropniak przewodowy trzustki (pancreatic ductal adenocarcinoma) jest zwykle rozpoznawany późno i słabo reaguje na leczenie, dlatego gemcytabina pozostaje podstawowym lekiem mimo ograniczeń. Gemcytabina zazwyczaj zabija komórki przez apoptozę, uporządkowaną, „cichą” formę zaprogramowanej śmierci komórki. Jednak więcej niż połowa guzów trzustki przebadanych w tym badaniu wykazywała wysokie poziomy białka GSDME, które może przestawić tę cichą śmierć na pyroptozę — szybką, „pękającą” formę śmierci komórki, która uszkadza błonę komórkową i uwalnia sygnały zapalne. To postawiło kluczowe pytanie: jeśli guzy mogą przechodzić pyroptozę, dlaczego tak wiele z nich nadal jest opornych na gemcytabinę?
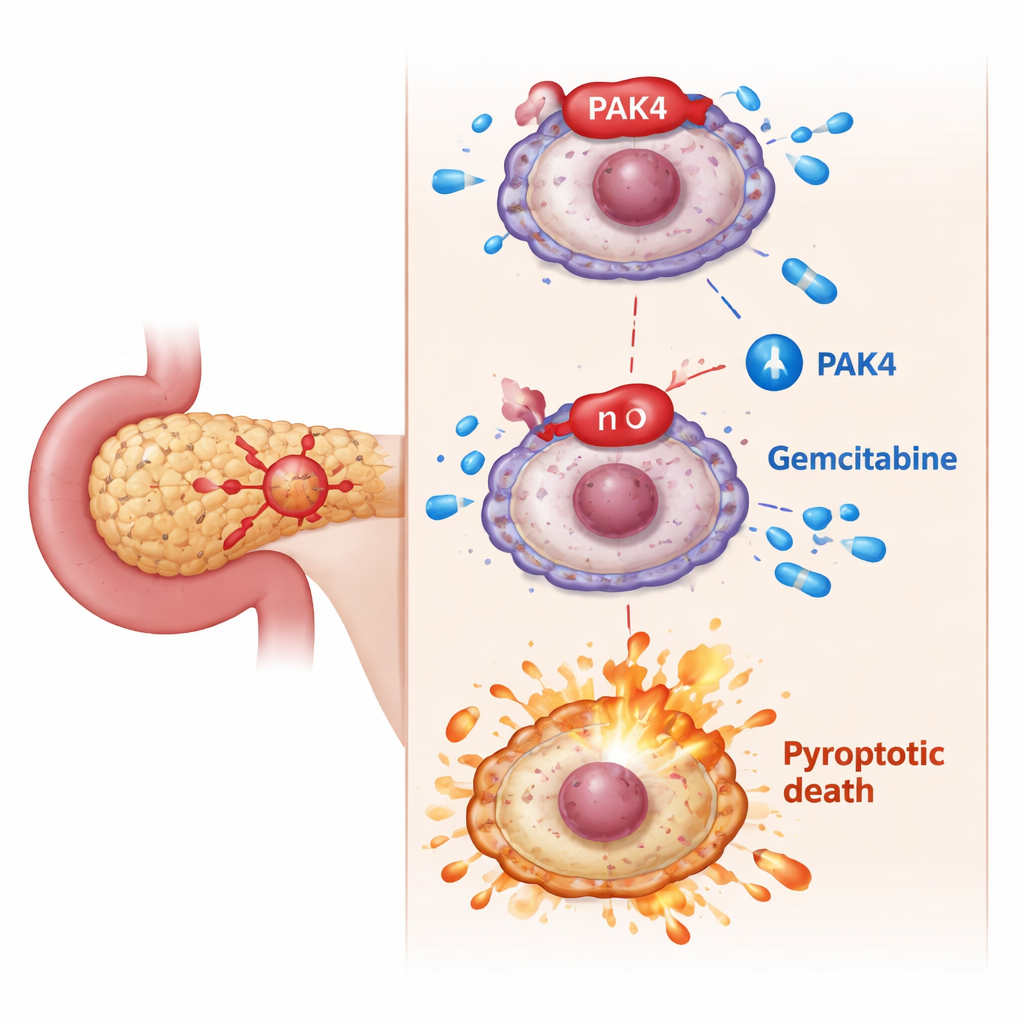
Ukryty hamulec: PAK4 blokuje „ognistą” śmierć komórki
Naukowcy skupili się na PAK4, białku promującym wzrost znanym z nadaktywności w raku trzustki i powiązanym ze słabą odpowiedzią na gemcytabinę. W eksperymentach komórkowych komórki nowotworowe o wysokim poziomie PAK4 były trudniejsze do zabicia gemcytabiną. Gdy zredukowano PAK4, gemcytabina nagle stała się znacznie bardziej śmiertelna: komórki wykazywały klasyczne cechy pyroptozy — pęcznienie, „balonowe” pęcherze, pęknięte błony i zwiększone uwalnianie zawartości wewnątrzkomórkowej. Na poziomie molekularnym ta zmiana zależała od pocięcia GSDME do aktywnego fragmentu przez inne białko, kaspazę-3. Zablokowanie kaspazy-3 powstrzymało GSDME przed wywołaniem pyroptozy, potwierdzając, że PAK4 zazwyczaj działa, hamując tę ścieżkę śmierci.
Jak PAK4 unieszkodliwia alarm śmierci komórkowej
Wnikliwsze badania wykazały, że PAK4 nie atakuje bezpośrednio GSDME. Zamiast tego sabotuje upstreamowy „czujnik alarmowy” o nazwie NLRP1. U pacjentów wyższe poziomy NLRP1 wiązały się z lepszym przeżyciem, co sugeruje, że pomaga on organizmowi kontrolować rozwój guza. W komórkach nowotworowych, gdy usunięto NLRP1, śmierć komórek indukowana gemcytabiną i aktywacja GSDME spadły gwałtownie, pokazując, że NLRP1 zasila mechanizm pyroptozy. Poziomy PAK4 i NLRP1 były odwrotnie skorelowane w próbkach guzów: tam, gdzie PAK4 był wysoki, NLRP1 był niski. Badanie wykazało, że aktywny PAK4 działa przez inne białko, ligazę E3 Mdm2, znakując NLRP1 do zniszczenia przez układ proteasomalny komórki. Oznaczając NLRP1 w ten sposób, PAK4 zapobiega uruchomieniu kaskady — przez kaspazę-9 i kaspazę-3 — która normalnie kończyłaby się GSDME-napędzaną pyroptozą.
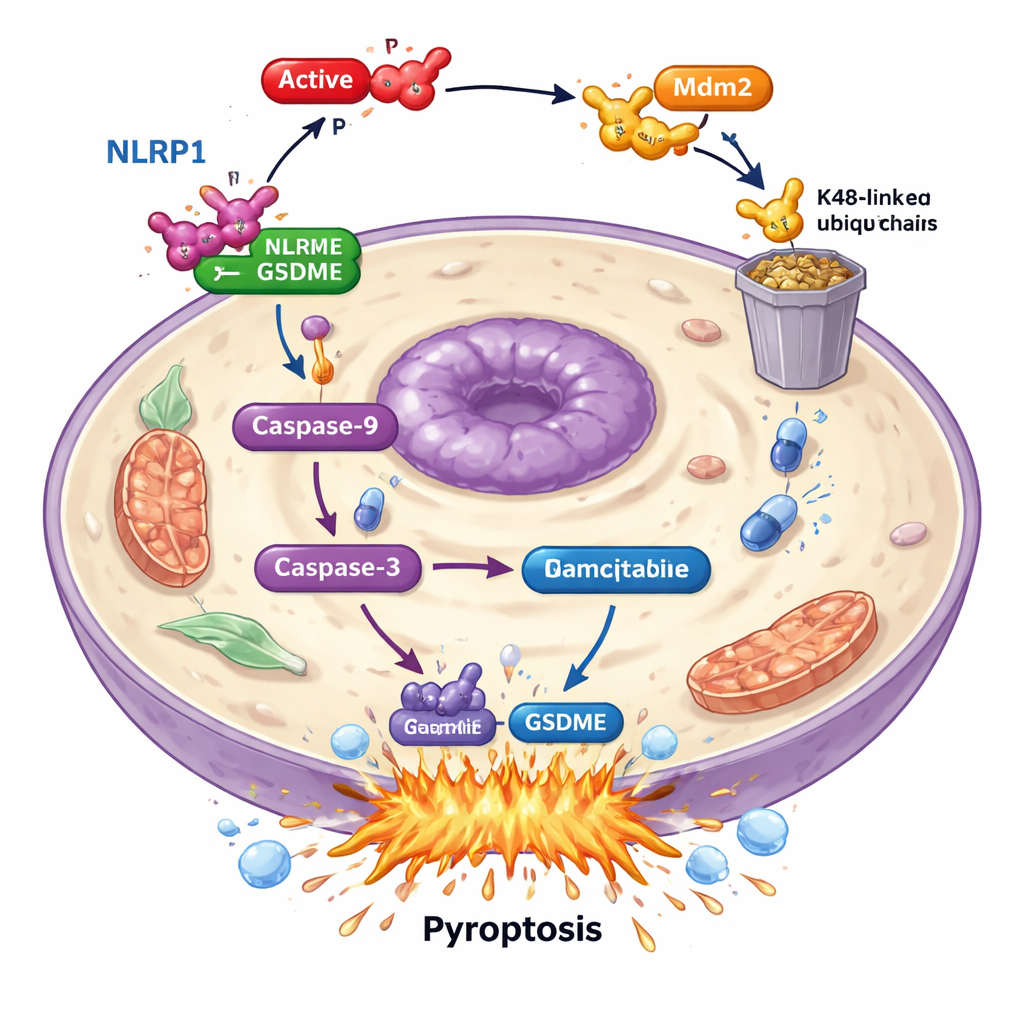
Wyłączenie PAK4, by wzmocnić chemioterapię
Ponieważ PAK4 działa jako hamulec pyroptozy, zespół sprawdził, czy zablokowanie jego aktywności może przywrócić zabójczą siłę gemcytabiny. Użyli inhibitora PAK4 o małej masie cząsteczkowej, PF-3758309. Sam inhibitor już skłaniał komórki raka trzustki ku pyroptozie, zwiększając aktywację kaspazy-3, cięcie GSDME i pęknięcia błony komórkowej. W połączeniu z gemcytabiną efekt był jeszcze silniejszy: więcej komórek zginęło przez pyroptozę, a molekularne oznaki tej ścieżki śmierci były wzmocnione. W modelach mysich z ludzkimi guzami trzustki zarówno zmniejszenie PAK4, jak i leczenie inhibitorem PAK4 sprawiły, że gemcytabina skuteczniej kurczyła guzy i zwiększała markery pyroptozy w nowotworach.
Co to znaczy dla pacjentów i przyszłych terapii
Mówiąc prosto, praca ta ujawnia molekularną blokadę — PAK4 — która powstrzymuje komórki raka trzustki przed umieraniem w szczególnie destrukcyjny sposób podczas chemioterapii. Wyłączając PAK4, lekarze mogliby skłonić guzy leczone gemcytabiną do przejścia w pyroptozę, zwiększając skuteczność leku i potencjalnie pobudzając układ odpornościowy do walki z rakiem. Choć potrzebne są dalsze badania w modelach pochodzących od pacjentów i próby kliniczne, badanie proponuje jasną drogę działania: celować w szlak PAK4–Mdm2–NLRP1–GSDME, by przekształcić oporne guzy w te podatne na leczenie, wykorzystując dostępne już leki w mądrze skombinowanych terapiach.
Cytowanie: Lu, T., Song, Y., Liang, K. et al. Targeting PAK4 promotes Gemcitabine-induced pyroptosis in pancreatic cancer via NLRP1/caspase-3/GSDME axis. Commun Biol 9, 260 (2026). https://doi.org/10.1038/s42003-026-09538-6
Słowa kluczowe: rak trzustki, oporność na gemcytabinę, pyroptoza, PAK4, terapia celowana