Clear Sky Science · pl
WDR62 jest niezbędny do prawidłowej proliferacji i wczesnej różnicowania mioblastów szkieletowych
Dlaczego wzrost mięśni wymaga precyzyjnego wyczucia czasu
Nasze mięśnie nie rosną tylko dlatego, że ćwiczymy; powiększają się i naprawiają dzięki precyzyjnemu tańcowi komórek macierzystych, które muszą się podzielić, odczekać, a dopiero potem przekształcić w działające włókna mięśniowe. W tym artykule rozkładamy na czynniki rolę często pomijanego białka WDR62 w utrzymywaniu tego rytmu. Gdy WDR62 jest nieobecny lub wadliwy, mięśnie są mniejsze, a komórki, które powinny spokojnie się mnożyć, zbyt szybko przechodzą w dojrzałe włókna, pozostawiając zbyt mało zapasowych komórek dla długoterminowej siły i naprawy.
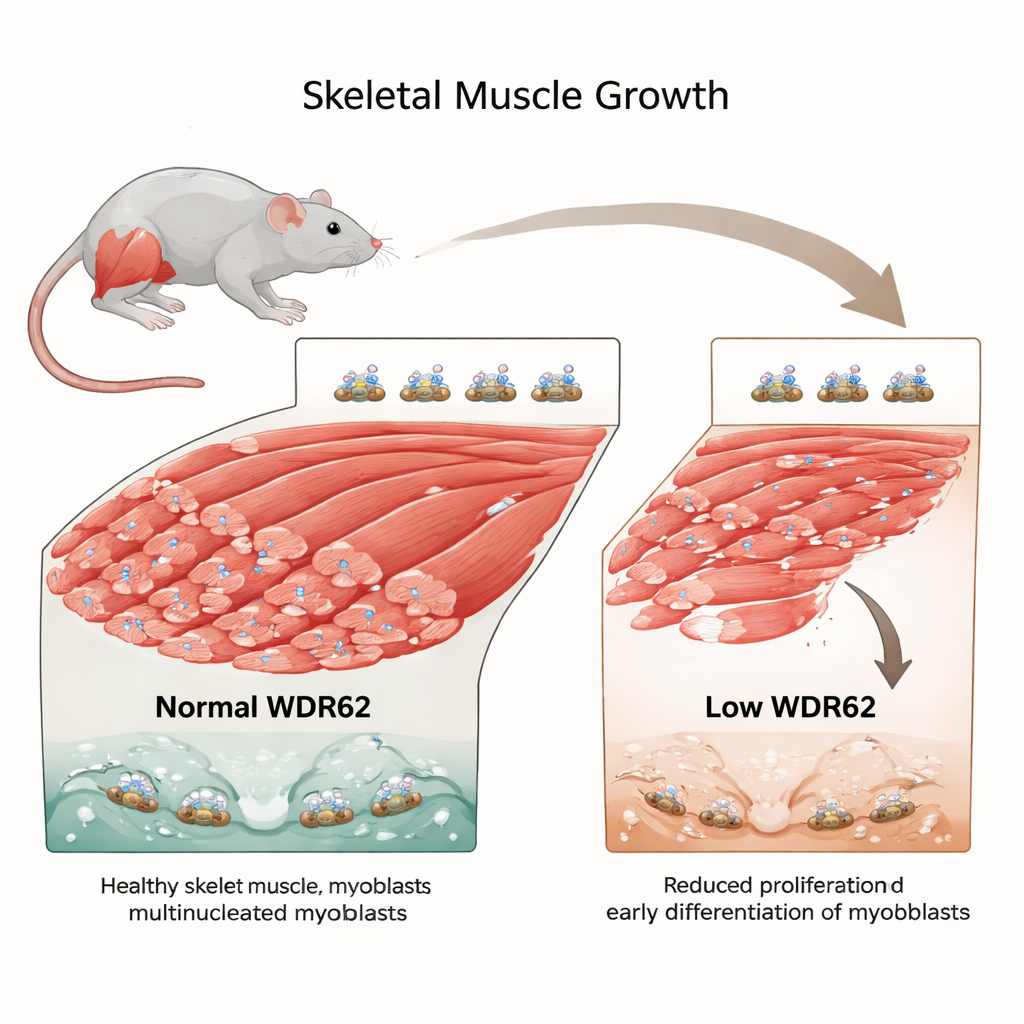
Ukryty organizator wewnątrz komórek macierzystych mięśni
WDR62 to białko zlokalizowane w małych strukturach komórkowych zwanych centrosomami, które pomagają układać rusztowanie rozdzielające chromosomy podczas podziału komórki. WDR62 już powiązano z rozwojem mózgu — jego utrata może powodować mniejszy mózg, ponieważ wczesne komórki macierzyste przestają się dzielić zbyt wcześnie. Autorzy zastanawiali się, czy podobne zjawisko zachodzi w mięśniach szkieletowych, gdzie wyspecjalizowane komórki macierzyste — tak zwane komórki satelitarne — budzą się po urazie, dzielą się kilkakrotnie jako mioblasty, a następnie łączą, by budować lub naprawiać włókna mięśniowe. Jeśli WDR62 pomaga tym komórkom prawidłowo się dzielić w mózgu, czy nie jest równie istotny dla budowy zdrowego mięśnia?
Mniejsze mięśnie i przyspieszone dojrzewanie
Aby to sprawdzić, zespół przebadał myszy zaprojektowane tak, by nie mieć funkcjonalnego WDR62. Nawet bez urazu dwie ważne dla ruchu mięśnie nogi — piszczelowy przedni (tibialis anterior) i prostownik palców długi (extensor digitorum longus) — były wyraźnie mniejsze niż u normalnych myszy. Pod mikroskopem podstawowa architektura mięśnia wyglądała normalnie, ale było nieco mniej włókien ogółem, co sugeruje, że nie było wystarczająco dużo mioblastów, by zbudować mięsień pełnych rozmiarów. Gdy badacze uszkodzili mięsień standardną toksyną, która wymusza regenerację, ogólny przebieg naprawy wyglądał zasadniczo normalnie. Jednak około tygodnia po urazie myszy pozbawione WDR62 miały więcej niedojrzałych, nowo powstałych włókien niż ich zdrowe odpowiedniki, co sugeruje, że ich mioblasty różnicowały się i łączyły wcześniej niż powinny.
Zachowane efekty od muszek owocowych po hodowane komórki
Aby sprawdzić, czy to zachowanie jest fundamentalne, a nie tylko mysim wyjątkiem, autorzy sięgnęli po muszki owocowe, które także mają prekursorowe komórki mięśni w rozwijającym się skrzydle. Zmniejszenie poziomu Wdr62 w tych muszych mioblastach prowadziło do mniejszej liczby komórek prekursorowych i większej liczby podziałów asymetrycznych — rozdziałów komórkowych dających jedną komórkę podobną do macierzystej i jedną bardziej zobowiązaną potomną. Zbyt wiele takich podziałów wyczerpuje pulę komórek macierzystych, podobnie jak obserwowano w mózgu myszy. Równolegle zespół wykorzystał klasyczną linię mysich komórek mięśniowych C2C12 hodowanych w naczyniach. Po zahamowaniu WDR62 w tych komórkach mniej komórek wchodziło w cykl komórkowy i się dzieliło, ale te, które to robiły, zaczynały nieco wcześniej łączyć się w wczesne włókna mięśniowe — ponownie wskazując na kompromis: zmniejszona proliferacja przy jednoczesnej przedwczesnej różnicowaniu.
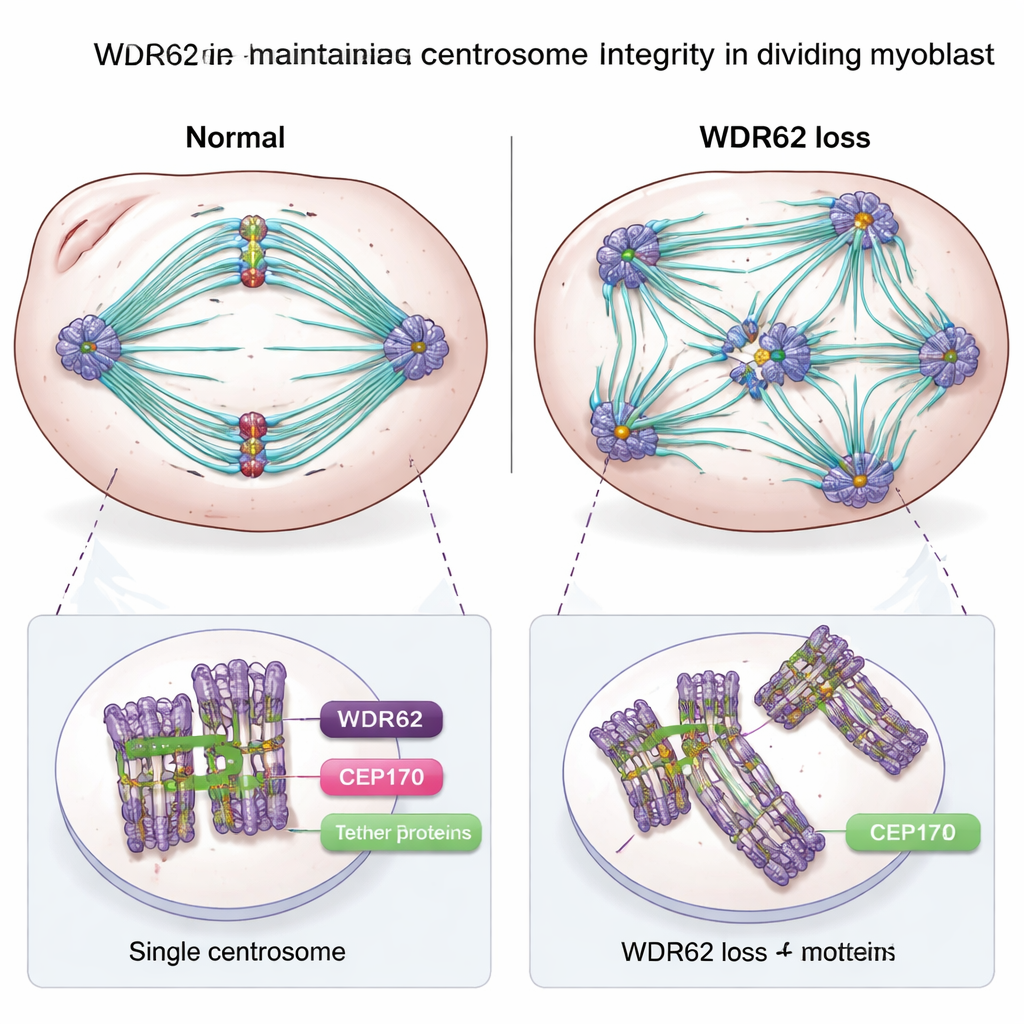
„Węzły rusztowania” komórki tracą równowagę
Zagłębiając się dalej, badacze zbadali same centrosomy. W zdrowych mioblastach każda dzieląca się komórka zwykle ma dwa centrosomy, z których każdy zawiera parę centrioli i ściśle regulowane połączenia utrzymujące je w właściwej konfiguracji. W mioblastach pozbawionych WDR62 wiele komórek miało zamiast tego dodatkowe centrioly i wiele centrosomów oraz nieprawidłowe wzorce spójności między nimi. Tego rodzaju strukturalne zamieszanie jest znane z zaburzania uporządkowanego tworzenia wrzeciona rozdzielającego chromosomy, spowalniając lub upośledzając podział komórkowy. Zespół wykazał również, że WDR62 pomaga rekrutować kolejne białko centrosomowe, CEP170, w przejściu od dzielącego się mioblastu do wczesnej, zlanej komórki mięśniowej. Razem te funkcje sugerują, że WDR62 jest kluczowym elementem machiny, która zarówno zachowuje integralność centrosomu podczas proliferacji, jak i pomaga reorganizować to rusztowanie, gdy komórki zobowiązują się do stania się mięśniem.
Co to znaczy dla zdrowia mięśni
Dla osoby nietechnicznej zasadnicze przesłanie jest takie, że budowanie i naprawa mięśni to nie tylko kwestia zwiększania liczby komórek; chodzi o zachowanie zdrowego zapasu komórek prekursorowych i precyzyjne decydowanie, kiedy mają przestać się dzielić i zacząć dojrzewać. WDR62 działa jak kierownik kontroli jakości w wewnętrznych „węzłach budowy” komórki, zapewniając, że mioblasty dzielą się czysto i pod właściwym kątem, zanim połączą się we włókna. Gdy WDR62 brakuje, mioblasty dzielą się mniej niezawodnie i zbyt wcześnie przechodzą w stan mięśniowy, co z czasem prowadzi do mniejszych mięśni i skromniejszego zapasu komórek naprawczych. Zrozumienie tej równowagi może w przyszłości pomóc w opracowaniu strategii leczenia chorób prowadzących do zaników mięśni, gdzie zachowanie lub przywrócenie puli komórek macierzystych mięśni jest tak samo ważne jak stymulacja ich wzrostu.
Cytowanie: Ho, U.Y., Shohayeb, B., Kamei, H. et al. WDR62 is required for proper proliferation and early differentiation of skeletal myoblasts. Commun Biol 9, 259 (2026). https://doi.org/10.1038/s42003-026-09537-7
Słowa kluczowe: komórki macierzyste mięśni, różnicowanie mioblastów, integralność centrosomu, WDR62, regeneracja mięśni szkieletowych