Clear Sky Science · pl
Fluwastatyna hamuje inicjację i progresję raka piersi poprzez celowanie w CYP4Z1
Dlaczego lek obniżający cholesterol ma znaczenie w raku piersi
Wiele kobiet leczonych z powodu raka piersi rozwija nieprawidłowe stężenia tłuszczów we krwi i stoi przed ciągłym ryzykiem nawrotu choroby lub jej rozsiewu. To badanie bada intrygującą koncepcję: czy powszechny lek obniżający cholesterol, fluwastatyna, mógłby zostać ponownie wykorzystany do spowolnienia lub zapobiegania rakowi piersi przez unieszkodliwienie białka napędzającego szczególnie niebezpieczne, podobne do komórek macierzystych komórki nowotworowe?
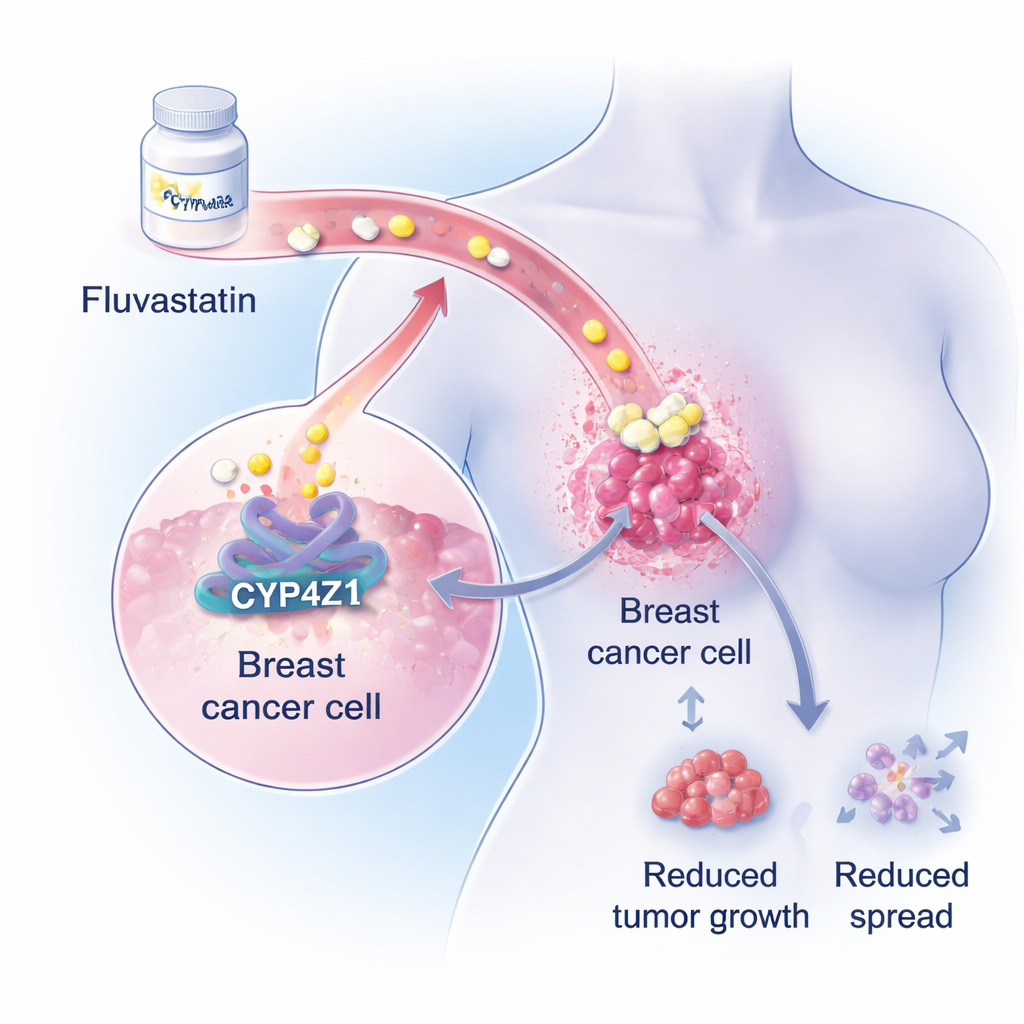
Ukryty czynnik napędzający wewnątrz guzów piersi
Naukowcy skupili się na mało znanym białku o nazwie CYP4Z1, występującym w wysokich poziomach w komórkach raka piersi, ale nie w zdrowej tkance piersi. Wcześniejsze badania wykazały, że CYP4Z1 pomaga komórkom nowotworowym zachowywać się bardziej jak komórki macierzyste — komórki mogące nieustannie się odnawiać, oporne na chemioterapię i zdolne do odtwarzania guza po leczeniu. W szerokich analizach genetycznych i biochemicznych zespół wykazał teraz, że nadaktywność CYP4Z1 silnie wzmacnia szlaki syntezy tłuszczów w komórkach raka piersi, zwłaszcza produkcję trójglicerydów, głównego tłuszczu magazynowego. Ponieważ wielu pacjentów z rakiem piersi już rozwija zaburzenia lipidowe podczas chemioterapii, rola CYP4Z1 promująca gromadzenie tłuszczu zasugerowała możliwość wykorzystania istniejących leków obniżających lipidy.
Ponowne zastosowanie fluwastatyny z kardiologii w onkologii
Aby sprawdzić ten pomysł, naukowcy przesiewowo przetestowali małą bibliotekę 23 zatwierdzonych przez FDA leków stosowanych do obniżania lipidów we krwi. Fluwastatyna, szeroko przepisywana statyna na wysoki cholesterol, wyróżniła się: bezpośrednio blokowała aktywność enzymatyczną CYP4Z1 w sposób zależny od dawki. Przy dawkach znacznie mniej szkodliwych dla normalnych komórek gruczołu mlekowego niż dla komórek nowotworowych, fluwastatyna wyraźnie zmniejszała kluczowe markery „stemness”, zdolność komórek raka piersi do tworzenia unoszących się „sfer guzowych” oraz ich zdolność do migracji i inwazji przez struktury przypominające tkanki w testach laboratoryjnych. Zwiększała także wrażliwość komórek nowotworowych na lek chemioterapeutyczny adriamycynę, co sugeruje, że może wzmocnić istniejące terapie.
Testowanie leku na żywych zwierzętach
Zespół następnie ocenił fluwastatynę w modelach mysich. U myszy wszczepionych ludzkimi komórkami raka piersi okresowe leczenie fluwastatyną spowalniało wzrost guza, obniżało poziomy markera „stemness” (ALDH1A1) oraz markera podziału komórkowego Ki67 w guzach i zmniejszało liczbę ognisk przerzutowych pojawiających się w płucach. Co ważne, myszy otrzymujące fluwastatynę utrzymywały masę ciała i nie wykazywały istotnych nieprawidłowości krwi ani szpiku kostnego, co wspiera korzystny profil bezpieczeństwa przy testowanej dawce. W bardziej realistycznym modelu genetycznym — myszach zmodyfikowanych tak, by rozwijały guzy piersi wywoływane przez gen rakotwórczy — badacze dodatkowo wprowadzili ludzki CYP4Z1 do tkanki gruczołu mlekowego. Te myszy rozwijały więcej zmian przednowotworowych i nowotworowych oraz więcej przerzutów do wątroby i płuc niż zwierzęta kontrolne. Leczenie fluwastatyną znacząco zmniejszyło zarówno liczbę zmian gruczołowych, jak i odległych przerzutów, zwłaszcza u myszy niosących dodatkowy gen CYP4Z1.
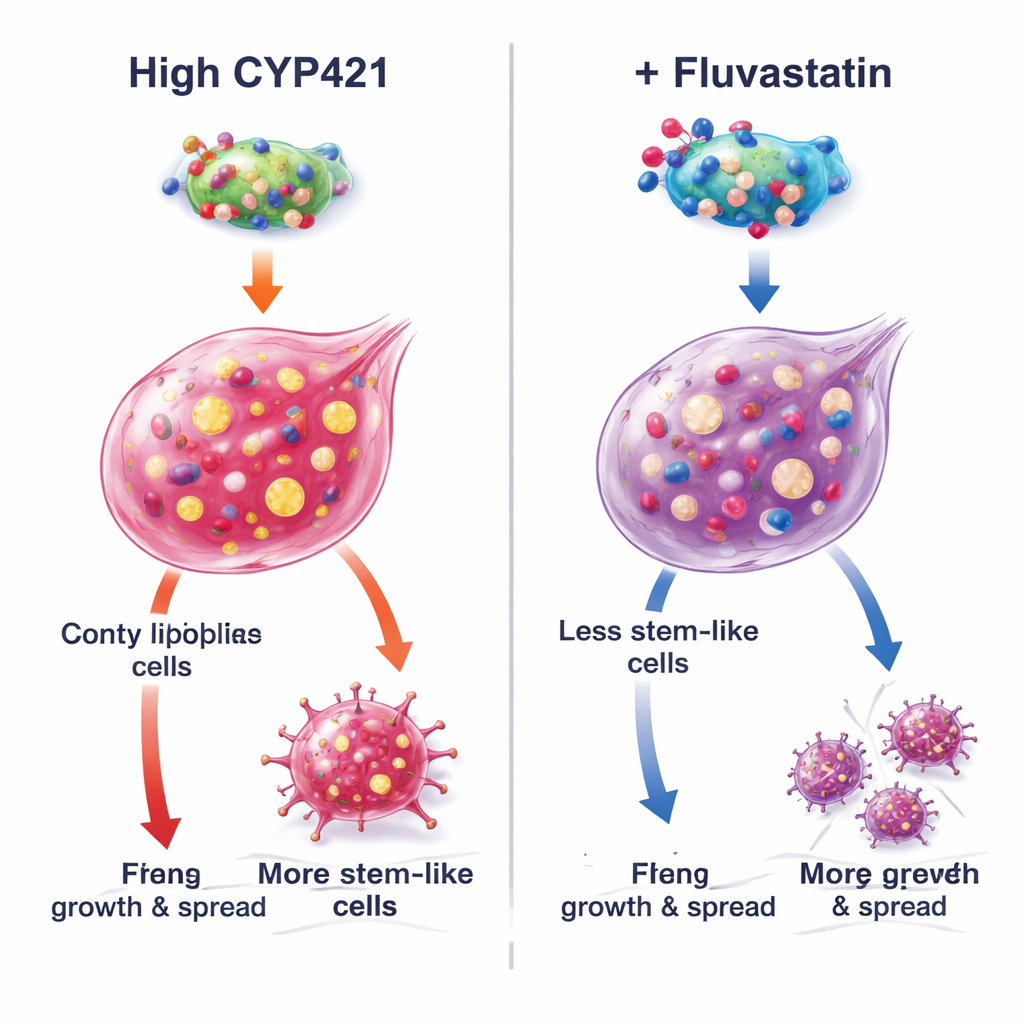
Jak fluwastatyna unieszkodliwia białko promujące rozwój nowotworu
Aby zrozumieć mechanizm, autorzy połączyli modelowanie komputerowe z precyzyjnym inżynierią białkową. Przewidzieli, że fluwastatyna wsuwa się w miejsce aktywne CYP4Z1 przy trzech krytycznych aminokwasach (Lys109, Pro444 i Arg450). Gdy te miejsca zostały zmutowane, aktywność CYP4Z1 spadła, a fluwastatyna nie mogła go dalej hamować, co potwierdziło te pozycje jako punkty dokowania. W komórkach naturalnie pozbawionych CYP4Z1 wprowadzenie normalnego białka zwiększało cechy „stemness” i aktywowało szlak promujący wzrost PI3K/AKT, podczas gdy fluwastatyna odwracała te efekty. Mutanty CYP4Z1 były mniej aktywne i mniej wrażliwe na lek. Dodatkowe eksperymenty wykazały, że efekt fluwastatyny słabł, gdy sztucznie zwiększano produkcję trójglicerydów lub gdy CYP4Z1 był wyciszony, podkreślając, że najsilniejsze działanie leku wynika z blokowania tego konkretnego białka i jego następstw w syntezie tłuszczów, a nie z wywoływania śmierci komórki poprzez żelazozależną „ferroptozę”.
Co to oznacza dla pacjentek
Podsumowując, badanie sugeruje, że fluwastatyna, poza obniżaniem cholesterolu, może hamować wczesne etapy i późniejsze rozsiewanie raka piersi w modelach doświadczalnych poprzez celowanie w CYP4Z1 — białko napędzające metabolizm tłuszczów i zachowania podobne do komórek macierzystych w guzach. Ponieważ fluwastatyna jest już zatwierdzona, a jej bezpieczeństwo dobrze poznane, wyniki te otwierają obiecującą drogę do szybszych badań klinicznych jako terapii uzupełniającej, zwłaszcza u pacjentek, których guzy wykazują silną ekspresję CYP4Z1. Choć potrzebne są dalsze badania, aby sprawdzić podejście u ludzi i zidentyfikować ewentualne dodatkowe cele leku, praca ta otwiera możliwość wykorzystania znanego leku kardiologicznego jako części nowej strategii przeciw agresywnym, skłonnym do nawrotów rakom piersi.
Cytowanie: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
Słowa kluczowe: rak piersi, fluwastatyna, komórki macierzyste nowotworu, metabolizm lipidów, ponowne zastosowanie leków