Clear Sky Science · pl
Ukierunkowane blokowanie splicingu genów może zaburzać pierwotne mikroRNA osadzone w intronach
Ukryte komunikaty wewnątrz naszych genów
Wiele nowych terapii genowych działa poprzez subtelną modyfikację komunikatów RNA w komórkach, lecz te RNA często kryją dodatkowe „notatki na marginesie”, które nauka dopiero zaczyna rozumieć. Artykuł pokazuje, że leki zaprojektowane do korekcji błędnego splicingu genów mogą przypadkowo podnosić poziom małych regulatorowych RNA ukrytych w intronach — niekodujących odcinkach między segmentami genu — z zaskakującymi efektami dla połączeń nerwowych i rozwoju.
Terapie genowe, które przepisują RNA
Oligonukleotydy antysensowne (ASO) to krótkie syntetyczne fragmenty materiału genetycznego, które wiążą się z RNA i zmieniają sposób jego odczytu lub przetwarzania. Kilka ASO jest już testowanych lub stosowanych w rzadkich chorobach genetycznych, zwłaszcza tam, gdzie przyczyną są błędy splicingu — etapu łączącego segmenty kodujące genu. Większość testów bezpieczeństwa koncentruje się na tym, czy ASO przywraca prawidłowy białkowy produkt i unika oczywistych skutków ubocznych. Jednak wiele genów zawiera również niekodujące RNA, w tym microRNA, umieszczone w intronach. Te drobne cząsteczki silnie modulują aktywność genów, a nawet do połowy znanych microRNA kręgowców pochodzi z intronów. Nowe badanie zadaje pytanie: co dzieje się z tymi wbudowanymi microRNA, gdy wymuszamy zmiany splicingu za pomocą ASO?
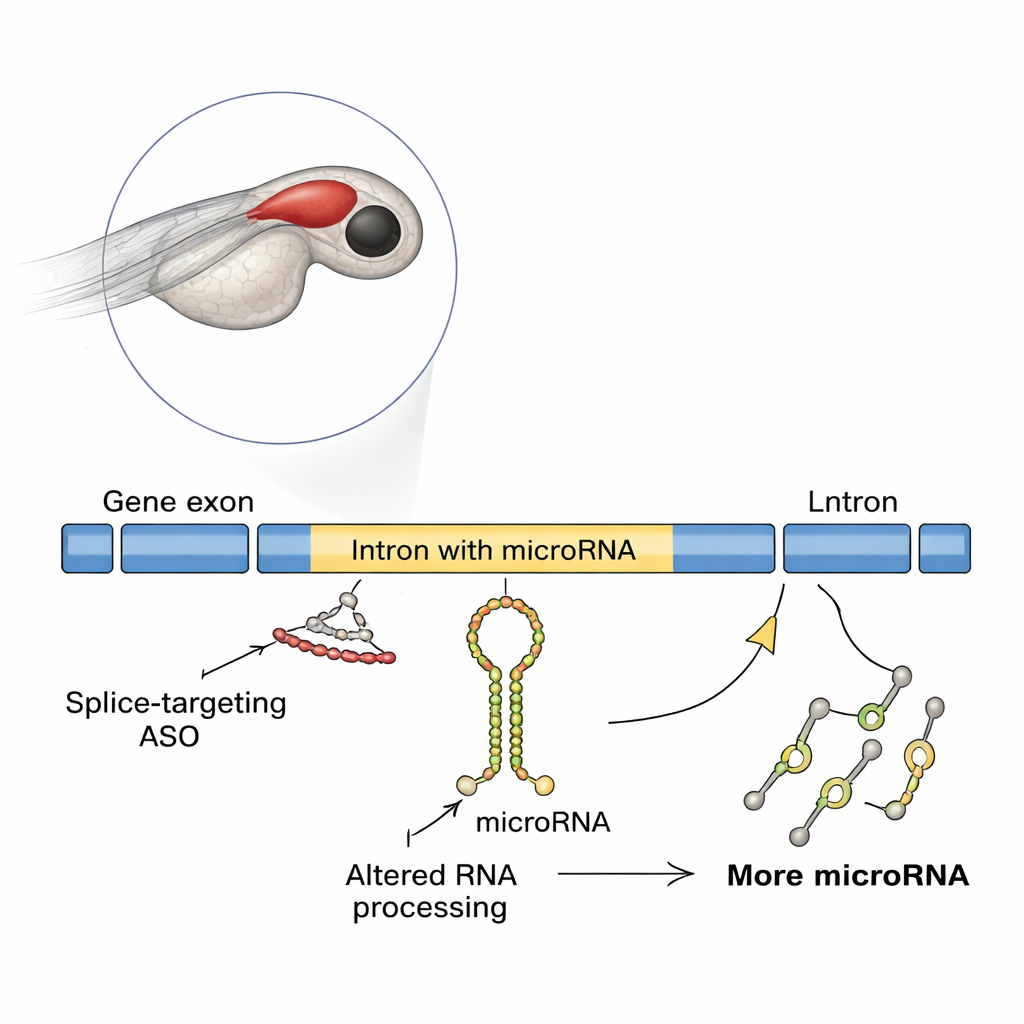
Zaskakujący efekt w rozwijającym się mózgu ryby
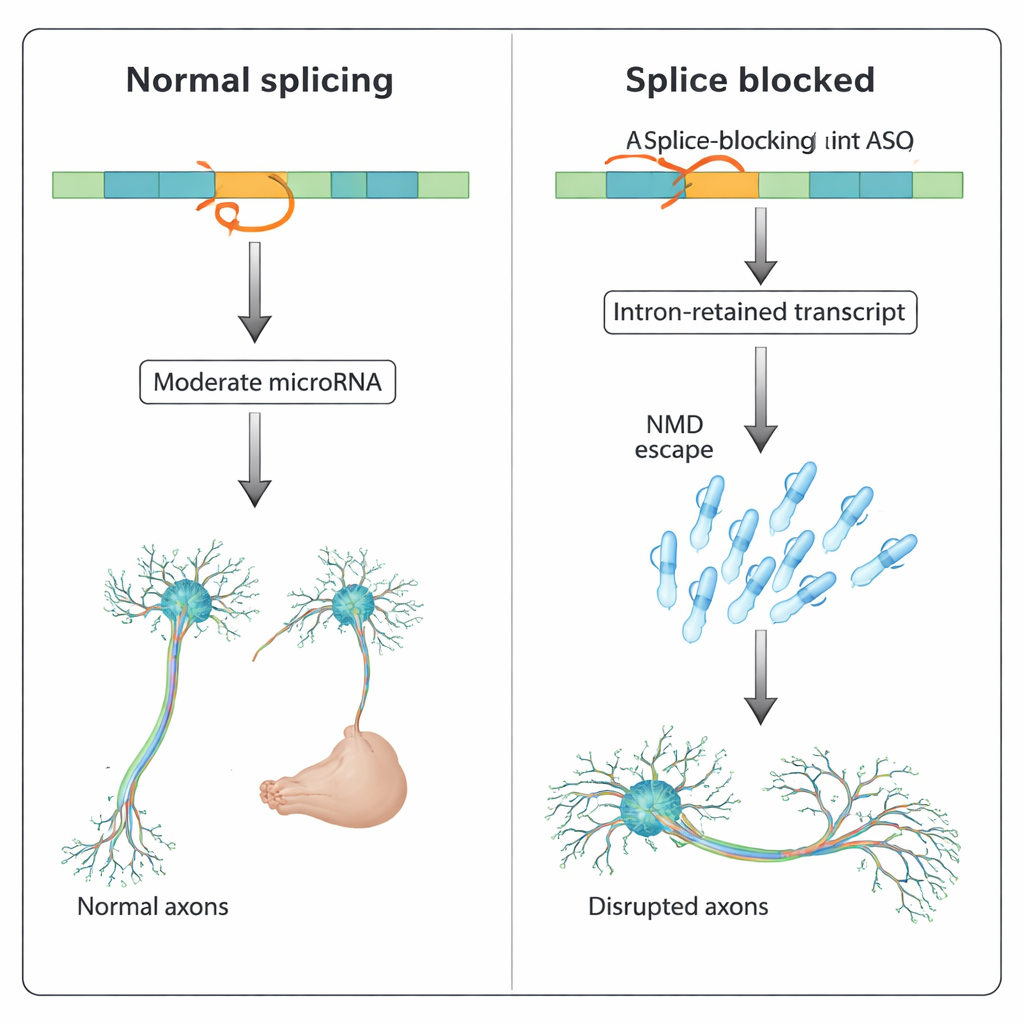
Naukowcy użyli danio pręgowanego, popularnego modelu kręgowca, którego przeźroczyste zarodki ułatwiają śledzenie rozwoju mózgu. Skoncentrowali się na genie nazwanym slit3, który pomaga prowadzić włókna nerwowe i zawiera microRNA mir-218a-1 osadzone w jednym z intronów. Gdy zablokowano inicjację translacji slit3, rozwój aksonów wydzielających hormony przysadki wyglądał normalnie. Jednak zastosowanie innego ASO, które blokowało splicing w konkretnym miejscu splicingu slit3, znacznie zmniejszyło liczbę aksonów kierujących się do tylnej części przysadki, mimo że liczba neuronów produkujących oksytocynę pozostała taka sama. Testy molekularne wykazały, że to ASO blokujące splicing powodowało retencję intronu w RNA genu, nieoczekiwanie zwiększając poziomy transkryptu slit3, jego długiego intronu oraz pierwotnego transkryptu intronowego mir-218a-1.
To microRNA, a nie utrata białka, napędza defekty
Aby rozdzielić przyczyny problemu z aksonami, autorzy porównali kilka scenariuszy. Zablokowanie samego dojrzałego mir-218a-1 nie zmieniało poziomów slit3, a oddzielne ASO celujące w inny miejsce splicingu blisko microRNA nie wywołało defektów aksonalnych ani nie podniosło poziomu mir-218a-1. Kluczowo, gdy ASO blokujące splicing slit3 połączono z ASO neutralizującym mir-218a-1, ułożenie aksonów w dużej mierze się przywróciło. Podobnie, u danio genetycznie pozbawionych mir-218a-1 to samo ASO blokujące splicing slit3 nie powodowało już defektów aksonalnych, podczas gdy wstrzyknięcie syntetycznego imitatu mir-218a mogło odtworzyć fenotyp u normalnych ryb. Te eksperymenty wskazują, że głównym czynnikiem zaburzenia rozwojowego jest podwyższone intronowe microRNA — a nie skrócone białko Slit3.
Szerszy wzorzec obejmujący wiele genów
Zespół zapytał następnie, czy efekt ten jest unikalny dla slit3. Przeszukali genom danio i znaleźli dziesiątki genów kodujących białka, które zawierają intronowe microRNA, z wieloma zaangażowanymi w rozwój i sygnalizację. Dwa takie geny, pank2 i dnm2a, wcześniej wykazywały poważne problemy rozwojowe po zablokowaniu ich splicingu przez ASO, w tym nagromadzenie płynu mózgowo‑rdzeniowego, powiększenie serca i deformacje ciała — problemy, których usunięcie tych genów przez knockout genetyczny nie odtwarzało. W tym badaniu współwstrzykiwanie ASO, które specyficznie blokowały intronowe microRNA mir-103 (w pank2) lub mir-199-5p (w dnm2a), częściowo ratowało te fenotypy wywołane przez ASO. W niektórych przypadkach blokada microRNA przywracała ekspresję genu gospodarza, w innych nie — co sugeruje, że zwiększona aktywność microRNA sama w sobie może być szkodliwa, nawet gdy ogólne zmiany poziomów są umiarkowane.
Co to oznacza dla przyszłych terapii
Wyniki ujawniają, że ASO ukierunkowane na splicing mogą powodować więcej niż pomijanie eksonów lub retencję intronów: mogą stabilizować transkrypty z zatrzymanym intronem, które uchodzą kontroli jakości komórkowej, i podnosić poziomy intronowych pierwotnych microRNA, które następnie błędnie regulują sieci genów docelowych. W rozwijających się neuronach taka niekontrolowana aktywność microRNA może zaburzać wzrost aksonów i ich łączność. Dla twórców leków oznacza to, że nietypowe lub „off‑targetowe” fenotypy w testach na zwierzętach niekoniecznie wynikają z ogólnych ścieżek toksyczności, takich jak aktywacja p53, lecz z niezamierzonych efektów na ukryte intronowe RNA. Dokładne porównanie ASO blokujących translację i tych blokujących splicing oraz monitorowanie ekspresji intronowych microRNA może pomóc wcześnie wykryć te ryzyka i dopracować projekty ASO, zanim trafią do pacjentów.
Cytowanie: Ali, M.H., Ramesh, A.R., Nedunchezhian, N. et al. Targeted blocking of gene splicing can dysregulate intron-embedded primary microRNAs. Commun Biol 9, 252 (2026). https://doi.org/10.1038/s42003-026-09529-7
Słowa kluczowe: oligonukleotydy antysensowne, microRNA, splicing RNA, rozwój danio pręgowanego, bezpieczeństwo terapii genowych