Clear Sky Science · pl
Nimbolide łagodzi ARDS i wrzodziejące zapalenie jelita grubego przez zakłócenie aktywacji inflamasomu NLRP3
Dlaczego powstrzymanie niekontrolowanego zapalenia ma znaczenie
Wiele poważnych chorób — od zagrażającej życiu niewydolności płuc po bolesne choroby jelit — napędzanych jest nie tylko przez drobnoustroje czy urazy, lecz także przez nadmierną reakcję własnego układu odpornościowego. Badanie to sprawdza, czy naturalny związek nimbolide, pozyskiwany z drzewa neem, może działać jak precyzyjny „hamulec” na jedną z potężnych maszyn zapalnych w komórkach odpornościowych, otwierając potencjalnie bezpieczniejszą drogę leczenia schorzeń takich jak ostra niewydolność oddechowa (ARDS) i wrzodziejące zapalenie jelita grubego.
Problemowy alarm wewnątrz komórek odpornościowych
W centrum tej opowieści znajduje się molekularny system alarmowy zwany inflamasomem NLRP3. Gdy komórki odpornościowe wyczuwają niebezpieczeństwo — sygnały z infekcji, uszkodzonych tkanek lub kryształów — może on składać się jak struktura z trzech części: czujnik NLRP3, adaptor ASC i enzym kaspaza‑1. Po zmontowaniu kompleks uruchamia silne przekaźnikowe molekuły, takie jak IL‑1β i IL‑18, oraz może wywołać zapalną formę śmierci komórki zwaną pyroptozą. Choć ta odpowiedź pomaga usuwać zagrożenia, jej nadmierna aktywacja przyczynia się do chorób przewlekłych i ostrych, w tym artretyzmu, powikłań cukrzycy, choroby Alzheimera, ARDS i zapalnych chorób jelit. Producenci leków próbowali ujarzmić NLRP3 za pomocą związków syntetycznych, lecz wiele kandydatów napotkało problemy związane z toksycznością, działaniami niepożądanymi lub nieodpowiednim zachowaniem w organizmie, co podkreśla potrzebę bezpieczniejszych i bardziej selektywnych inhibitorów.
Odkrycie silnego inhibitora pochodzenia roślinnego
Naukowcy przesiewali 126 naturalnych związków, aby sprawdzić, które najlepiej blokują uwalnianie IL‑1β z mysich komórek odpornościowych. Nimbolide wyróżnił się, zmniejszając wydzielanie IL‑1β o ponad 80% przy testowanych dawkach. Dalsze eksperymenty wykazały, że nimbolide silnie hamuje aktywację kaspazy‑1, uwalnianie IL‑1β oraz śmierć komórkową przez pyroptozę w makrofagach pochodzenia szpikowego myszy, z siłą porównywalną do leku referencyjnego MCC950. Co ważne, nimbolide nie tłumił uwalniania innych mediatorów zapalenia, takich jak IL‑6, co sugeruje działanie ukierunkowane, a nie ogólne wyciszenie odporności. Testowany przeciw różnym wyzwalaczom aktywującym NLRP3 — takim jak ATP, nigericyna, kryształy aluminiowe i imiquimod — nimbolide konsekwentnie zmniejszał aktywność inflamasomu, także w ludzkich komórkach THP‑1. Dla porównania, nie blokował dwóch pokrewnych inflamasomów, AIM2 i NLRC4, co podkreśla jego specyficzność wobec NLRP3.
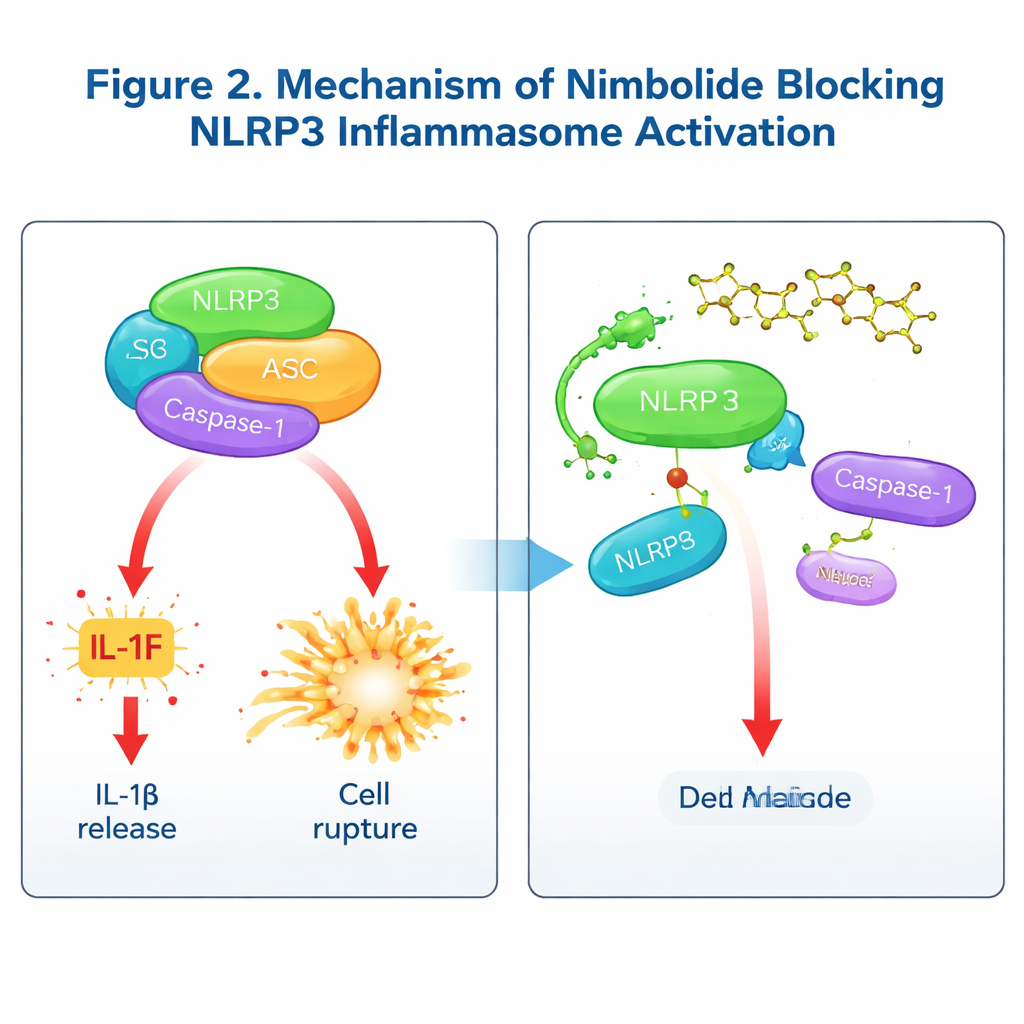
Jak nimbolide blokuje maszynę zapalną
Aby zrozumieć mechanizm działania nimbolide, zespół sprawdził, czy zakłóca wczesne etapy „primingu” kontrolowane przez szlak NF‑κB, czy późniejsze fazy, gdy inflamasom fizycznie się montuje. Krótkotrwałe podanie po primingu pozostawiło kluczowe sygnały primingu i ekspresję genów nietknięte, a jednocześnie zmniejszyło IL‑1β i aktywację kaspazy‑1, co pokazuje, że nimbolide działa głównie na etap składania kompleksu. Szczegółowe testy biochemiczne wykazały, że nimbolide nie zmienia przemieszczeń potasu ani wapnia, uszkodzeń mitochondriów ani interakcji NLRP3 z białkiem pomocniczym NEK7. Zamiast tego zakłóca kluczowe połączenie między NLRP3 a ASC, zmniejsza klastrowanie ASC w tzw. „specks” i uniemożliwia NLRP3 tworzenie wyższych porządków oligomerów. Dzięki testom wiązania i modelowaniu molekularnemu autorzy pokazali, że nimbolide bezpośrednio przyłącza się do regionu NACHT NLRP3 przy konkretnym aminokwasie, lizynie 565 (Lys565). Po zmutowaniu tego miejsca nimbolide nie był już w stanie chronić NLRP3 przed degradacją ani zerwać jego połączenia z ASC, potwierdzając Lys565 jako kluczowy punkt dokowania. Co istotne, podczas gdy inne leki często celują w aktywność ATPazy NLRP3, nimbolide hamuje składanie kompleksu bez wpływu na wykorzystanie ATP, oferując odmienny mechanizm działania.
Testy nimbolide w chorobach płuc i jelit
Zespół następnie sprawdził, czy ten efekt molekularny przekłada się na rzeczywistą ochronę w modelach chorobowych. U myszy, którym podano toksynę bakteryjną wywołującą ARDS, leczenie nimbolidem przed ekspozycją zmniejszyło uszkodzenie tkanki płucnej, gromadzenie się płynu i przeciek białka do przestrzeni powietrznych. W płucach było mniej napływających komórek odpornościowych oraz niższe poziomy IL‑1β zarówno w tkance płucnej, jak i we krwi. Podobne korzyści obserwowano w modelu, w którym toksyna była podana bezpośrednio drogami oddechowymi. W odrębnym modelu wrzodziejącego zapalenia jelita grubego, gdzie myszy otrzymywały chemiczny czynnik uszkadzający okrężnicę, nimbolide ograniczał utratę masy ciała, poprawiał konsystencję stolca i wyniki krwawienia, zachowywał długość okrężnicy oraz zmniejszał mikroskopowe oznaki zapalenia i erozji tkanek, równocześnie obniżając IL‑1β w okrężnicy. Co kluczowe, u myszy genetycznie pozbawionych NLRP3 choroba była już łagodniejsza, a nimbolide nie dawał dodatkowej korzyści, podkreślając, że jego efekt ochronny zależy od blokowania NLRP3.
Co to może oznaczać dla przyszłych terapii
Dla osób niebędących specjalistami najważniejsza lekcja jest taka: nimbolide działa jak inteligentny hamulec na jeden z najsilniejszych przełączników zapalnych organizmu. Przyłączając się do precyzyjnego miejsca na NLRP3 i zapobiegając składaniu się inflamasomu, łagodzi nadmierne zapalenie zarówno w płucach, jak i w jelitach, nie wyciszając przy tym szeroko układu odpornościowego. Choć sam nimbolide będzie wymagał jeszcze udoskonaleń w zakresie stabilności i sposobu podawania, zanim stanie się lekiem, praca ta stawia go jako obiecujący punkt wyjścia — i plan działania — do projektowania następnej generacji leków przeciwko chorobom napędzanym przez NLRP3, takim jak ARDS i wrzodziejące zapalenie jelita grubego.
Cytowanie: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
Słowa kluczowe: nimbolide, inflamasom NLRP3, zapalenie, ostra niewydolność oddechowa, wrzodziejące zapalenie jelita grubego