Clear Sky Science · pl
Badanie asocjacyjne w skali epigenomu poziomu interleukiny‑6 we krwi łączy metylację DNA ze zdrowiem immunometabolicznym i zapalnym
Dlaczego to ma znaczenie dla zdrowia codziennego
Przewlekłe, niskiego stopnia zapalenie cicho kształtuje ryzyko chorób takich jak cukrzyca typu 2, choroba serca czy zapalne choroby jelit. Kluczowym graczem w tym procesie jest białko sygnałowe we krwi zwane interleukiną‑6 (IL‑6). W niniejszym badaniu postawiono fundamentalne pytanie: w jaki sposób IL‑6 oddziałuje z naszym epigenomem — chemicznymi znacznikami na DNA, które pomagają kontrolować aktywność genów — i co to oznacza dla naszego długoterminowego zdrowia?
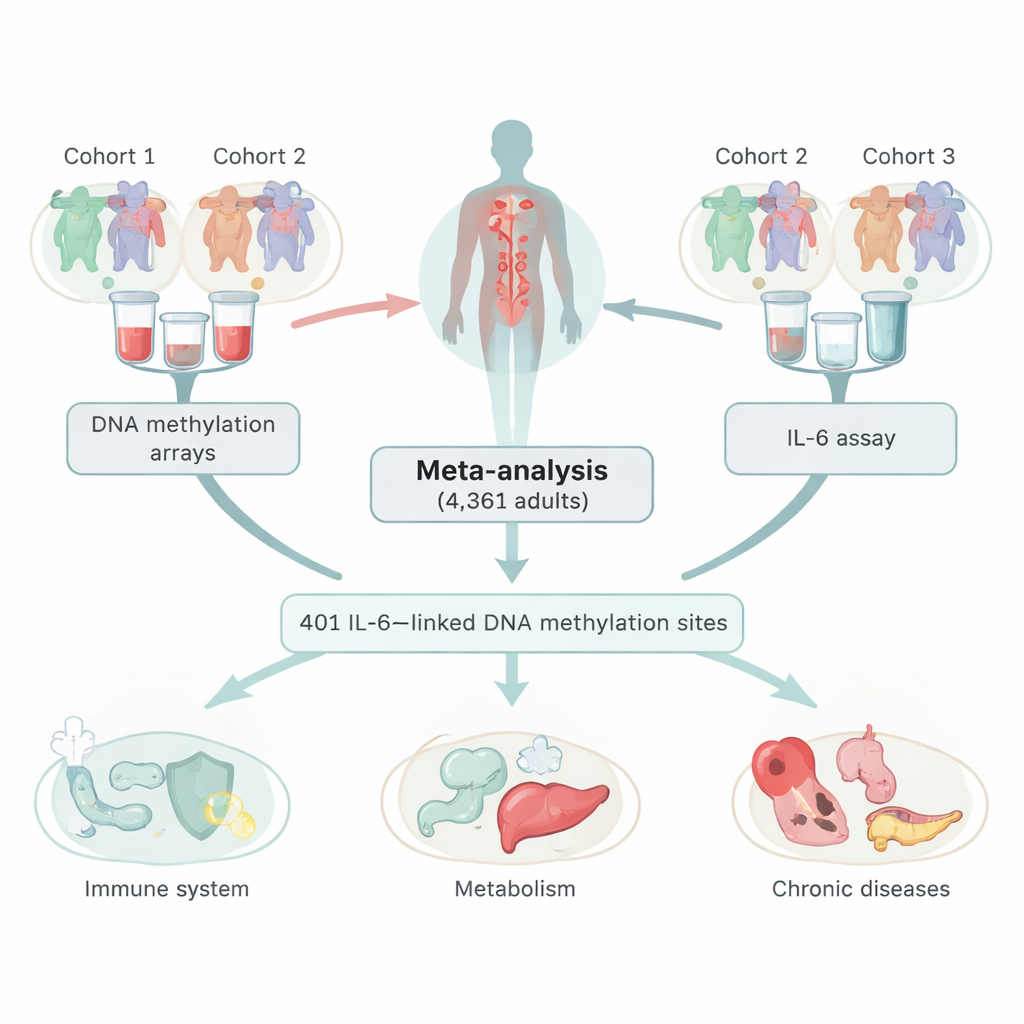
Spoglądając na chemiczne znaczniki na DNA
Naukowcy połączyli dane z trzech dużych badań europejskich obejmujących 4 361 dorosłych, którzy oddali próbki krwi. W tych próbkach zmierzono zarówno poziomy IL‑6, jak i metylację DNA — powszechny chemiczny znacznik na DNA, który może zwiększać lub zmniejszać aktywność genów bez zmiany sekwencji genetycznej. Przeskanowawszy ponad 400 000 miejsc w całym genomie, zidentyfikowali 401 lokusów, w których poziomy metylacji korelowały z ilością IL‑6 krążącej we krwi. Większość tych miejsc wykazywała odwrotny wzór: wyższe IL‑6 wiązało się z niższą metylacją w tych punktach. Zespół dokładnie sprawdził, że te powiązania nie były jedynie efektem palenia, różnic w typach komórek krwi ani innego markera zapalenia, białka C‑reaktywnego (CRP).
Łączenie zapalenia z metabolizmem i chorobami
Następnie autorzy sprawdzili, czy miejsca powiązane z IL‑6 nakładają się z sygnałami widzianymi w innych dużych badaniach epigenetycznych. Stwierdzili silne wzbogacenie cech o komponencie zapalnym lub metabolicznym, w tym wskaźnika masy ciała (BMI), lipidów we krwi, ciśnienia krwi, poziomu cukru, cukrzycy typu 2, przewlekłej choroby nerek oraz zaburzeń psychiatrycznych i związanych ze stresem. Wiele z tych samych miejsc metylacji było wcześniej powiązanych z CRP, lecz wzorce sugerowały, że IL‑6 i CRP niosą częściowo odrębne sygnatury epigenetyczne. Innymi słowy, chemiczne znaczniki związane z IL‑6 nie są jedynie wierną kopią tych związanych z CRP i mogą dostarczać dodatkowych informacji o stanie zapalnym i metabolicznym danej osoby.
Gdzie w genomie dzieje się działanie
Aby zrozumieć, co te miejsca metylacji mogą robić, zespół przypisał je do znanych regionów regulacyjnych genomu. Stwierdzono, że miejsca związane z IL‑6 koncentrowały się w aktywnych elementach kontrolnych, takich jak enhancer’y — odcinki DNA, które pomagają włącząć geny — zamiast w obszarach niemych. Miejsca te znajdowały się również w pobliżu sekwencji wiążących czynniki transkrypcyjne, które bezpośrednio regulują IL‑6 i odpowiedzi na stres, w tym NF‑κB, Atf4, CHOP i Nrf2. Łącząc dane o metylacji z dużymi zestawami danych ekspresji genów, badacze powiązali ponad 400 genów z miejscami związanymi z IL‑6. Wiele z tych genów leży w centrum kontroli odporności i metabolizmu, w tym SOCS3, IL6R, AIM2, IFI16, MTOR i RORC, i uczestniczy w szlakach napędzających aktywację oraz wykorzystanie energii w wyspecjalizowanym typie komórek T (komórkach Th17) zaangażowanych w przewlekłe choroby zapalne.
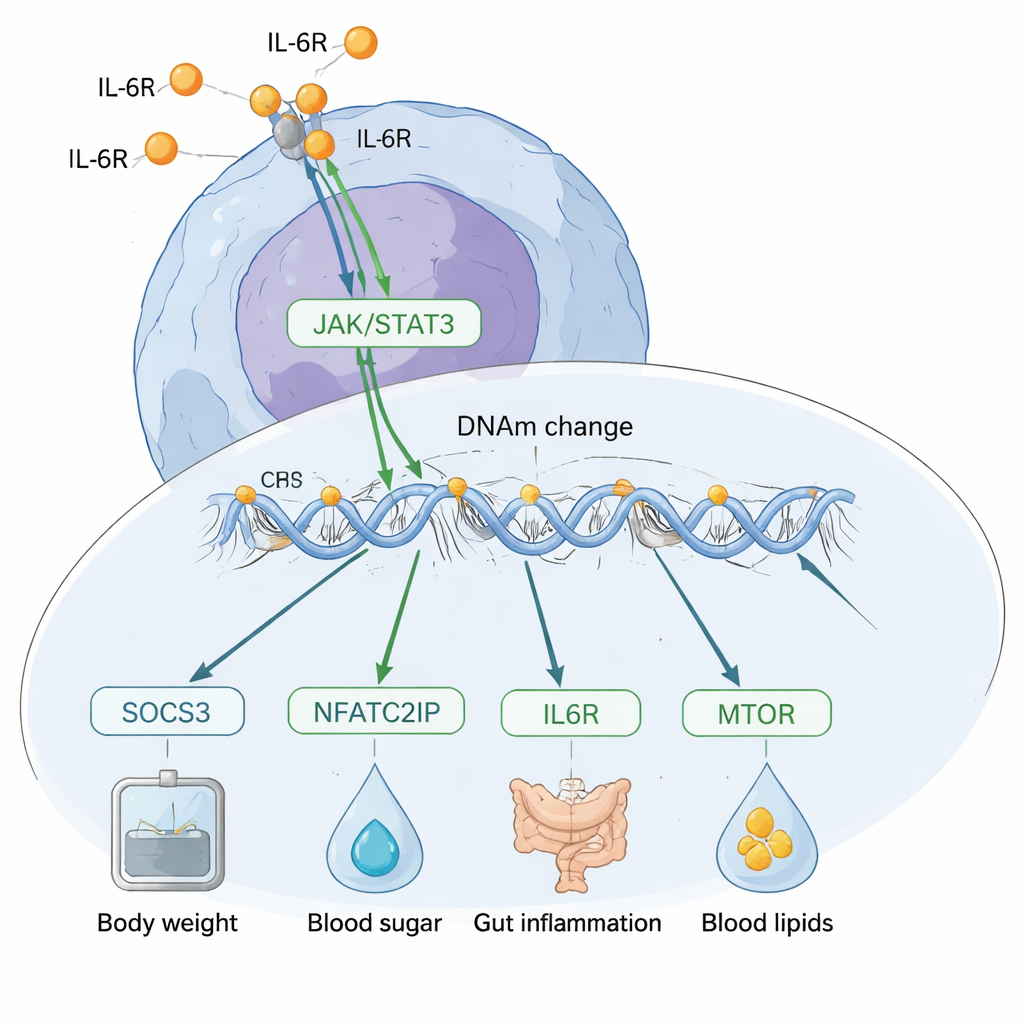
W którą stronę biegnie przyczyna i skutek?
Głównym wyzwaniem jest ustalenie, czy metylacja DNA powoduje zmiany w IL‑6, czy też IL‑6 przekształca metylację. Zespół zastosował kilka genetycznych metod, aby zbadać ten kierunek. W skali całego genomu ich analizy „triangulacyjne” wspierały model, w którym IL‑6 w większości przypadków napędza zmiany w metylacji DNA, a nie odwrotnie. Następnie przyjrzeli się bliżej konkretnym miejscom i stwierdzili, że zmiany metylacji w pobliżu genu SOCS3 wydają się pośredniczyć w wpływie IL‑6 na czynniki ryzyka takie jak masa ciała, poziom cholesterolu, poziom CRP i zapalne choroby jelit. Natomiast jedno wyróżniające się miejsce w pobliżu regulatora genowego o nazwie NFATC2IP wykazywało ślady wpływania na produkcję IL‑6 i wydawało się także oddziaływać na wiele stanów, w tym BMI, cukrzycę typu 2 i zapalenie jelit.
Co to oznacza dla przyszłej prewencji i leczenia
Dla czytelnika niebędącego specjalistą centralny przekaz jest taki, że IL‑6 i epigenetyczne znaczniki na DNA są ściśle powiązane w sposób mający wpływ na wiele powszechnych chorób. W większości przypadków IL‑6 zdaje się zostawiać chemiczny „odcisk” na genomie, szczególnie w komórkach odpornościowych, oznaczając i być może stabilizując stany prozapalne. W kilku kluczowych miejscach metylacja może natomiast pomagać ustalić, ile IL‑6 jest produkowane i jak silnie reagują szlaki odpornościowe. Te odkrycia wskazują, że wzorce metylacji DNA są obiecującymi wskaźnikami stanu zapalnego i zdrowia metabolicznego wykrywalnymi we krwi, oraz sugerują, że precyzyjnie ukierunkowane zmiany epigenetyczne — zwłaszcza wokół genów takich jak SOCS3 i NFATC2IP — mogłyby w przyszłości uzupełniać leki blokujące IL‑6 w zapobieganiu lub leczeniu chorób przewlekłych.
Cytowanie: Sinke, L., van Dongen, J., Delerue, T. et al. Epigenome-wide association study of circulating interleukin-6 connects DNA methylation to immunometabolic and inflammatory health. Commun Biol 9, 242 (2026). https://doi.org/10.1038/s42003-026-09520-2
Słowa kluczowe: interleukina‑6, metylacja DNA, zapalenie, choroby metaboliczne, epigenetyka