Clear Sky Science · pl
MAT2A zwiększa transkrypcję PARN przez SRF, przyspieszając glikolizę i napędzając złośliwy rozwój w mięsakach kości
Dlaczego to badanie nad rakiem kości ma znaczenie
Mięsak kości (osteosarcoma) jest najczęstszym nowotworem kości u dzieci i nastolatków, a metody leczenia praktycznie się nie zmieniły przez dekady. Wielu młodych pacjentów wciąż ma złe rokowania, zwłaszcza gdy nowotwór się rozsiewa lub opiera chemioterapii. To badanie ujawnia ukryty „włącznik główny” — białko o nazwie MAT2A — które pomaga komórkom osteosarcomy rosnąć, przebudowywać gospodarkę energetyczną i tworzyć agresywne guzy, oraz pokazuje, że lek ukierunkowany na MAT2A może spowalniać lub zmniejszać te guzy w modelach laboratoryjnych.
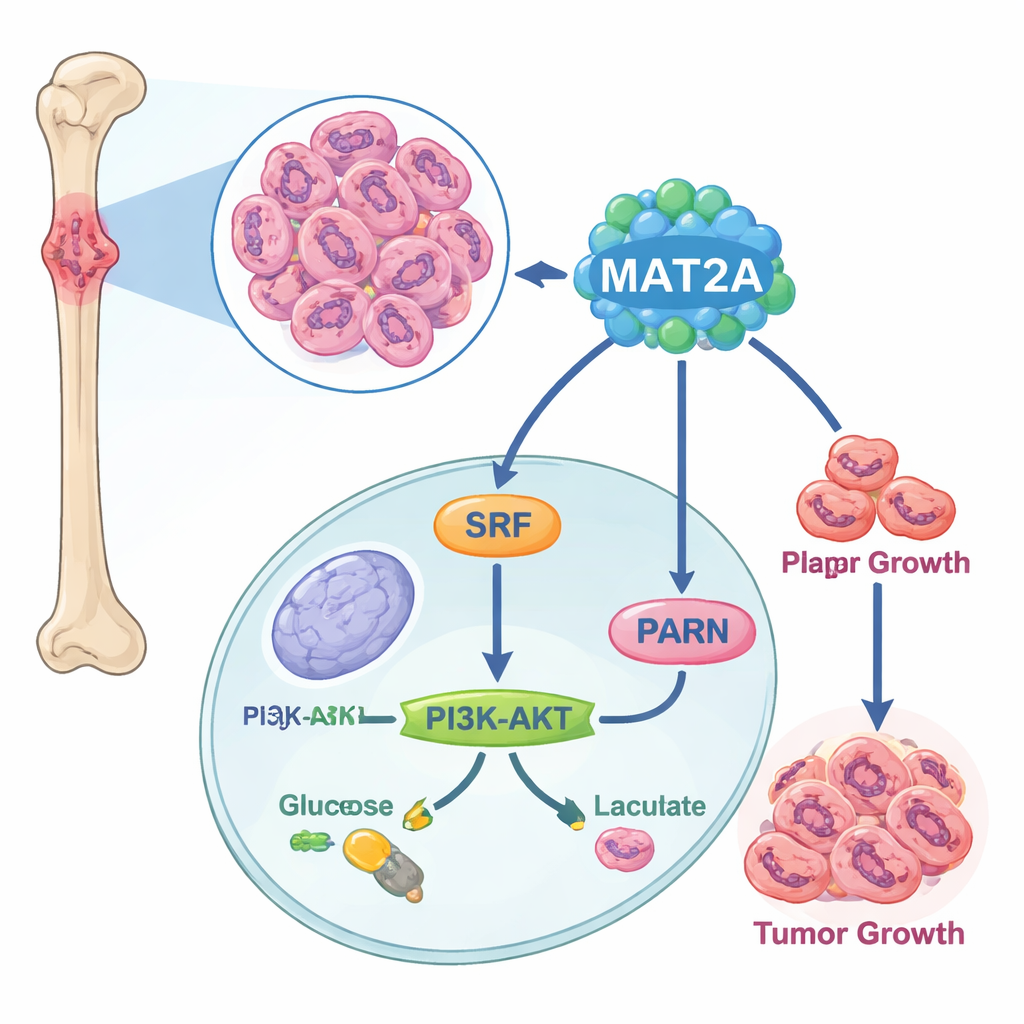
Ukryty silnik wewnątrz komórek nowotworowych
Naukowcy zaczęli od porównania próbek raka kości z normalną tkanką kostną na poziomie pojedynczych komórek. Stwierdzili, że tkanka osteosarcomy zawiera więcej komórek budujących guz i mniej komórek układu odpornościowego, oraz że jeden gen w szczególności — MAT2A — był nietypowo aktywny w komórkach nowotworowych. Analizy publicznych baz danych nowotworowych i hodowli komórkowych potwierdziły, że poziomy MAT2A były znacznie wyższe w osteosarcomie niż w zdrowych komórkach kostnych, a pacjenci z wyższym MAT2A mieli skłonność do bardziej zaawansowanej choroby i zajęcia węzłów chłonnych. Postawiło to MAT2A w centrum uwagi jako potencjalny czynnik napędzający chorobę, a nie tylko biernego obserwatora.
Wyłączenie MAT2A spowalnia wzrost nowotworu
Aby sprawdzić, jak ważne jest MAT2A dla zachowania guza, zespół użył narzędzi genetycznych do obniżenia poziomów MAT2A w liniach komórkowych osteosarcomy. Gdy MAT2A zostało wyciszone, komórki nowotworowe dzieliły się wolniej i częściej ulegały zaprogramowanej śmierci. U myszy, którym wszczepiono te zmodyfikowane komórki, guzy rosły znacznie wolniej i były istotnie mniejsze, mimo że masa ciała zwierząt pozostawała stabilna. Te eksperymenty wykazały, że komórki osteosarcomy silnie polegają na MAT2A zarówno w kwestii przeżycia, jak i zdolności do tworzenia guzów.
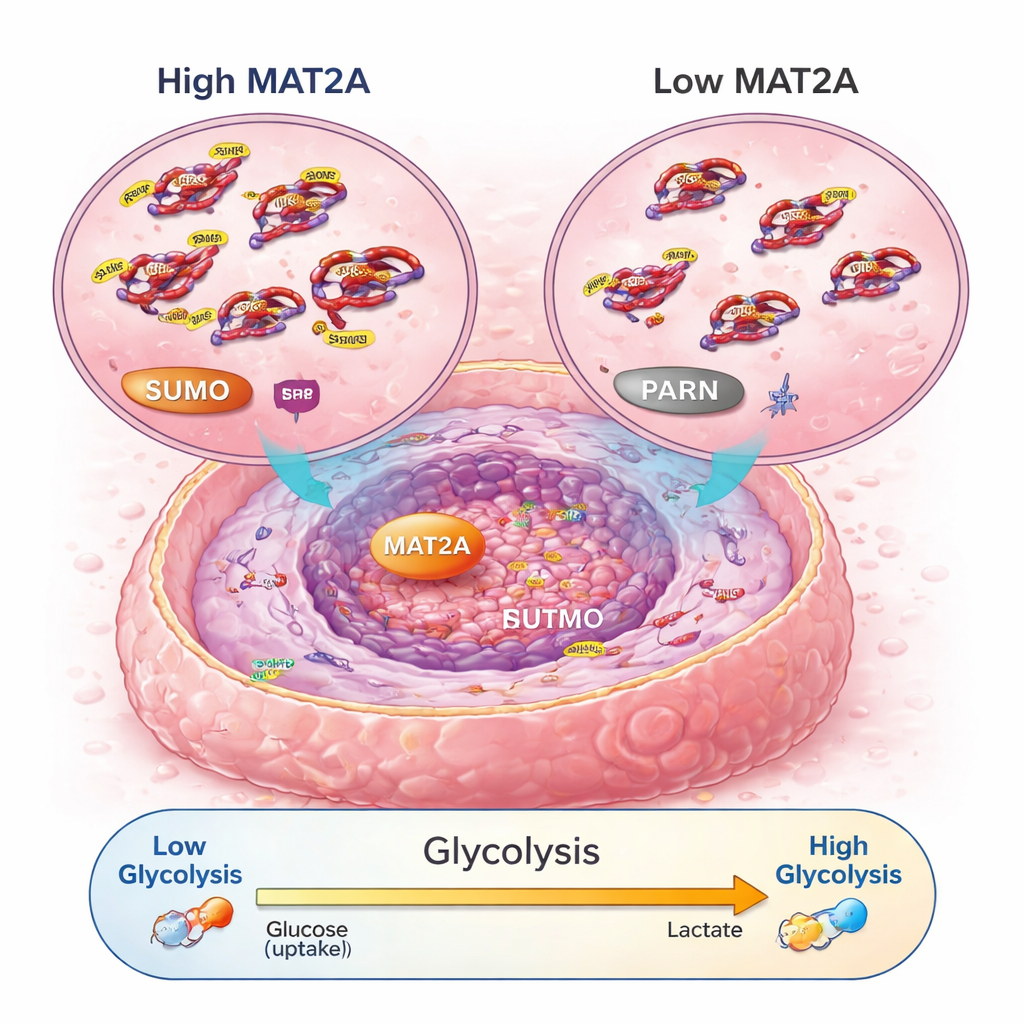
Przekaźnik sygnału, który zwiększa zużycie paliwa przez komórki
Badając mechanizmy głębiej, naukowcy odkryli, że MAT2A robi więcej niż tylko swoją zwykłą metaboliczną pracę. W jądrze komórkowym wiąże się z czynnikiem transkrypcyjnym o nazwie SRF, pomagając utrzymać SRF w stanie stabilnym i aktywnym poprzez promowanie modyfikacji SUMO. Z kolei SRF aktywuje gen PARN, który następnie uruchamia dobrze znany szlak PI3K–AKT i zwiększa maszyny odpowiedzialne za glikolizę tlenową — szybką, lecz mało wydajną drogę wytwarzania energii, którą preferują komórki nowotworowe. Gdy MAT2A zostało zmniejszone, komórki nowotworowe produkowały mniej ATP (waluty energetycznej), pobierały mniej glukozy, wytwarzały mniej kwasu mlekowego i przesuwały się z powrotem w stronę spokojniejszego, tlenowego oddychania. Zakłócenie PARN lub AKT mogło cofnąć efekty pro-wzrostowe i pro-glikolityczne MAT2A, potwierdzając, że ten przekaźnik — MAT2A → SRF → PARN → PI3K–AKT — działa jako kluczowy obwód energetyczny i wzrostowy w osteosarcomie.
Nietradycyjna rola i podatny na leki cel
Co zaskakujące, wersja MAT2A pozbawiona normalnej aktywności enzymatycznej nadal wspierała stabilność SRF i aktywację PARN, co oznacza, że ta sprzyjająca rakowi rola nie zależy od jego zwykłej reakcji chemicznej. Zamiast tego MAT2A działa bardziej jak rusztowanie organizujące inne białka. Ma to praktyczne implikacje: leki niekoniecznie muszą blokować centrum katalityczne, by osłabić guzy. Badacze przetestowali inhibitor małocząsteczkowy o nazwie FIDAS-5, zaprojektowany do oddziaływania z MAT2A, zarówno w hodowlach komórkowych, jak i modelach mysich. Leczenie zmniejszyło poziom SRF w jądrze, obniżyło sygnalizację PARN i PI3K–AKT, stłumiło glikolizę, spowolniło wzrost komórek i wywołało śmierć komórek nowotworowych. U myszy FIDAS-5 zmniejszył lub spowolnił rozwój guzów bez zauważalnej utraty masy ciała, co sugeruje tolerowalne skutki uboczne w tym układzie.
Co to oznacza dla pacjentów i przyszłych terapii
Dla osób niebędących specjalistami główne przesłanie jest takie, że komórki osteosarcomy polegają na MAT2A, aby utrzymać swoje programy wzrostu i silniki spalania cukru na pełnych obrotach. Stabilizując kluczowe białka kontrolne i wzmacniając łańcuch sygnałów, MAT2A pomaga guzom rosnąć szybciej i stawać się bardziej agresywnymi. Zablokowanie tego białka — zarówno metodami genowymi, jak i za pomocą leku takiego jak FIDAS-5 — odcina to wsparcie, zmuszając komórki nowotworowe do zwolnienia tempa, mniej intensywnego spalania energii i ostatecznie do śmierci. Chociaż przed wprowadzeniem takich terapii do kliniki wciąż wiele pracy, badanie to stawia MAT2A jako obiecujący nowy cel w walce z rakiem kości, otwierając potencjalną drogę do bardziej precyzyjnych i mniej toksycznych metod leczenia dla młodych pacjentów.
Cytowanie: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
Słowa kluczowe: mięsak kości, MAT2A, metabolizm nowotworowy, szlak PI3K AKT, terapia celowana