Clear Sky Science · pl
Analiza heterogenności epitopów w immunobarwieniach na podstawie serii rozcieńczeń przeciwciał
Dlaczego jakość barwienia przeciwciał ma znaczenie
Od śledzenia komórek nowotworowych po diagnozowanie infekcji — współczesna biologia w dużej mierze polega na przeciwciałach, które „rozświetlają” określone cząsteczki w komórkach. Tymczasem wiele laboratoriów boryka się z cichym problemem: barwienia bywają zbyt słabe, zbyt zaszumione lub po prostu mylące. W artykule przedstawiono praktyczne, komputerowe podejście do wydobycia większej ilości informacji z rutynowej serii rozcieńczeń przeciwciał, które pomaga badaczom dostroić barwienie dla uzyskania czystszych obrazów, bardziej wiarygodnych pomiarów, a nawet nowych sposobów znakowania kilku celów w jednym kanale koloru. 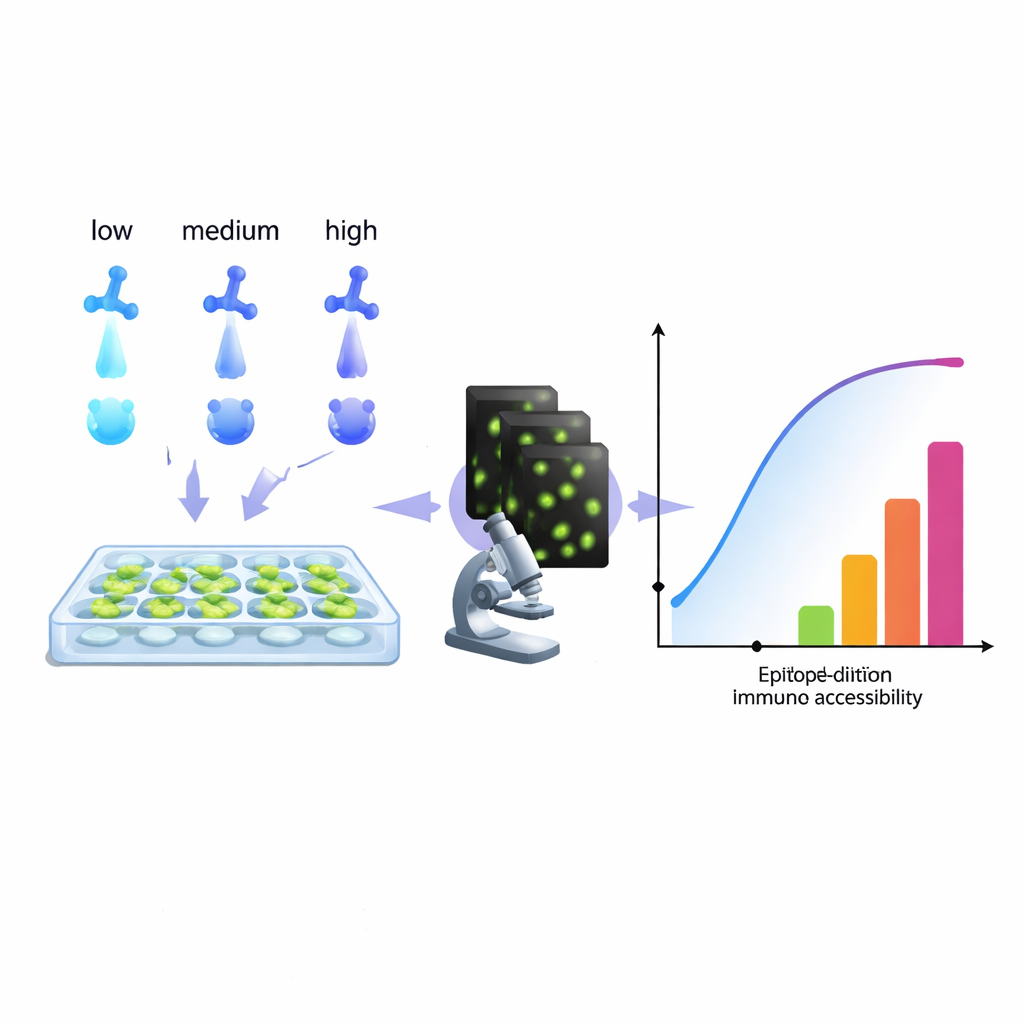
Jak naukowcy zwykle dobierają stężenia przeciwciał
Przy przygotowywaniu eksperymentu immunobarwienia badacze zazwyczaj sugerują się kartą katalogową przeciwciała, próbują kilku rozcieńczeń i wybierają to, które „wygląda dobrze”. W rzeczywistości jednak niezliczone drobne czynniki — kształt białka, zagęszczenie w komórce, pH i to, jak dobrze przeciwciało może się wcisnąć — decydują, czy przeciwciało się przyczepi, czy zostanie zmyte. Tradycyjne narzędzia mierzące wiązanie przeciwciał, takie jak powierzchniowy rezonans plazmonowy, działają najlepiej na oczyszczonych białkach na sztucznych powierzchniach, a nie na gęsto upakowanych komórkach lub tkankach. Oznacza to, że liczby przez nie podawane mogą nie odzwierciedlać rzeczywistego systemu biologicznego, w którym przeciwciało jest stosowane. W efekcie laboratoria mogą nieświadomie wybierać stężenia, które zwiększają rozmyte tło lub ukrywają ważne, ale mniej dostępne cele.
Przekształcanie prostych serii rozcieńczeń w „mapy dostępności”
Autorzy proponują inne podejście: traktować standardową serię rozcieńczeń przeciwciała jako bogaty zbiór danych i dopasować go modelem odzwierciedlającym to, co naprawdę widzi mikroskop — przeciwciała, które pozostają związane nawet po wielokrotnym myciu. Analizując, jak sygnał rośnie wraz ze stężeniem, ich algorytm rekonstruuje „histogram dostępności”. Zamiast próbować wydzielić czyste stałe chemiczne wiązania, histogram ten grupuje miejsca docelowe w techniczne „klasy epitopów” na podstawie tego, jak łatwo dają się zabarwić w rzeczywistych warunkach. Pojedynczy epitope biologiczny może pojawić się w różnych klasach, jeśli na przykład w jednym miejscu komórki jest łatwo dostępny, a w zatłoczonej przestrzeni trudniej go zabarwić. Co istotne, ta metoda działa bezpośrednio na danych z mikroskopu, bez potrzeby oczyszczonych białek czy dodatkowego sprzętu, więc każde laboratorium, które może przeprowadzić serię rozcieńczeń i zmierzyć fluorescencję, w zasadzie może zbudować takie histogramy. 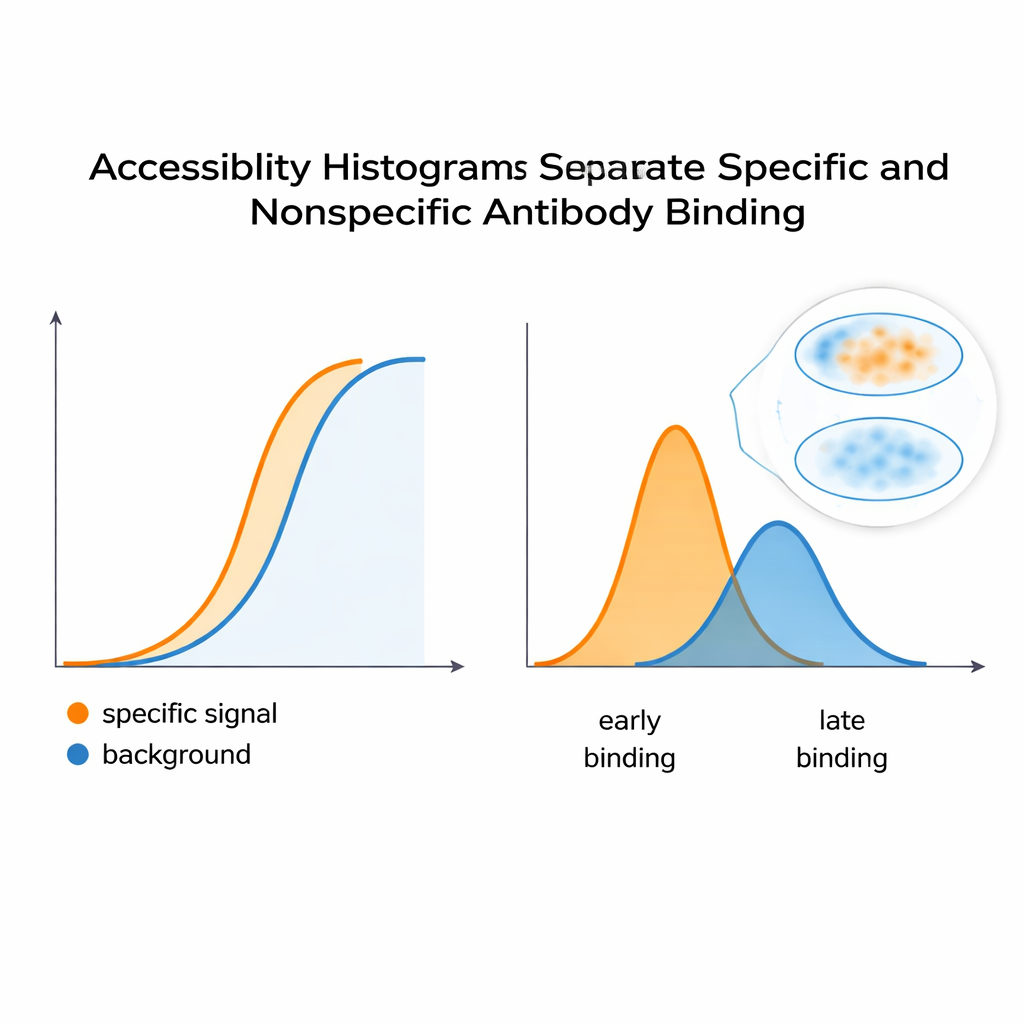
Oddzielanie prawdziwego sygnału od tła
Aby sprawdzić, czy te histogramy rzeczywiście odzwierciedlają zachowanie barwienia, zespół zbudował kontrolowany układ używając komórek HeLa i dwóch przeciwciał monoklonalnych: jednego imitującego pożądany, specyficzny sygnał i drugiego działającego jak niechciane tło. Po zmieszaniu skurczona krzywa fluorescencji wyglądała jak pojedyncza, gładka odpowiedź — nic nie sugerowało dwóch odrębnych wkładów. Jednak analiza obliczeniowa podzieliła tę krzywą na oddzielne piki w histogramie dostępności, ujawniając przynajmniej dwie leżące u podstaw klasy epitopów. Podobna strategia zastosowana do przeciwciała rozpoznającego miejsce wrażliwe na kształt w podjednostce regulacyjnej PKA wykazała, że zmiany konformacji białka — wywołane przez cząsteczkę zwaną cAMP — przesuwają rozkład dostępnych epitopów. To sugeruje, że metoda może wykrywać, kiedy struktury białkowe otwierają się lub zamykają, zmieniając łatwość wiązania przeciwciał wewnątrz komórek.
Wybieranie lepszych rozcieńczeń i barwienie więcej przy użyciu jednego koloru
Ponieważ każdy pik w histogramie dostępności dominuje przede wszystkim w określonym zakresie stężeń, autorzy wykorzystują te piki jako wskazówkę do wyboru „optymalnych” rozcieńczeń. Piki o niskiej dostępności, pojawiające się dopiero przy bardzo wysokich stężeniach przeciwciała, prawdopodobnie obejmują wiązanie nieswoiste, podczas gdy wczesne piki często odzwierciedlają zamierzony cel. Modelując, jak poszczególne piki budują łączną krzywą odpowiedzi na dawkę, zespół może zasugerować rozcieńczenia maksymalizujące sygnał specyficzny zanim pojawią się problematyczne piki — czasem znacznie bardziej rozcieńczone niż zalecenia producenta. Rozwijają też ten pomysł w sprytną formę „obliczeniowego multiplexowania”. Barwiąc tę samą utrwaloną próbkę wielokrotnie wybranymi stężeniami, obrazując po każdej rundzie i odejmując wcześniejsze obrazy od późniejszych, izolują sygnały związane z różnymi klasami dostępności, skutecznie rozdzielając wiele celów w jednym kanale fluorescencji.
Co to oznacza dla codziennej pracy w laboratorium
Mówiąc prosto, praca ta przekształca rutynowy krok rozwiązywania problemów — wykonanie serii rozcieńczeń przeciwciała — w narzędzie ilościowe. Histogramy dostępności pomagają naukowcom dostrzec ukrytą złożoność w ich barwieniach, wybrać rozcieńczenia, które redukują mylące tło, oraz w niektórych przypadkach rozdzielić nakładające się sygnały bez potrzeby stosowania dodatkowych znaczników fluorescencyjnych. Choć model leżący u podstaw jest celowo prosty i nie oddaje każdego molekularnego detalu, został zaprojektowany tak, by być łatwym w użyciu i wystarczająco odpornym na dane z rzeczywistych eksperymentów. Jeśli podejście to zostanie szeroko przyjęte, może uczynić techniki oparte na przeciwciałach — od podstawowego obrazowania po testy diagnostyczne — bardziej niezawodnymi, informacyjnymi i mniej zależnymi od prób i błędów.
Cytowanie: Tschimmel, D., Saeed, M., Milani, M. et al. Computational epitope heterogeneity analysis in immunostainings from antibody-dilution series. Commun Biol 9, 238 (2026). https://doi.org/10.1038/s42003-026-09517-x
Słowa kluczowe: barwienie przeciwciał, immunofluorescencja, dostępność epitopu, odpowiedź na dawkę, obliczeniowe multiplexowanie