Clear Sky Science · pl
Strategiczne postępy w badaniach strukturalnych małych (<100 kDa) GPCR przy użyciu krio-EM
Dlaczego małe „wyłączniki” komórkowe mają znaczenie dla medycyny
Wiele współczesnej medycyny działa przez dyskretne podrażnianie małych przełączników osadzonych w błonach komórkowych — receptorów sprzężonych z białkiem G (GPCR). Te przełączniki wyczuwają hormony, zapachy i leki, a około jedna trzecia wszystkich zatwierdzonych leków działa na nie. Aby projektować bezpieczniejsze i inteligentniejsze leki, naukowcy potrzebują szczegółowych, trójwymiarowych obrazów tych receptorów, zwłaszcza w ich formach „wyłączonych” (nieaktywnych), na które wiele leków jest skierowanych. Artykuł wyjaśnia, jak badacze uczą się obserwować niektóre z najmniejszych GPCR za pomocą krioelektronowej mikroskopii (krio‑EM) — potężnej metody obrazowania cząsteczek zamrożonych w stanie zbliżonym do naturalnego.
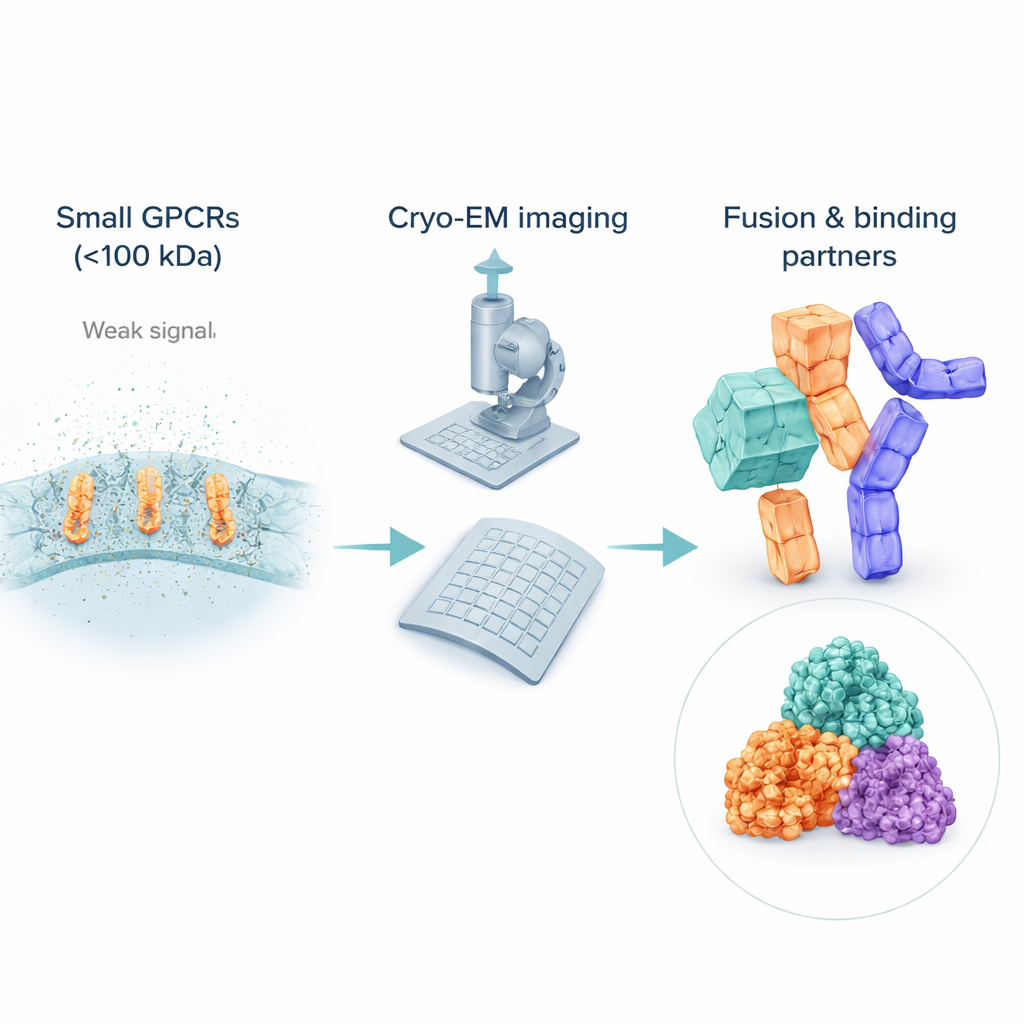
Trudność w obserwowaniu bardzo małych receptorów
Chociaż krio‑EM zrewolucjonizowała biologię strukturalną, wciąż ma problemy z małymi, elastycznymi cząsteczkami. Wiele nieaktywnych GPCR waży znacznie poniżej 100 kilodaltonów, co utrudnia ich wykrywanie i wyrównywanie w zaszumionych obrazach. Aby zachować je w stanie rozpuszczalnym, naukowcy otaczają te receptory pęcherzykami detergentowymi lub substytutami lipidów, które dla wiązki elektronów mogą wyglądać „większe” niż sam receptor, tłumiąc sygnał białka. W przeciwieństwie do aktywnych receptorów związanych z masywnymi partnerami, takimi jak białka G, nieaktywne GPCR często nie mają wyraźnych zewnętrznych cech, więc algorytmy komputerowe mają trudności z uśrednieniem wielu obrazów do ostrego widoku 3D. W efekcie większość struktur nieaktywnych GPCR pochodzi nadal z starszych metod rentgenowskich, pozostawiając lukę w pokryciu krio‑EM tam, gdzie działają liczne leki.
Powiększanie receptorów przy pomocy wbudowanych pomocników
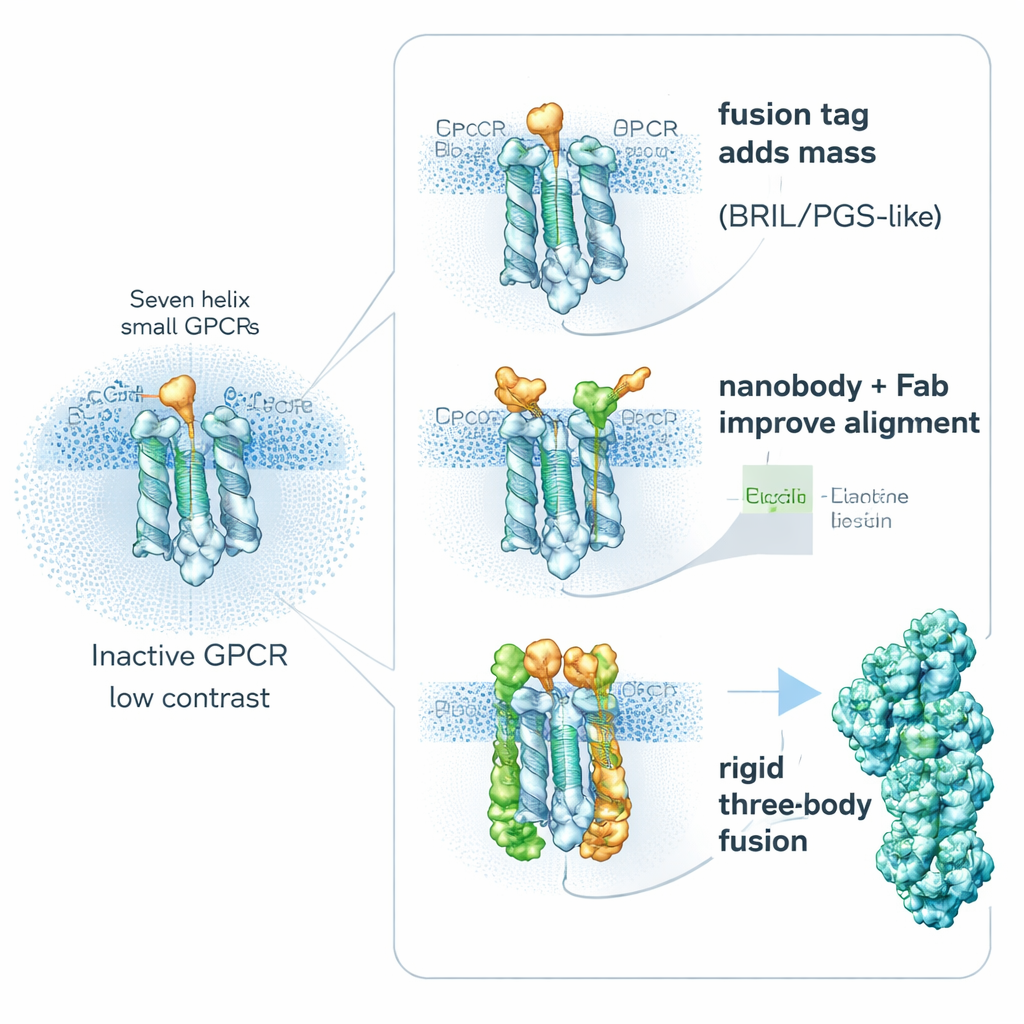
Jedna kluczowa strategia jest zaskakująco prosta: celowo „obciążyć” receptor, zwiększając jego masę. Badacze genetycznie łączą małe, stabilne białka pomocnicze z ruchliwymi fragmentami GPCR, aby zwiększyć ich rozmiar i sztywność, nie blokując istotnych miejsc wiązania leków. Popularne pomocniki to BRIL (wiązanie czterech helis), PGS (termostabilny fragment enzymu) oraz większe białko w formie zacisku, takie jak kalcyneuryna. Partnerzy fuzyjni są często wstawiani do ruchomej wewnętrznej pętli łączącej dwie helisy. Usztywniając ten obszar, zmniejszają rozmycie wynikające z ruchu molekularnego i zapewniają rozpoznawalne kształty, które pomagają komputerom wyrównywać cząstki. Badania pokazują, że dokładne położenie i orientacja fragmentu fuzyjnego może przesądzić o powodzeniu projektu: w jednym receptorze inaczej umieszczony znacznik PGS poprawił rozdzielczość z rozmytych 6 angstremów do znacznie jaśniejszych 3,7 angstremów.
Wypożyczanie przeciwciał i zaprojektowanych łączników jako uchwyty
Druga droga unika wprowadzania dużych fuzji do receptora i zamiast tego dołącza z zewnątrz wysokoafine „uchwyty”. Maleńkie fragmenty przeciwciał zwane nanobiałkami oraz pokrewne łączniki można wytworzyć tak, by rozpoznawały nieaktywne GPCR i przyczepiały się do ruchomych wewnętrznych pętli. Przykładem jest Nanobody‑6, stworzony początkowo jako czujnik dla jednego receptora opioidowego, a następnie ponownie użyty, po drobnych modyfikacjach, do stabilizacji kilku innych GPCR w ich formach nieaktywnych. Ponieważ wiąże się off‑center, dostarcza każdej cząstce wyraźną wskazówkę orientacji, co ułatwia uśrednianie obrazów. Badacze często rozszerzają ten pomysł, dodając drugą warstwę — zwykły fragment przeciwciała rozpoznający sam nanobiałko — tworząc masywniejszy, bardziej sztywny kompleks, który ostro pokazuje się w krio‑EM. Inne zaprojektowane łączniki, takie jak DARPiny, mogą służyć jako modułowe dystanse lub łączniki do większych białkowych klatek, dalej wzmacniając sygnał z bardzo małych celów.
Sprytniejszy projekt próbki i przetwarzanie obrazów wspomagane AI
Łączenie pomocników czy dodawanie łączników to tylko część opowieści. Przegląd podkreśla, że dobre struktury zaczynają się od starannie zaprojektowanych konstrukcji receptorów: przycinania włóknistych końców, wprowadzania stabilizujących mutacji i wykorzystania nowoczesnych narzędzi do przewidywania struktur, by zidentyfikować części mogące sprawiać problemy. Po stronie obrazowania starsze sztuczki, takie jak płyty fazowe zwiększające kontrast dla słabych cząstek, są uzupełniane lub nawet zastępowane przez narzędzia sztucznej inteligencji. Programy głębokiego uczenia potrafią wyłapywać malutkie cząstki ukryte w zaszumionych mikrographach, a nowe algorytmy mogą sortować obrazy według różnych kształtów, gdy receptory przyjmują wiele konformacji. W połączeniu z pomocnikami punktowymi te postępy przesuwają krio‑EM w kierunku niezawodnego rozróżniania białek błonowych, które dawniej uważano za zbyt małe lub zbyt dynamiczne do badania.
Co to oznacza dla przyszłych leków
Artykuł konkluduje, że nie istnieje pojedynczy „magiczy” pomocnik działający dla wszystkich receptorów, ale rozrastające się narzędzie skrzynkowe partnerów fuzyjnych, łączników przypominających przeciwciała i metod napędzanych AI stopniowo otwiera nieaktywny krajobraz GPCR dla krio‑EM. Dla laików kluczowy wniosek jest taki, że sprawiając, by małe receptory wyglądały na większe i bardziej uporządkowane dla mikroskopu, naukowcy wreszcie mogą uzyskać szczegółowe migawki dokładnych kształtów, do których wiele leków preferencyjnie się wiąże. Te strukturalne plany powinny przyspieszyć projektowanie leków, które precyzyjniej wyłączają te komórkowe przełączniki — lub subtelnie regulują ich aktywność — z mniejszą liczbą efektów ubocznych.
Cytowanie: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
Słowa kluczowe: receptory sprzężone z białkiem G, kriomikroskopia elektronowa, odkrywanie leków, biologia strukturalna, rusztowania nanobiałkowe