Clear Sky Science · pl
Łączenie napięcia molekularnego i trakcji komórkowej: wieloskalowe podejście do mechaniki ognisk adhezyjnych
Jak komórki wyczuwają i pociągają swoje otoczenie
Za każdym razem, gdy komórka się porusza, dzieli lub przekształca tkankę, potajemnie szarpie swoje otoczenie. Te mikroskopijne pociągnięcia mechaniczne są kluczowe w gojeniu ran, rozsiewie nowotworów i rozwoju narządów, a jednocześnie trudno je zobaczyć, a jeszcze trudniej zmierzyć. Niniejsze badanie przedstawia nowy sposób obserwacji tych sił z dwóch perspektyw jednocześnie: jak silnie cała komórka ciągnie po miękkim materiale oraz jak duże siły przenoszą poszczególne „sprężyny molekularne” wewnątrz miejsc kotwiczenia komórki. Łącząc te widoki, praca pomaga wyjaśnić, jak komórki odczuwają sztywność i regulują swoje przyczepienie do otoczenia.
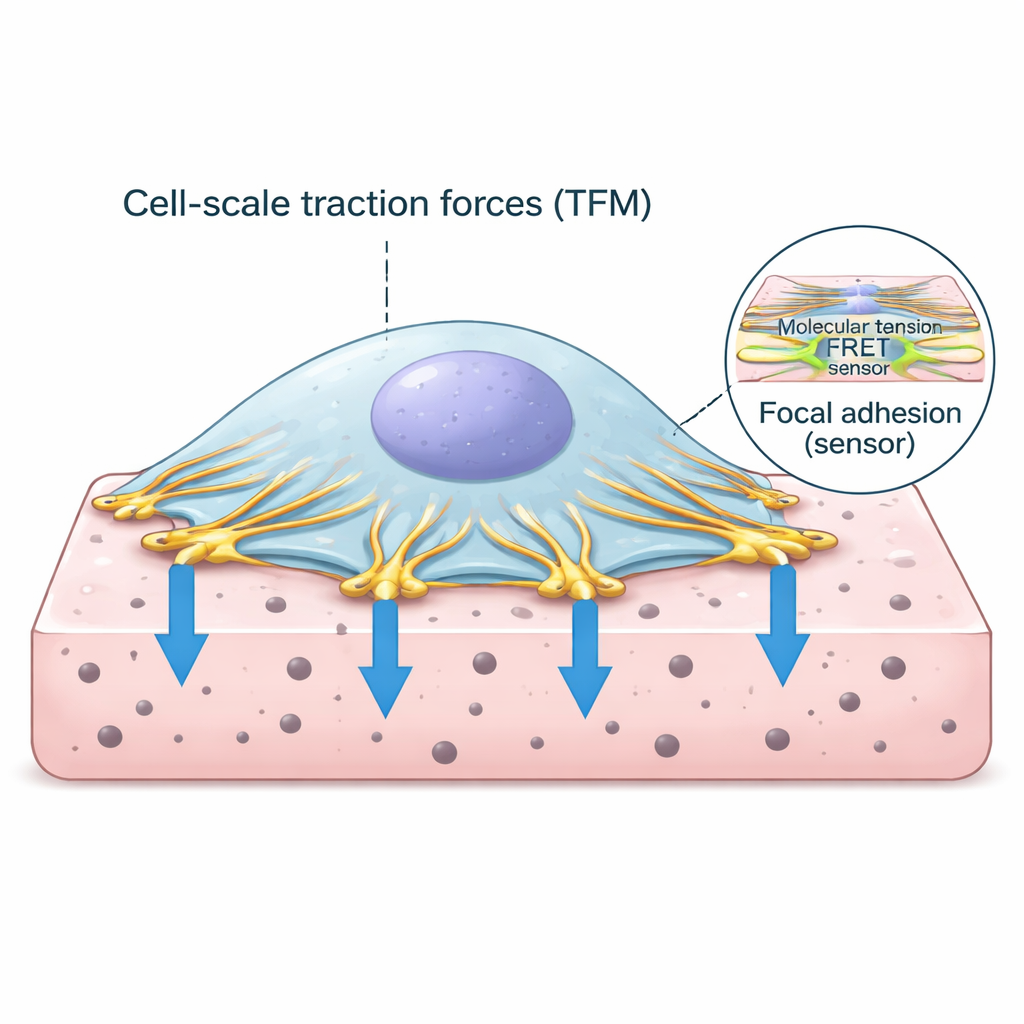
Punkty uchwytu komórki na zewnętrznym świecie
Komórki nie unoszą się po prostu w tkankach; zakotwiczają się za pomocą wyspecjalizowanych punktów kontaktowych zwanych ogniskami adhezyjnymi. W tych miejscach wewnętrzny szkielet komórki złożony z włókien aktynowych łączy się z białkami przebiegającymi przez błonę komórkową i zaczepiającymi się o macierz zewnątrzkomórkową. Jednym z kluczowych białek w tym kompleksie kotwiczącym jest winculina, która zachowuje się jak ogniwo wrażliwe na siłę. Gdy kurczliwy aparat komórki napina aktynę, winculina odczuwa obciążenie i pomaga wzmocnić połączenie. Zrozumienie, ile siły przechodzi przez te ogniwa i jak to się odnosi do ogólnego pociągania komórki, jest kluczowe dla rozszyfrowania, jak tkanki zachowują zdrowie lub stają się chore.
Dwa okna na siłę komórkową
Naukowcy połączyli dwie potężne techniki w jednym przepływie pracy. Po pierwsze, mikroskopia sił trakcyjnych mierzy, jak bardzo komórka odkształca miękki, żelopodobny podkład, śledząc ruch małych fluorescencyjnych kulek w żelu. Na podstawie tych przesunięć kulek można obliczyć rozkład sił pchających i ciągnących pod komórką. Po drugie, specjalnie zaprojektowane białko winculiny niesie fluorescencyjny czujnik napięcia, który zmienia sygnał świetlny, gdy się rozciąga. Z wykorzystaniem zaawansowanego obrazowania czasu życia (lifetime imaging) zespół przekształcił ten sygnał świetlny w odczyt napięcia molekularnego przy winculinie. Zaprojektowali cienkie, płaskie hydrożele, które można było obrazować z wysoką rozdzielczością, oraz napisali niestandardowe oprogramowanie do wyrównywania, segmentacji i analizy obu zestawów danych aż do pojedynczych miejsc adhezji.
Jak sztywność zmienia wysiłek komórki
Gdy komórki hodowano na miękkich w porównaniu z twardszymi żelami, ich ogólne zachowanie zmieniało się w wyraźny sposób. Na sztywniejszych podłożach komórki bardziej się rozprzestrzeniały i wywierały silniejsze siły trakcyjne na powierzchnię żelu. Jednocześnie fluorescencyjny odczyt z czujnika winculiny wskazywał wyższe napięcie molekularne w ogniskach adhezyjnych. Co ciekawe, podstawowe cechy strukturalne tych ognisk—takie jak ich liczba czy średni rozmiar—nie zmieniały się znacznie między miękkimi a sztywnymi żelami. Zamiast tego zmienił się sposób organizacji sił. Duże, promieniście ułożone ogniska z większą ilością winculiny miały tendencję do przenoszenia wyższych trakcji, co sugeruje, że zarówno geometria, jak i skład molekularny tych miejsc pomagają ustalać, jak mocno komórka ciągnie.
Złożona relacja między siłami lokalnymi a molekularnymi
Bardziej wnikliwa obserwacja pojedynczych ognisk ujawniła, że związek między lokalną trakcją a napięciem winculiny nie jest jednorodny. W niektórych komórkach ogniska generujące wyższe trakcji wykazywały również wyższe napięcie winculiny, co sugeruje, że zaangażowane, obciążone połączenia dzielą siłę bardziej bezpośrednio przez swoje ogniwa molekularne. W innych komórkach pojawiał się przeciwny wzorzec: obszary silnej trakcji wiązały się z niższym napięciem winculiny, podczas gdy inne ogniska dźwigały większe obciążenia molekularne bez generowania dużych Sił zewnętrznych. Wiele komórek nie wykazywało w ogóle wyraźnego wzorca. Te odmienne zachowania prawdopodobnie odzwierciedlają różne stany komórki—takie jak aktywne rozprzestrzenianie się, stabilna adhezja czy retrakcja—i sugerują, że komórki mogą redystrybuować siły w sieci adhezyjnej na różne sposoby.
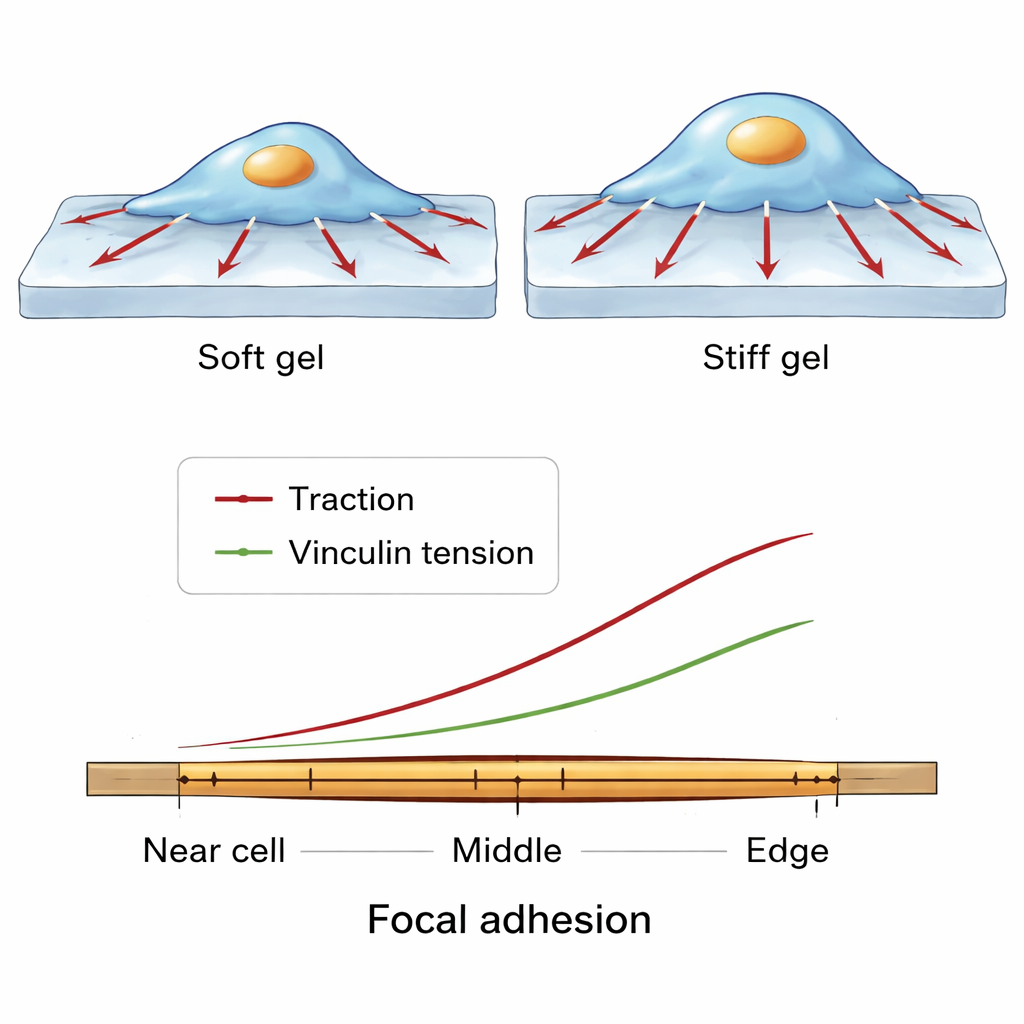
Wzorce sił na drobnej skali wzdłuż pojedynczego punktu uchwytu
Zespół przyjrzał się jeszcze dokładniej, badając, jak siły zmieniają się wzdłuż długości pojedynczego ogniska adhezyjnego, od strony bliższej środka komórki do krawędzi przy obwodzie komórki. Wśród wielu komórek i warunków ujawnił się spójny wzorzec. Molekuły winculiny były najgęściej upakowane w kierunku środka ogniska. Jednak zarówno trakcja wywierana na podłoże, jak i napięcie molekularne winculiny rosły w kierunku zewnętrznego, bardziej obwodowego końca. Sugeruje to swoisty balans: w centralnych rejonach wiele cząsteczek winculiny może rozdzielać obciążenie, więc każda z nich odczuwa mniejsze napięcie, podczas gdy na zewnętrznej krawędzi mniej cząsteczek dźwiga stosunkowo większą siłę, wspierając mocne lokalne pociąganie przy zachowaniu integralności ogniska.
Co to oznacza dla zdrowia i choroby
Łącząc mapy trakcji obejmujące całą komórkę z pomiarami napięcia na poziomie białka, to badanie oferuje wieloskalowy obraz tego, jak komórki zarządzają swoim mechanicznym chwytaniem. Praca pokazuje, że w miarę jak środowisko staje się bardziej sztywne, komórki zarówno silniej ciągną, jak i bardziej obciążają swoje ogniwa winculiny, ale szczegółowy związek między siłami zewnętrznymi a napięciem molekularnym różni się między ogniskami i między komórkami. Jednocześnie zachowany wydaje się być wyraźny przestrzenny wzorzec rozkładu sił wewnątrz pojedynczych ognisk. Dla czytelnika niezaznajomionego ze specjalistyką kluczowe przesłanie jest takie, że komórki precyzyjnie regulują zarówno miejsce, jak i sposób pociągania, redystrybuując siłę między wieloma małymi „sprężynami” molekularnymi, aby dostosować się do różnych środowisk mechanicznych—zasada, która może leżeć u podstaw procesów tak różnych, jak rozwój tkanek, włóknienie czy inwazja nowotworowa.
Cytowanie: Aytekin, S., Kimps, L., Coucke, Q. et al. Linking molecular tension and cellular tractions: a multiscale approach to focal adhesion mechanics. Commun Biol 9, 236 (2026). https://doi.org/10.1038/s42003-026-09514-0
Słowa kluczowe: mechanika komórek, ogniska adhezyjne, winculina, mikroskopia sił trakcyjnych, mechanotransdukcja