Clear Sky Science · pl
Dynamiczne skutki wtórnego cięcia RNA przez LbuCas13a w komórkach ludzkich
Przekształcenie bakteryjnej obrony w precyzyjny mechanizm samobójczy komórek
Naukowcy odkryli sposób na przekształcenie bakteryjnego białka odpornościowego w wysoce selektywny „wyłącznik samodestrukcji” dla komórek ludzkich. Wykorzystując enzym CRISPR o nazwie LbuCas13a, potrafią rozpoznać wybrany komunikat RNA w komórce, a następnie rozdrabniać niemal wszystkie pozostałe RNA tej komórki. Dla czytelników niezaawansowanych naukowo jest to intrygujące, ponieważ komunikaty RNA kontrolują, jakie białka komórka wytwarza; umiejętność ich kasowania na żądanie otwiera drzwi do nowych terapii przeciwnowotworowych, strategii przeciwwirusowych i potężnych narzędzi badawczych.
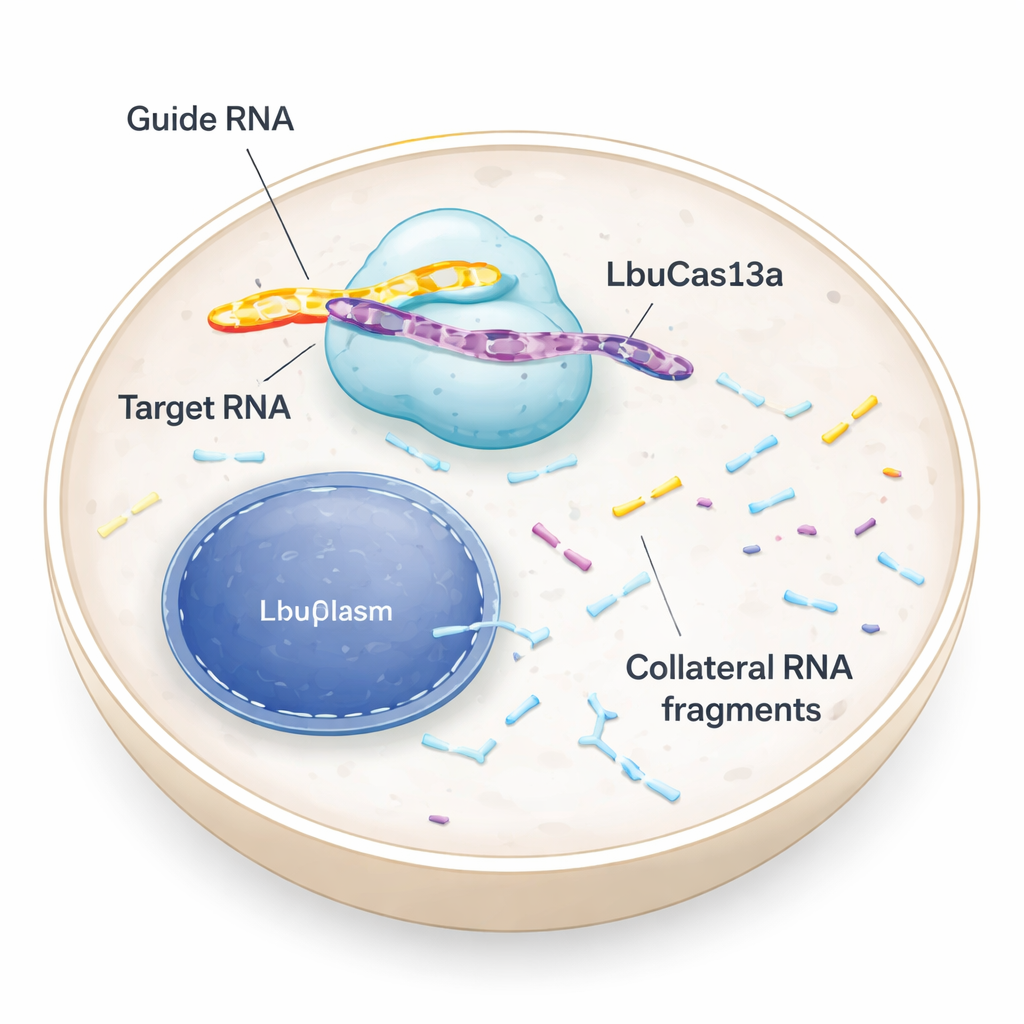
Cząsteczki nożyczek, które celują w RNA, a nie w DNA
Większość osób słyszała o narzędziach CRISPR, które tną DNA i przepisywują kod genetyczny. LbuCas13a jest inny: rozpoznaje i tnie RNA, tymczasowe komunikaty przenoszące instrukcje z DNA do „fabryk” białek w komórce. U bakterii enzymy Cas13 są częścią obrony przeciwwirusowej. Gdy wykryją wirusowe RNA, nie tylko tną tego intruza, lecz także zaczynają przecinać wiele innych RNA w pobliżu. Ta tak zwana aktywność „wtórna” może wprowadzić zainfekowane komórki w stan uśpienia lub śmierć, co pomaga chronić społeczność bakteryjną. Wczesne testy w komórkach zwierzęcych i ludzkich sugerowały, że wtórne cięcie przez Cas13 jest słabe lub nieobecne, więc enzym był głównie używany jako precyzyjny „wyłącznik” RNA. Nowe badanie poddaje to założenie rewizji i pokazuje, że przy właściwych warunkach aktywność wtórna w komórkach ludzkich może być silna i użyteczna.
Uwolnienie wtórnego cięcia w komórkach ludzkich
Zespół porównał kilka wariantów Cas13 i stwierdził, że LbuCas13a jest szczególnie potężny. Dostarczyli oczyszczone białko LbuCas13a, wstępnie załadowane krótkim RNA przewodnikiem, bezpośrednio do komórek ludzkich — forma molekularnej „iniekcji białka” zwana dostawą rybonukleoproteinową (RNP). Gdy przewodnik pasował do docelowego RNA — na przykład genu znacznika fluorescencyjnego lub obfitych naturalnych komunikatów jak GAPDH i 18S rRNA — enzym najpierw przecinał ten cel, a potem zaczął rozkładać wiele innych RNA. W ciągu około 50 minut ogólny profil RNA komórki zmieniał się dramatycznie, pojawiały się charakterystyczne fragmenty cięcia. Efekt wtórny obserwowano przy różnych metodach dostarczania i w szeregu typów komórek, co pokazuje, że nie był to efekt jednej linii komórkowej ani jednego sztucznego celu.
Z rozdrabniania RNA do śmierci komórki i selekcji
Co dzieje się z komórką, której komunikaty RNA nagle znikają? Korzystając z obrazowania komórek żywych, badacze zaobserwowali, że komórki ekspresjonujące docelowe RNA stopniowo wchodziły w apoptozę, uprządkowaną formę zaprogramowanej śmierci komórki oznaczaną charakterystycznymi „wczesnymi sygnałami ostrzegawczymi” przed rozpadem komórki. Co ważne, sąsiednie komórki, które nie ekspresjonowały docelowego RNA, pozostały w dużej mierze nienaruszone, demonstrując, że samodestrukcja jest specyficzna. Grupa następnie wykorzystała tę cechę jako narzędzie selekcyjne. Gdy zmieszali komórki niosące cel z komórkami normalnymi i aktywowali LbuCas13a, komórki z celem były selektywnie eliminowane przez kilka dni. Powtarzanie zabiegu wielokrotnie obniżało ich odsetek jeszcze bardziej. Pokazali, że można to wykorzystać do wzbogacania komórek poprawnie poddanych edycji genów, a także można było dostroić system do atakowania komórek nowotworowych nadprodukujących onkogen, tutaj CDK4, przy oszczędzaniu pokrewnych komórek wytwarzających znacznie mniej tego RNA.
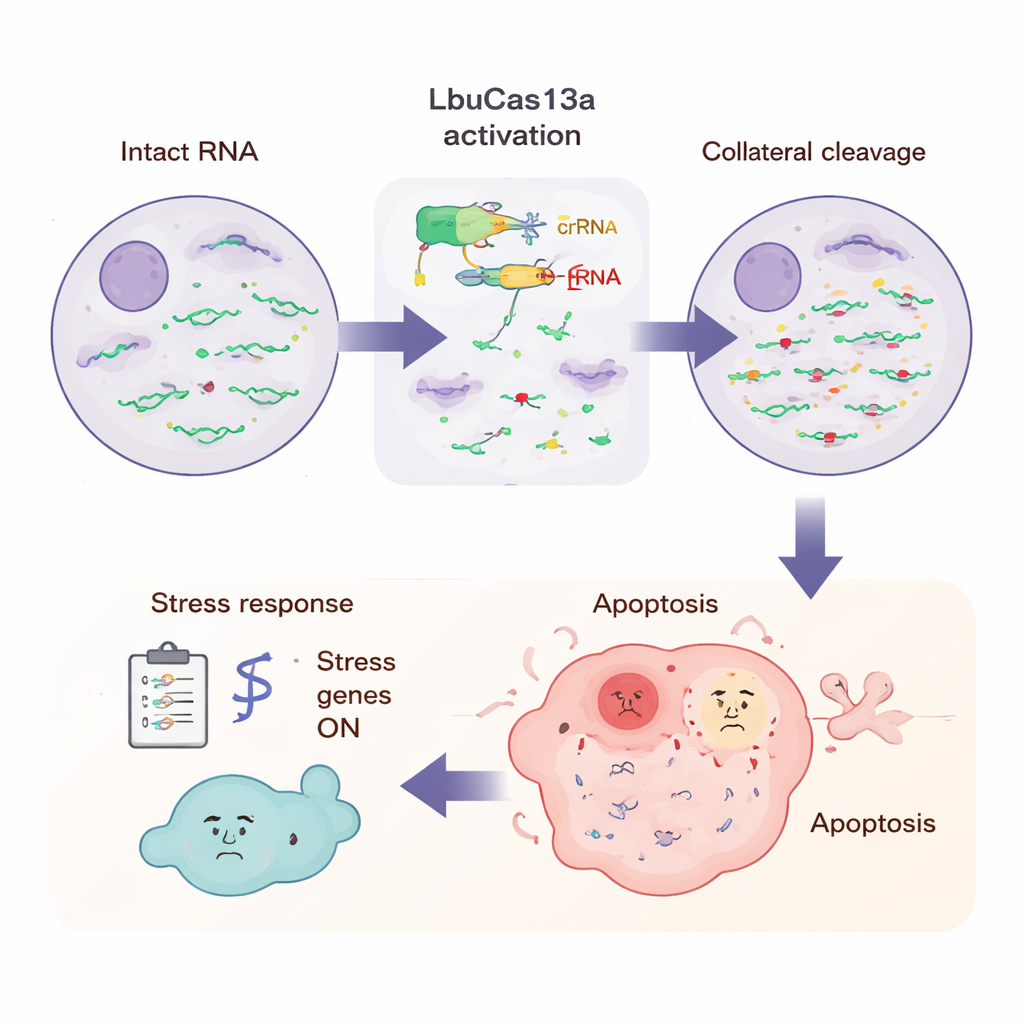
Czego doświadcza komórka podczas ataku
Aby zobaczyć szerszy obraz, naukowcy zmierzyli wszystkie RNA w komórce w kilku punktach czasowych po aktywacji LbuCas13a. Dzięki dodaniu znanych standardów RNA mogli wykazać, że większość kodujących białka RNA w cytoplazmie spadła o ponad połowę w ciągu kilku godzin, podczas gdy pewne RNA — na przykład komunikaty mitochondrialne i niektóre jądrowe RNA niekodujące — zostały w dużej mierze oszczędzone. Sekwencjonowanie długich odczytów ujawniło, że cięcie zachodziło w powtarzalnych, specyficznych pozycjach nukleotydowych, często w elastycznych regionach pętlowych RNA bogatych w uracyl, co odpowiada wzorcom zaobserwowanym w eksperymentach in vitro. W późniejszych punktach czasowych włączonych zostało wiele genów stresu i wrodzonej odporności, w tym powiązanych z sygnałami zapalnymi i obroną przeciwwirusową. Ten wzorzec sugeruje, że komórka wyczuwa nagły napływ połamanych końców RNA podobnie jak wykrywa infekcję wirusową, uruchamiając program alarmowy kończący się apoptozą.
Dlaczego to ma znaczenie i dokąd to prowadzi
W prostych słowach badanie pokazuje, że LbuCas13a można przekształcić w przewodnikowy „wyłącznik śmierci” komórek: jeśli komórka produkuje zbyt dużo określonego RNA, aktywacja LbuCas13a wobec tego RNA powoduje niemal całkowitą utratę RNA, reakcję typu immunologicznego, a następnie kontrolowaną śmierć komórki. Ponieważ proces w dużej mierze zależy od obfitości docelowego RNA, można go wykorzystać do eliminacji komórek nadekspresjonujących szkodliwe geny — na przykład pewnych komórek nowotworowych — albo do oczyszczania niepożądanych komórek w kulturach mieszanych podczas badań czy wytwarzania terapii komórkowych. Jednocześnie praca stanowi przestrogę: narzędzia CRISPR skierowane na RNA mogą mieć silne skutki uboczne, które trzeba starannie kontrolować. Zrozumienie, kiedy i jak zachodzi wtórne cięcie RNA, jest niezbędne dla bezpiecznego stosowania technologii Cas13 w medycynie i biotechnologii.
Cytowanie: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
Słowa kluczowe: CRISPR-Cas13, cięcie RNA, śmierć komórki, celowanie w nowotwory, narzędzia do edycji genów