Clear Sky Science · pl
Modulacja ludzkich receptorów klasy B1 GPCR przez lipidy błony plazmatycznej
Tłuszcze, które dopracowują odbiorniki wiadomości w naszych komórkach
Nasze komórki polegają na maleńkich antenach białkowych zwanych receptorami, które wyczuwają hormony i neuroprzekaźniki. Wiele najważniejszych leków działa poprzez oddziaływanie z tymi receptorami. Badanie to pokazuje, że powszechne tłuszcze w zewnętrznej warstwie komórek robią znacznie więcej niż tworzą bierne tło: bezpośrednio chwytają i kształtują całą rodzinę kluczowych receptorów, subtelnie sterując tym, jak sygnały są włączane lub wyłączane. Zrozumienie tej ukrytej warstwy kontroli może pomóc w projektowaniu mądrzejszych leków o mniejszych skutkach ubocznych.
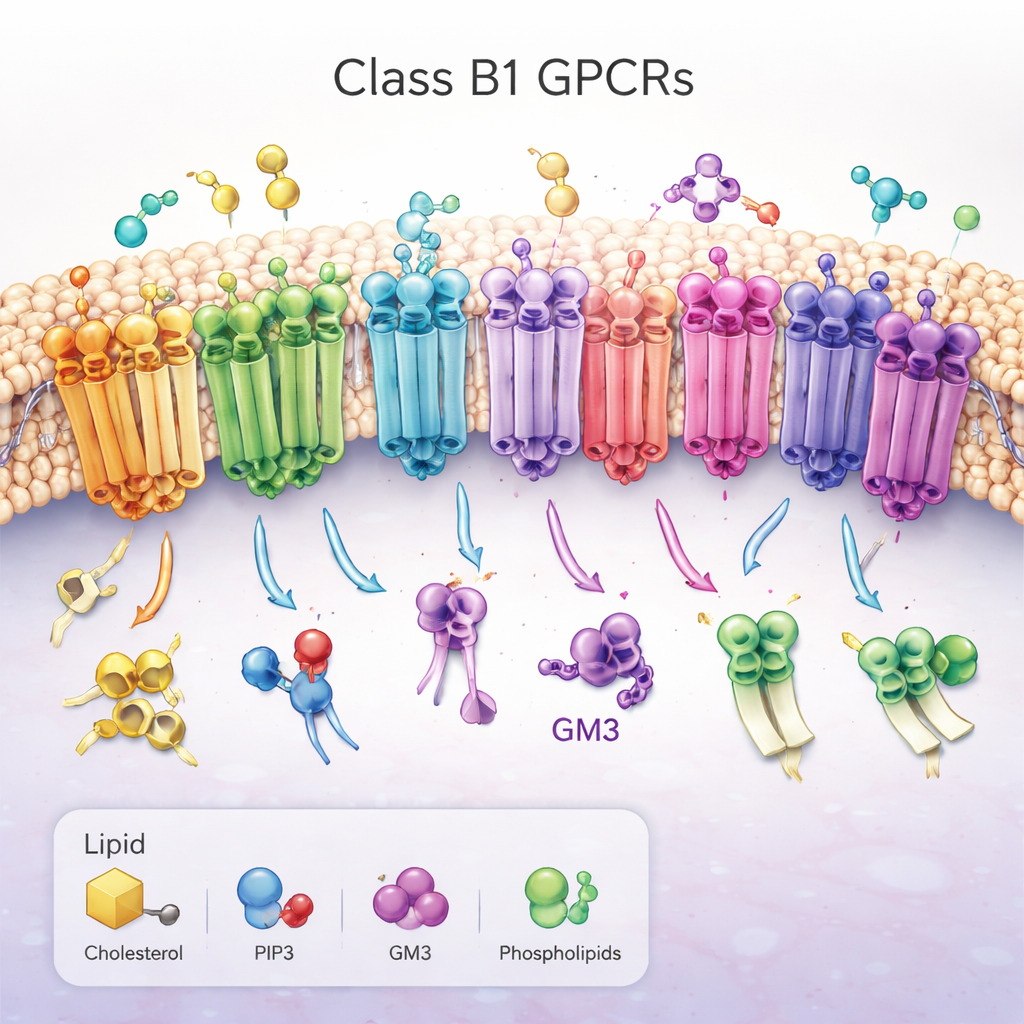
Rodzina istotnych molekularnych anten
Praca koncentruje się na receptorach klasy B1 sprzężonych z białkiem G (GPCR), zbiorze 15 blisko spokrewnionych receptorów, które pomagają kontrolować poziom cukru we krwi, metabolizm, wzrost i reakcje na stres. Przechodzą przez zewnętrzną błonę komórkową, z dużą "główką" na zewnątrz komórki, która chwyta cząsteczki podobne do hormonów, oraz wiązką siedmiu helis przebijających tłuszczową membranę. Po aktywacji receptory zmieniają kształt po wewnętrznej stronie komórki, odsłaniając rowek, który rekrutuje białkowych partnerów i uruchamia kaskady sygnalizacyjne. Ze względu na ich kluczową rolę w chorobach takich jak cukrzyca i otyłość, receptory klasy B1 są głównymi celami leków, jednak to, jak regulują je otaczające lipidy błonowe, pozostawało w dużej mierze tajemnicą.
Symulowanie receptorów w ich naturalnym sąsiedztwie
Zamiast badać receptory w sztucznych pęcherzykach z detergentem, badacze umieścili wszystkie 15 ludzkich receptorów klasy B1 GPCR w komputerowo zbudowanych błonach, które naśladują złożoną mieszankę tłuszczów w prawdziwych komórkach. Z użyciem techniki zwanej gruboziarnistą dynamiką molekularną przeprowadzili wiele długich symulacji każdego receptora w obu jego stanach — aktywnym i nieaktywnym — łącznie dając około milisekundy symulowanego czasu. Śledzili, jak trzy «regulacyjne» lipidy — cholesterol, lipid sygnałowy PIP2 oraz cukrowo udekorowany tłuszcz GM3 — zbliżają się, wiążą i odłączają od różnych regionów każdego receptora. Aby inni mogli odtworzyć i rozbudować ten ogromny zbiór danych, uchwycili każdy krok przygotowania i analizy za pomocą otwartego narzędzia workflow o nazwie aiida-gromacs, a swoje wyniki oparte na fizyce porównali z przewidywaniami nowego modelu AI (Chai‑1), który zgaduje, jak białka wiążą małe cząsteczki.
Ukryte kieszenie i zachowany chwyt lipidowy
Symulacje odkryły powtarzające się wzorce wiązania w całej rodzinie receptorów. Cholesterol, najbardziej znany z dyskusji dietetycznych, był widoczny nie tylko osadzający się w wcześniej poznanym miejscu na jednej z helis, lecz także w «głębokich błonowych» kieszeniach między helisami, z jego polarową główką zakopaną nietypowo głęboko w membranie. Jeden receptor, receptor sekretynowy, wykazał szczególnie długotrwałe wiązanie cholesterolu w odrębnych kieszeniach w formach aktywnej i nieaktywnej, co sugeruje, że cholesterol może silnie faworyzować określony sposób sygnalizacji. PIP2 wykazywał uderzająco zachowane zachowanie: grupował się wokół wewnętrznej powierzchni receptorów przy styku dwóch helis i krótkiego odcinka ogonka (TM6, TM7 i H8), szczególnie gdy receptory były w stanie aktywnym. W tym miejscu sieci dodatnio naładowanych aminokwasów chwytały ujemnie naładowaną grupę główkową PIP2, sugerując mechanizm, dzięki któremu ten lipid mógł stabilizować aktywny kształt lub pomagać rekrutować partnerów sygnalizacyjnych od strony wewnętrznej komórki.
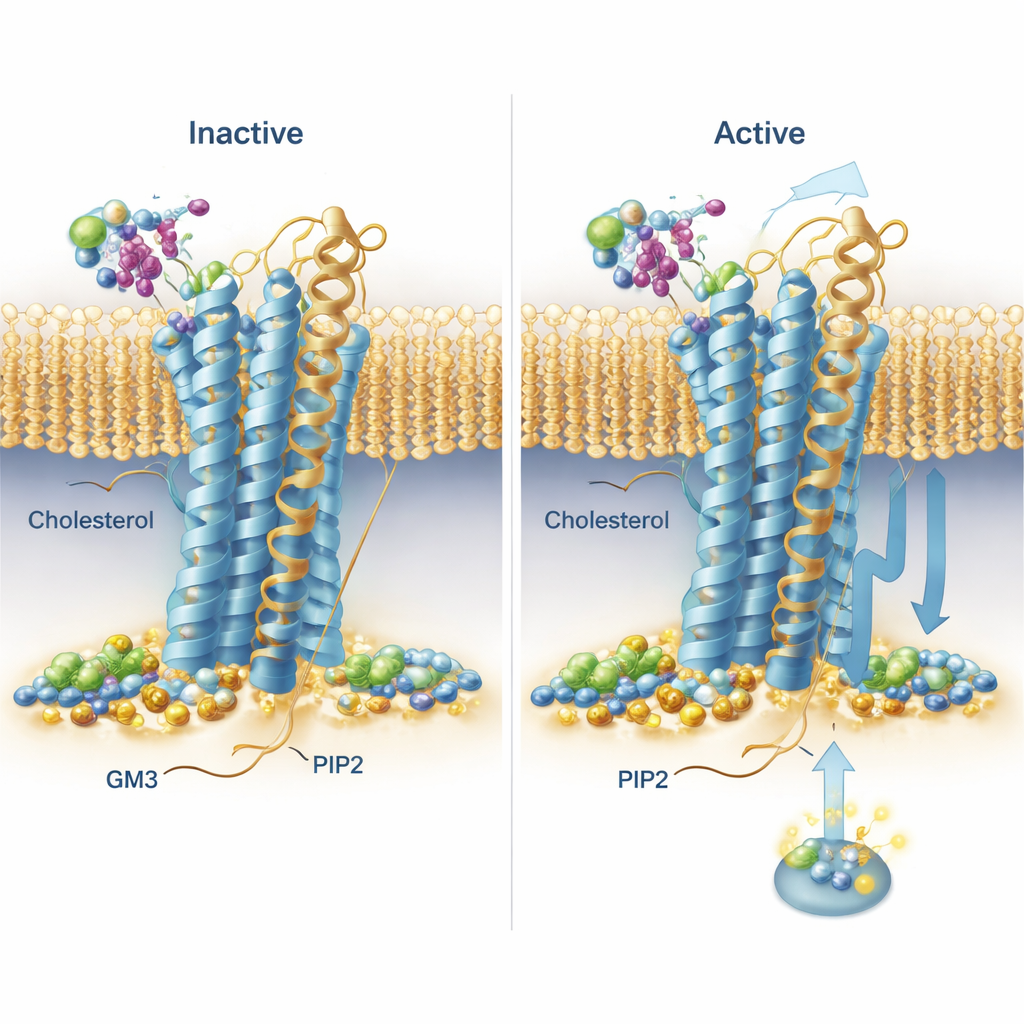
Cukrowo powleczony lipid, który popycha ruch receptora
GM3, złożony lipid z cukrową główką, głównie wchodził w interakcje z dużymi zewnętrznymi „główkami” receptorów. Zespół zauważył, że zewnętrzne domeny niektórych receptorów mocno się kołysały i wyginały względem błony, podczas gdy inne były bardziej ograniczone. Dla dwóch receptorów istotnych w kontekście leków — GLP‑1R i GIPR — przebadali rolę GM3 szczegółowo. W symulacjach z obecnym GM3 lipid albo wtulał się przy podstawie zewnętrznej domeny i kieszeni wiążącej ligand (GLP‑1R), albo przylgnął do najbardziej wysuniętego końca zewnętrznej domeny (GIPR), w obu przypadkach wpływając na swobodę ruchu tych domen. Aby przetestować te przewidywania w żywych komórkach, badacze użyli techniki opartej na świetle (TR‑FRET), która informuje, jak blisko jest oznakowana „główka” receptora względem błony. Kiedy obniżyli poziomy GM3 przy użyciu małocząsteczkowego inhibitora, zaobserwowali mierzalne zmiany w przesunięciach główek receptorów po stymulacji, co ogólnie zgadza się z ideą, że GM3 dostraja elastyczność receptorów w sposób zależny od typu receptora i jego stanu.
Dlaczego te partnerstwa lipid–receptor mają znaczenie
Razem badanie maluje obraz receptorów klasy B1 nie tylko jako przełączników hormonów, lecz jako elementów ściśle zaaranżowanego tańca z otaczającymi lipidami. Cholesterol może zajmować ukryte kieszenie i subtelnie faworyzować określone rezultaty sygnalizacyjne, PIP2 tworzy zachowany wewnętrzny „uchwyt”, który może zablokować receptory w formach aktywnych i kierować białkami-partnerami, a GM3 modyfikuje sposób, w jaki zewnętrzne regiony receptorów poruszają się i spotykają swoje ligandy. Dla laików kluczowe przesłanie jest takie, że błona jest aktywną warstwą regulacyjną: drobne różnice w składzie lipidowym mogą zmieniać zachowanie tego samego receptora w różnych tkankach lub stanach chorobowych. Mapując te interakcje szczegółowo i udostępniając podstawowe dane symulacyjne, praca ta tworzy podstawy do projektowania przyszłych leków, które będą wykorzystywać lub unikać specyficznych kontaktów z lipidami, co potencjalnie uczyni terapie bardziej selektywnymi i skutecznymi.
Cytowanie: Chao, K.W., Wong, L., Oqua, A.I. et al. Human class B1 GPCR modulation by plasma membrane lipids. Commun Biol 9, 317 (2026). https://doi.org/10.1038/s42003-025-09445-2
Słowa kluczowe: receptory sprzężone z białkiem G, lipidy błonowe, cholesterol, PIP2, GM3