Clear Sky Science · pl
Strukturalne spojrzenie na transport metaloklasterów w rusztowaniu montażowym nitrogenazy NifEN
Jak natura buduje potężne narzędzie chemiczne
Azot jest wokół nas w powietrzu, ale większość organizmów nie potrafi go wykorzystać w tej postaci. Specjalny enzym zwany nitrogenazą rozwiązuje ten problem, przekształcając azot atmosferyczny w amoniak — kluczowy składnik życia i nawozów. W centrum nitrogenazy znajduje się gęsty metalowy „klaster”, który przeprowadza wymagające reakcje chemiczne, lecz mechanizm składania tej złożonej struktury pozostawał niejasny. W artykule przygląda się temu procesowi, ujawniając, jak białkowe rusztowanie NifEN działa jak elastyczny terminal załadunkowy i system przenośników dla metalowego ładunku klastra.
Molekularna fabryka stojąca za nawozami i paliwami
Nitrogenaza jest naturalnym odpowiednikiem przemysłowych procesów wytwarzania amoniaku i paliw ciekłych. Zamiast wielkich reaktorów mikroby używają zwartej, białkowej maszyny napędzanej energią komórkową. Jej wydajność zależy od wyjątkowo złożonego centrum metalowego, zbudowanego z żelaza, siarki, molibdenu, węgla i grupy organicznej. Montaż tego rdzenia jest zbyt delikatny, by polegać na przypadku, dlatego komórki angażują zespół pomocniczych białek. Jednym z najważniejszych jest NifEN, które odbiera niemal gotowy, całkowicie żelazny prekursor (zwany L‑klastrem), pomaga przekształcić go w dojrzałą formę (M‑klaster), a następnie przekazuje do pracującej nitrogenazy. Zrozumienie, jak NifEN zarządza tym ruchem, może pomóc w projektowaniu mikroorganizmów do czystszej produkcji nawozów lub nowych paliw węglowych.
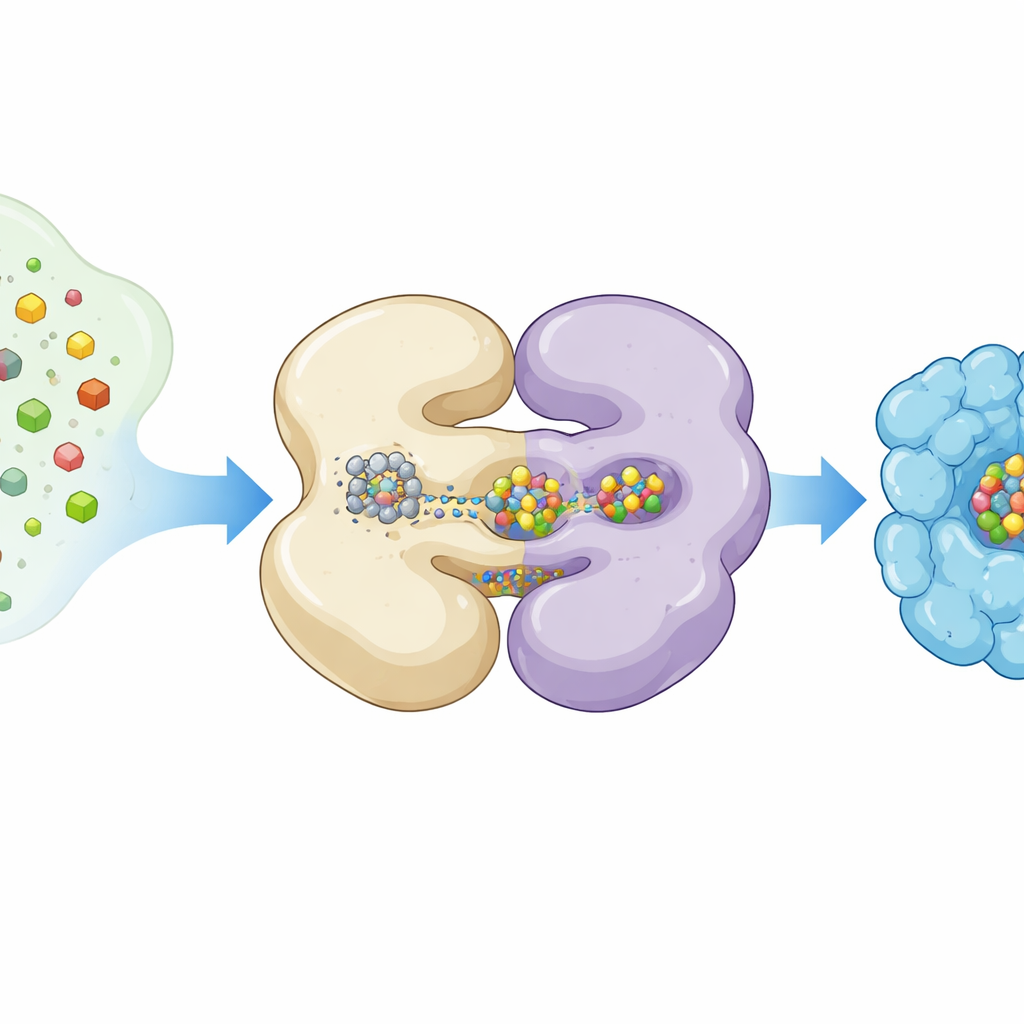
Widzieć poruszającą się maszynę dzięki zamrożonym migawkom
Autorzy wykorzystali kriogeniczną mikroskopię elektronową, technikę obrazowania białek w bardzo niskich temperaturach, aby uchwycić NifEN w różnych pozycjach pracy. Wyrazili NifEN w bakteriach laboratoryjnych w sposób, który pozostawił część kopii białka z L‑klastrem, a inne puste. Sortując miliony pojedynczych obrazów, odtworzyli dwie główne konformacje: formę „apo” pozbawioną ruchomego klastra oraz formę „holo” z klasrem związanym w wewnętrznym miejscu. Obie formy mają wspólne jądro złożone z czterech podjednostek ułożonych w dwie pary, lecz w obecności L‑klastra jedna połowa NifEN staje się znacząco bardziej uporządkowana, a kilka helis kołysze się do wewnątrz, zaciskając się wokół metalowego ładunku.
Ukryty tunel dla metalowego ładunku
Porównanie struktur pustej i załadowanej ujawniło uderzającą cechę: długi tunel przebiegający przez dimer NifEN. W stanie pustym przejście jest szerokie i otwarte; po związaniu klastra zwęża się, gdy białko zaciska pasażera. Wcześniejsze struktury krystaliczne pokazywały alternatywną „zewnętrzną” pozycję L‑klastra blisko powierzchni białka. Scalając wszystkie obserwacje, badacze wnioskowali, że klaster może zajmować co najmniej dwa stanowiska na NifEN — jedno ukryte wewnętrznie i jedno odsłonięte — i poruszać się między nimi wzdłuż zakrzywionej ścieżki sterowanej przesunięciami elastycznej domeny. Ruch ten wydaje się być bardziej swobodny niż w docelowej nitrogenazie, której aktywny klaster jest trzymany sztywno, co sugeruje, że NifEN jest zaprojektowane do przekazywania, a nie do długotrwałej katalizy.
Partnerzy dokujący i ciągła trasa
Aby zrozumieć, jak NifEN łączy się ze swoimi partnerami z góry i z dołu łańcucha, zespół połączył swoje eksperymentalne struktury z modelami obliczeniowymi AlphaFold 3 oraz niższą rozdzielczością mikroskopii elektronowej kompleksów białkowych. Modele sugerują, że enzym NifB, który tworzy L‑klaster z mniejszych fragmentów żelazowo‑siarkowych, dokuje w dolinie na jednej powierzchni NifEN. Stamtąd można prześledzić ciągły tunel od metalowych centrów NifB bezpośrednio do tunelu NifEN i dalej do wewnętrznego stanowiska L‑klastra. Na przeciwległej powierzchni NifEN inne miejsce dokowania mieści NifH, białko wprowadzające molibden i grupę organiczną, by dopełnić kofaktor. W tej konfiguracji L‑klaster znajduje się przy powierzchni, idealnie ustawiony do modyfikacji. Mutacje kluczowych aminokwasów wyściełających proponowaną trasę zaburzają załadunek, przemieszczanie lub dojrzewanie klastra, co dostarcza dowodów eksperymentalnych na model taśmy konwekcyjnej.
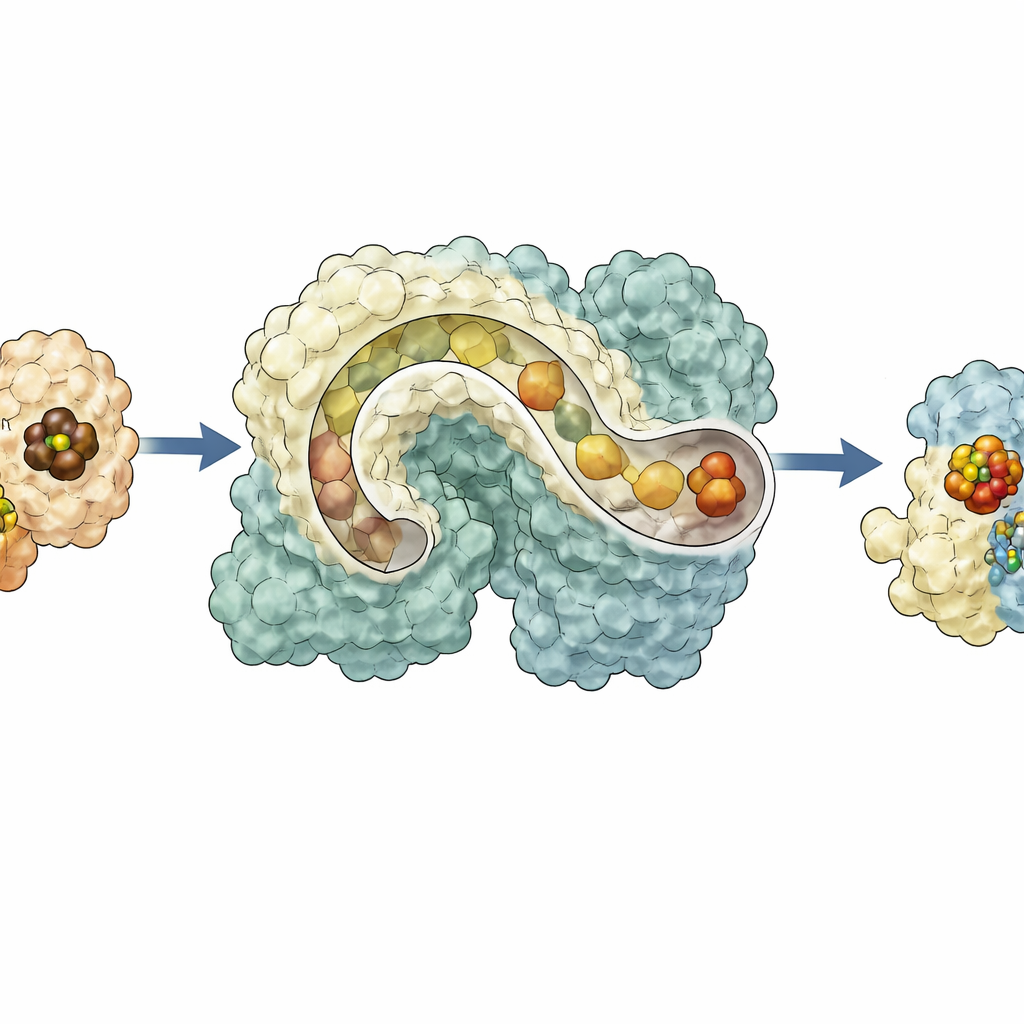
Dlaczego elastyczne rusztowanie ma znaczenie
W całości wyniki przedstawiają NifEN jako dynamiczne centrum, które odbiera metalowe jądro od NifB z jednej strony, przemieszcza je do wewnętrznej komory, a następnie prezentuje na przeciwnej powierzchni do wykończenia przez NifH, zanim skieruje dojrzały klaster z powrotem do środka w celu dostarczenia do nitrogenazy. Schemat transportu sterowanego konformacją wyjaśnia, jak wiele delikatnych kroków może być skoordynowanych w ramach jednej białkowej struktury i sugeruje, jak pradawne enzymy mogły ewoluować z bardziej elastycznych rusztowań do dzisiejszych wysoko wyspecjalizowanych katalizatorów. Dla osób niebędących specjalistami praca pokazuje, że nawet na poziomie nanoskopowym natura polega na liniach montażowych, tunelach i ruchomych częściach, by budować molekularne narzędzia leżące u podstaw globalnych cykli azotu, produkcji żywności i potencjalnie przyszłych zielonych technologii.
Cytowanie: Neumann, B., Brandon, K.A., Quechol, R. et al. Structural insights into metallocluster trafficking in the nitrogenase assembly scaffold NifEN. Nat Catal 9, 281–294 (2026). https://doi.org/10.1038/s41929-026-01489-9
Słowa kluczowe: nitrogenaza, montaż metaloklasterów, rusztowanie NifEN, kriogeniczna mikroskopia elektronowa, biologiczne wiązanie azotu