Clear Sky Science · pl
Szybkie przewidywanie aktywacji elektrycznej w lewej komorze za pomocą geometrycznego uczenia głębokiego: krok w stronę planowania terapii resynchronizacji serca
Dlaczego synchronizacja ma znaczenie dla słabego serca
Dla wielu osób z ciężką niewydolnością serca drobne impulsy elektryczne z wszczepionego urządzenia mogą pomóc komorom serca kurczyć się bardziej synchronicznie. Leczenie to, zwane terapią resynchronizacji serca, może łagodzić objawy i przedłużać życie. Jednak u około jednej trzeciej pacjentów korzyści są niewielkie, często dlatego że elektroda stymulacyjna po lewej stronie serca nie może zostać umieszczona w optymalnym miejscu. W badaniu sprawdzono, czy modele komputerowe napędzane współczesną sztuczną inteligencją mogą szybko przewidywać, jak prąd elektryczny rozchodzi się po lewej stronie serca, i pomóc lekarzom wybrać lokalizacje stymulacji dopasowane do konkretnego pacjenta.
Od powolnych symulacji do natychmiastowych przewidywań
Najdokładniejsze dzisiejsze modele komputerowe serca opierają się na złożonych równaniach odwzorowujących, jak sygnały elektryczne przemieszczają się w tkance mięśnia sercowego. Choć szczegółowe, symulacje te mogą trwać minuty na potężnych komputerach — zdecydowanie za długo, by stosować je rutynowo w trakcie procedury medycznej. Autorzy postawili sobie za cel stworzenie szybkich modeli „zastępczych”, które potrafiłyby nauczyć się na podstawie tych ciężkich symulacji, a następnie odtwarzać ich wyniki niemal natychmiast. Skoncentrowali się na lewej komorze, głównej komorze pompującej serca, oraz na przewidywaniu „map czasów aktywacji”, które pokazują, jak szybko różne obszary tej komory są elektrycznie uruchamiane podczas uderzenia serca.
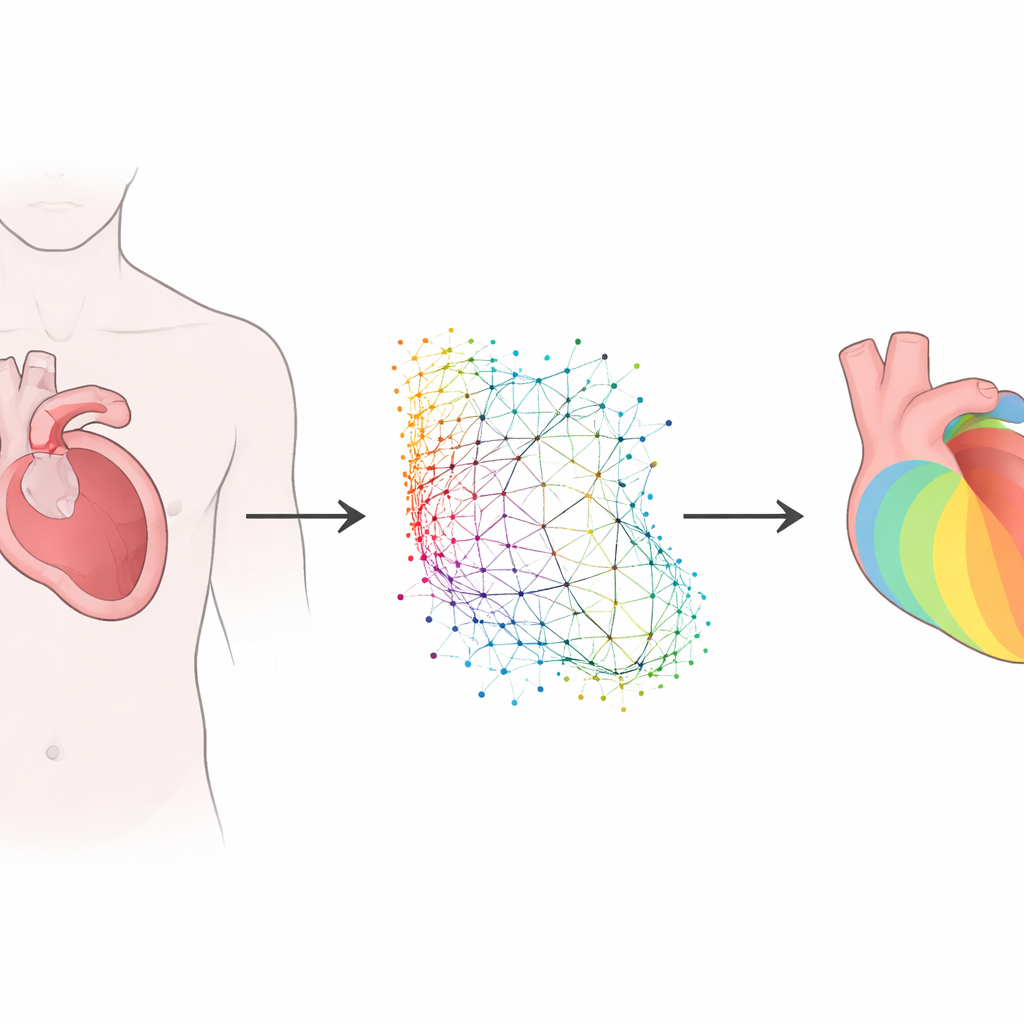
Nauczanie SI języka kształtów serca
Serce każdej osoby ma nieco inny kształt, a te różnice wpływają na sposób rozchodzenia się fal elektrycznych. Zamiast wymuszać dopasowanie wszystkich serc do sztywnej siatki, badacze zastosowali rodzinę metod zwanych geometrycznym uczeniem głębokim, które potrafią pracować bezpośrednio z nieregularnymi kształtami. Opracowali i porównali dwa powiązane podejścia. Pierwsze, oparte na grafowej sieci neuronowej, traktuje lewą komorę jako zbiór punktów połączonych jak siatka. Drugie, nazwane geometrycznie informowanym operatorem neuronowym, najpierw koduje tę nieregularną geometrię na regularnej wewnętrznej siatce, przetwarza ją, a następnie mapuje wynik z powrotem na pierwotną anatomię. Oba modele przyjmują trójwymiarowy kształt serca, lokalizacje miejsc stymulacji oraz przewodnictwo tkanki i przewidują, jak aktywacja rozprzestrzenia się przez ścianę mięśnia.
Budowanie wirtualnej populacji serc
Ponieważ duże zbiory rzeczywistych danych pacjentów z pełnymi trójwymiarowymi mapami aktywacji są rzadkie, zespół wygenerował własny zestaw danych syntetycznych. Wykorzystali 75 rzeczywistych kształtów lewej komory obejmujących serca zdrowe i chore i użyli statystycznego modelu kształtu, aby stworzyć 35 000 syntetycznych wariantów. Dla każdego przypisano realistyczne kierunki włókien mięśniowych, wybrano jedno lub dwa miejsca stymulacji i zmieniano przewodnictwo tkanki w szerokim zakresie. Szczegółowe symulacje oparte na fizyce wygenerowały mapy czasów aktywacji dla wszystkich tych wirtualnych serc, które następnie posłużyły do uczenia i testowania modeli głębokiego uczenia. Modele sprawdzono również z siatkami o wyższej rozdzielczości oraz na geometrach lewej komory pochodzących z dwóch niezależnych kohort klinicznych, aby ocenić, jak dobrze uogólniają się poza syntetyczny zestaw treningowy.
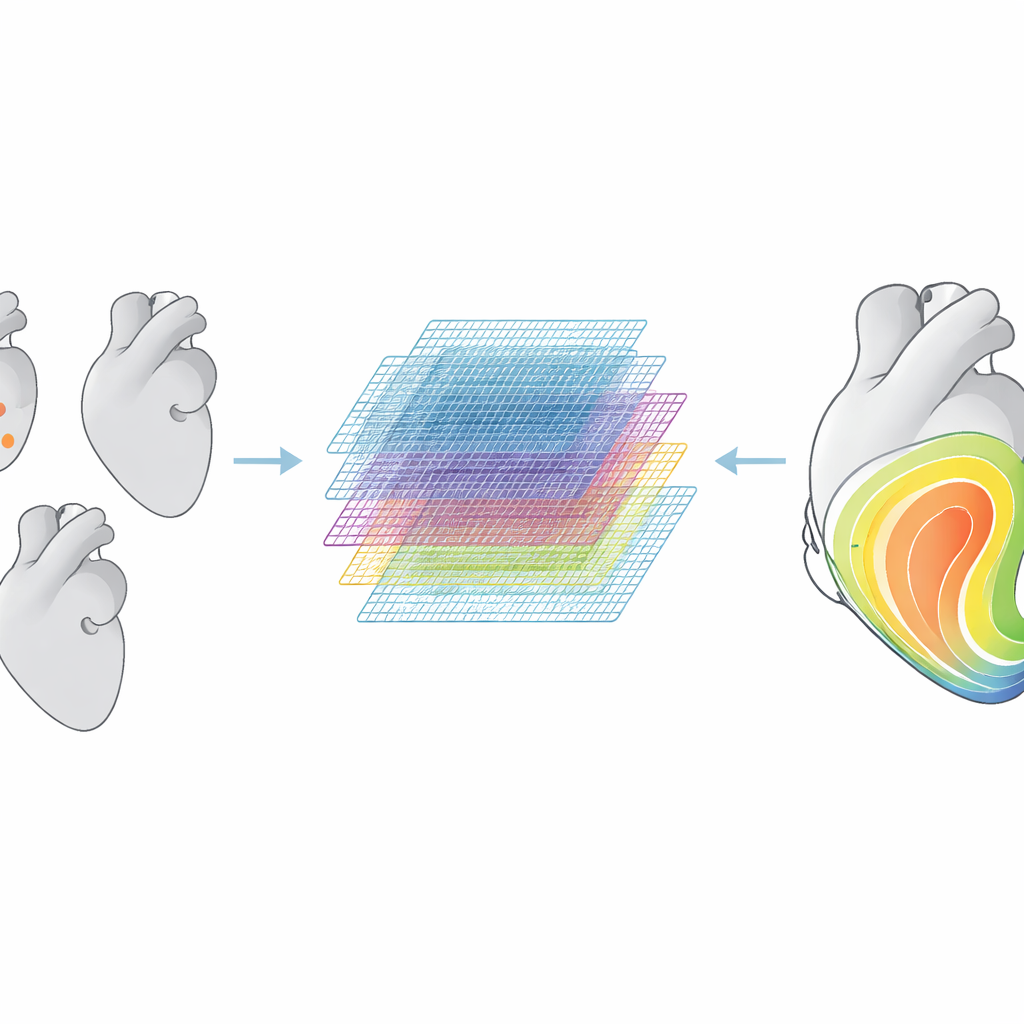
Jak dobrze działały modele?
Na sercach syntetycznych podobnych do tych, na których były trenowane, oba modele przewidywały mapy aktywacji z niewielkimi błędami, ale geometrycznie informowany operator neuronowy był mniej więcej dwukrotnie dokładniejszy niż grafowa sieć neuronowa. Po przejściu do rzeczywistych kształtów serca błąd wzrósł dla obu modeli i ich wydajność stała się porównywalna. To wskazuje, że głównym ograniczeniem nie jest moc algorytmów, lecz luka między uproszczonymi kształtami treningowymi a pełną złożonością anatomii pacjentów. Mimo to modele potrafiły dokonywać przewidywań w milisekundach — znacznie szybciej niż tradycyjna symulacja zajmująca około dziesięciu minut — co czyni je atrakcyjnymi do zadań wymagających tysięcy powtórzeń, takich jak przeszukiwanie wielu możliwych miejsc stymulacji.
Testowanie wirtualnego narzędzia planowania
Zespół następnie osadził wytrenowane modele w koncepcyjnym przepływie pracy planowania terapii resynchronizacji. Wychodząc od kształtu lewej komory i zaszumionej mapy aktywacji mającej naśladować pomiary kliniczne, przepływ pracy najpierw działał odwrotnie, aby oszacować naturalne miejsce stymulacji pacjenta i przewodnictwo tkanki. Następnie przeszukiwał powierzchnię komory w poszukiwaniu drugiego miejsca stymulacji, które minimalizowałoby całkowity czas aktywacji — wielkość powiązaną w poprzednich badaniach z lepszą odpowiedzią na terapię. Oba modele głębokiego uczenia potrafiły odzyskać kluczowe parametry specyficzne dla pacjenta z zaszumionych danych i zaproponować miejsca stymulacji, które znacząco skracały czas aktywacji, wszystko to w ciągu kilkudziesięciu sekund na pojedynczym procesorze graficznym. Autorzy przygotowali także interfejs webowy, w którym użytkownicy mogą przesyłać geometrie, badać scenariusze stymulacji i interaktywnie uruchamiać optymalizację.
Co to oznacza dla pacjentów
Praca ta pokazuje, że starannie wytrenowane modele głębokiego uczenia mogą naśladować szczegółowe symulacje elektryczne lewej komory dla wielu kształtów i konfiguracji stymulacji oraz robić to wystarczająco szybko, by wykorzystać je w narzędziach planowania. Choć obecne modele opierają się na danych treningowych syntetycznych i uwzględniają jedynie zachowanie elektryczne lewej komory, tworzą podstawy dla bardziej kompleksowych cyfrowych bliźniaków obejmujących obie strony serca i jego mechaniczną czynność pompowania. Przy bogatszych danych rzeczywistych i dalszym doskonaleniu takie narzędzia mogłyby pewnego dnia pozwolić klinicystom przetestować wiele strategii stymulacji na komputerze przed procedurą, zwiększając szansę na to, że każdy pacjent otrzyma konfigurację urządzenia, która rzeczywiście przywróci synchronię serca.
Cytowanie: Naghavi, E., Wang, H., Ziaei-Rad, V. et al. Rapid prediction of cardiac activation in the left ventricle with geometric deep learning: a step towards cardiac resynchronization therapy planning. npj Digit. Med. 9, 225 (2026). https://doi.org/10.1038/s41746-026-02399-7
Słowa kluczowe: terapia resynchronizacji serca, geometryczne uczenie głębokie, elektrofizjologia serca, modelowanie indywidualne pacjenta, cyfrowy bliźniak