Clear Sky Science · pl
Odszyfrowanie osi immunoregulacyjnej ERS–CAF za pomocą multimodalnej sztucznej inteligencji oraz jej prognostyczna i terapeutyczna wartość pan‑nowotworowa
Zajrzeć do guza bez skalpela
Lekarze onkolodzy coraz częściej dostrzegają, że otoczenie guza może mieć znaczenie równie duże jak sam guz. Jednak wielokrotne pobieranie próbokształtów tego ukrytego sąsiedztwa za pomocą biopsji jest inwazyjne i często niepraktyczne. Badanie to pokazuje, jak sztuczna inteligencja (AI) może odczytywać rutynowe skany medyczne i obrazy mikroskopowe, aby wywnioskować trudne do zmierzenia procesy odpornościowe i bliznowate wewnątrz guzów, potencjalnie przekształcając codzienne obrazowanie w rodzaj „cyfrowej biopsji” działającej w różnych nowotworach.
Ukryte komórki wspierające, które kształtują raka
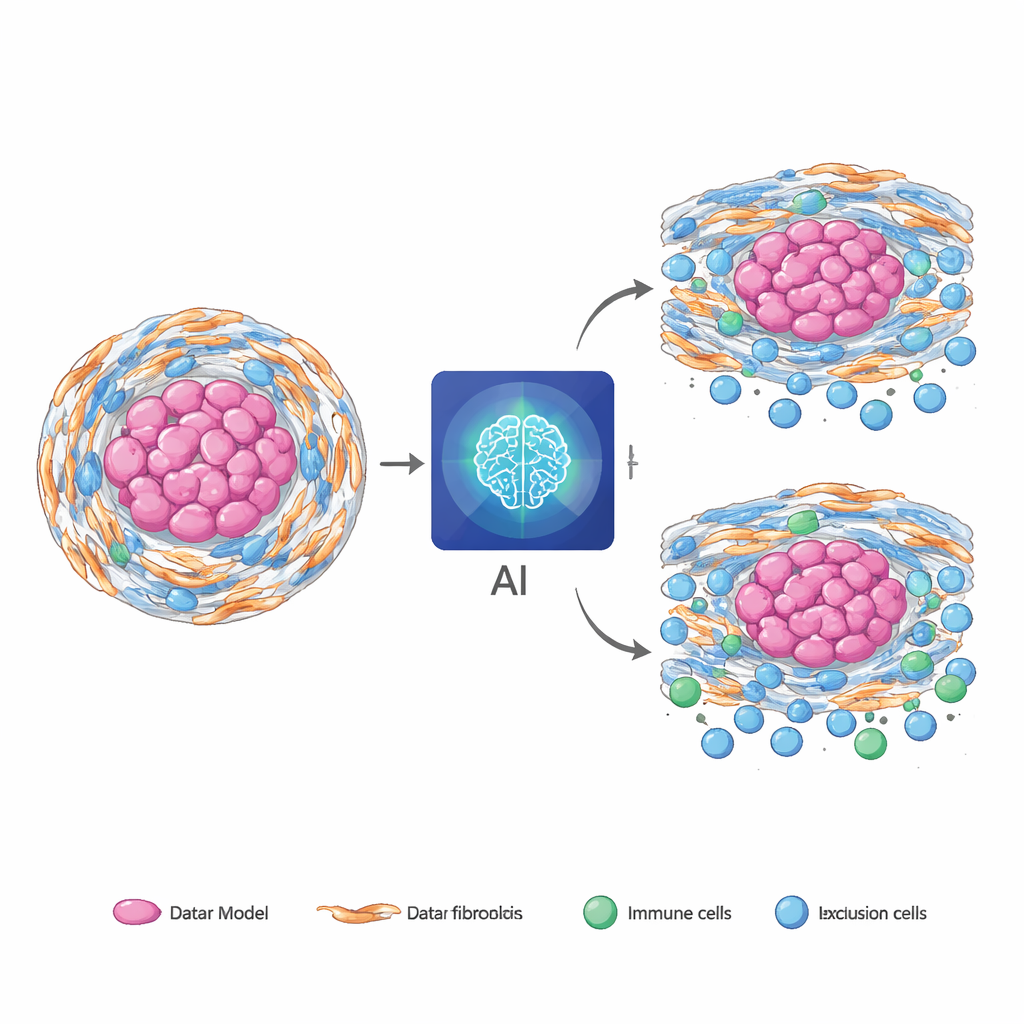
Wiele nowotworów litych jest otoczonych twardą, włóknistą otoczką tworzoną przez wyspecjalizowane komórki wspierające zwane fibroblastami. Gdy te komórki doświadczają stresu w fabryce białek komórki (siateczce śródplazmatycznej), przyjmują agresywny, sprzyjający rakowi stan. W chordomie, rzadkim nowotworze kości, te zestresowane fibroblasty tworzą gęstą matrycę i pomagają wykluczać komórki odpornościowe, osłabiając skuteczność terapii. Podobne włókniste, ubogie w komórki odpornościowe środowiska pojawiają się w innych nowotworach, takich jak trzustkowy i jelita grubego, co sugeruje, że ta biologia nie jest unikatowa dla jednej choroby. Problem polega na tym, że obecne metody mierzenia tych zestresowanych fibroblastów i ich immunoblockingowego zachowania opierają się na próbkach tkankowych i złożonych testach molekularnych, które trudno powtarzać i które mogą pominąć istotne obszary guza.
Nauczyć AI dostrzegać niewidoczną biologię
Naukowcy zastanawiali się, czy standardowe przedoperacyjne skany MRI i rutynowe preparaty H&E zawierają już wizualne wskazówki dotyczące bariery immunologicznej wywołanej zestresowanymi fibroblastami. Stworzyli trzy liczbowe „skale referencyjne” z sekwencjonowania RNA guza: jedną odzwierciedlającą aktywność programu stresowego we fibroblastach, drugą podsumowującą siłę sygnalizacji tych komórek wobec komórek odpornościowych, oraz trzecią opisującą różnorodność otaczających populacji komórek odpornościowych i wspierających. Zamiast przewidywać tysiące genów, ich AI została wytrenowana do przewidywania tylko tych trzech biologicznie istotnych wskaźników wyłącznie na podstawie obrazów. W tym celu zespół połączył dwie gałęzie: jedną analizującą teksturę i cechy kształtu w MRI, oraz drugą skanującą tysiące małych regionów w cyfrowym preparacie i wykorzystującą mechanizm uwagi kierowany językowo, by skupić się na obszarach odpowiadających eksperckim opisom tkanki włóknistej i ubogiej w odporność.
Łączenie skanów i preparatów dla silniejszych sygnałów
W 126 pacjentach z chordomą, u których dostępne były dopasowane MRI, preparaty patologiczne, dane RNA i obserwacja, zintegrowany model AI przewyższył modele używające wyłącznie MRI lub wyłącznie preparatów. Jego przewidywania trzech molekularnych wskaźników ściśle zgadzały się z pomiarami opartymi na RNA i pozostały dobrze skalibrowane między różnymi szpitalami i skanerami. Gdy patolodzy niezależnie zaznaczali obszary włókniste i z wykluczeniem immunologicznym, „gorące punkty” AI często pokrywały te same rejony, co sugeruje, że śledziła autentyczną biologię, a nie tylko wielkość guza. Model uchwycił także wartość prognostyczną: wyższe przewidywane wskaźniki stresu fibroblastów i sygnalizacji wiązały się z gorszym przeżyciem, podczas gdy większa przewidywana różnorodność mikrośrodowiska dawała częściową ochronę. Dodanie tych wskaźników pochodzących z AI do rutynowych czynników klinicznych poprawiło zdolność rozróżniania pacjentów o wysokim i niskim ryzyku w czasie.
Od rzadkich guzów do powszechnych nowotworów
Kluczowym testem było sprawdzenie, czy model wytrenowany w całości na chordomie da się wykorzystać „jak jest” w innych, częstszych nowotworach. Zastosowany bez ponownego uczenia do guzów trzustki, żołądka i jelita grubego z dużych publicznych zbiorów danych, wersja modelu oparta tylko na preparatach nadal wykazywała istotne dopasowanie między przewidywaniami na podstawie obrazów a świeżo obliczonymi wskaźnikami opartymi na RNA. W niektórych z tych nowotworów wyniki AI poprawiły prognozowanie przeżycia pacjentów ponad standardowe informacje kliniczne i pomogły wyróżnić pacjentów bardziej prawdopodobnych do korzyści z chemioterapii. Aby ułatwić wdrożenie podejścia tam, gdzie patologia cyfrowa jest ograniczona, zespół sprowadził pełen multimodalny model do wersji opartej tylko na MRI, która zachowała większość mocy predykcyjnej przy szybszym działaniu i mniejszym zapotrzebowaniu na moc obliczeniową.
Co to może oznaczać dla pacjentów
Podsumowując, wyniki wspierają ideę, że rutynowe obrazy medyczne cicho kodują informacje o zestresowanych komórkach wspierających, wykluczeniu immunologicznym i różnorodności mikrośrodowiska — cechach, które zwykle wymagają kosztownych testów molekularnych. Choć obecne badanie ma charakter retrospektywny i wymaga walidacji prospektywnej, wskazuje na przyszłość, w której standardowy skan i preparat mogą nieinwazyjnie zasygnalizować guzy z wrogą, włóknistą barierą immunologiczną, pokierować, którzy pacjenci mogą skorzystać z dodatkowych testów lub terapii dopasowanych do nich, i robić to w wielu typach nowotworów bez dodatkowego obciążenia dla pacjentów.
Cytowanie: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
Słowa kluczowe: mikrośrodowisko guza, obrazowanie nowotworów, sztuczna inteligencja, fibroblasty, immunoterapia