Clear Sky Science · pl
Algorytmiczne decyzje o antybiotykoterapii w zakażeniach dróg moczowych z wykorzystaniem prognozy użyteczności leczenia uwzględniającej preferencje przepisywaczy
Inteligentniejsze antybiotyki dla powszechnych infekcji
Zakażenia dróg moczowych (ZUM) należą do najczęstszych powodów przepisywania antybiotyków. Wybór właściwego leku to jednak balans: lekarze muszą wyleczyć infekcję, unikać poważnych działań niepożądanych i jednocześnie chronić społeczeństwo przed narastającą opornością. W tym badaniu przedstawiono nowy typ algorytmu podejmowania decyzji, który ma wspierać klinicystów, łącząc duże zbiory danych szpitalnych z realnymi priorytetami lekarzy, pomagając wybierać antybiotyki skuteczne dla pacjenta, a jednocześnie bezpieczniejsze z perspektywy populacji.
Problem z „mocnymi” lekami
Współczesna medycyna opiera się na antybiotykach, lecz nadużywanie szerokospektralnych, „mocnych” leków napędza globalny kryzys oporności. Organizacja Narodów Zjednoczonych wyznaczyła cel: do 2030 r. 70% stosowania antybiotyków na świecie powinno pochodzić z węższego, pierwszego rzędu arsenału, określanego przez WHO jako leki z kategorii „Access”. W praktyce wielu klinicystów skłania się ku szerszym środkom, oznaczonym „Watch” lub „Reserve”, obawiając się, że wąsko ukierunkowany lek zawiedzie wobec bakterii opornych, zwłaszcza u ciężko chorych pacjentów. W rezultacie często wymieniamy długoterminowe ryzyko narastającej oporności na krótkoterminowe poczucie bezpieczeństwa, bez jasnych narzędzi pomagających ocenić, kiedy bezpieczniejszy, węższy lek rzeczywiście zadziała równie dobrze.
Nauczanie algorytmu myślenia jak klinicysta
Naukowcy zbudowali algorytm podejmowania decyzji o antybiotykoterapii ukierunkowany na ZUM, wykorzystując szczegółowe elektroniczne dane medyczne od niemal 94 000 hospitalizowanych pacjentów z Bostonu. Najpierw wytrenowali modele predykcyjne, aby oszacować dla 13 różnych antybiotyków prawdopodobieństwo wrażliwości wywołujących zakażenie bakterii oraz prawdopodobieństwo wystąpienia komplikacji, takich jak zakażenie Clostridioides difficile czy poważna toksyczność leku. Następnie poprosili 49 brytyjskich klinicystów z różnych specjalności o wypełnienie internetowego ćwiczenia rankingowego, w którym wybierali między fikcyjnymi antybiotykami różniącymi się cechami takimi jak ryzyko działań niepożądanych, przydatność w ZUM, koszt, przynależność do kategorii Access lub Watch/Reserve oraz forma podania (doustna lub dożylna). Analizując te rankingi, zespół skwantyfikował, jak mocno lekarze cenią poszczególne cechy — na przykład jak bardzo wolą leki ukierunkowane na ZUM, o niskiej toksyczności i w formie doustnej, zamiast bardziej ryzykownych lub „mocniejszych” opcji.
Dodanie siatki bezpieczeństwa dla bardzo chorych pacjentów
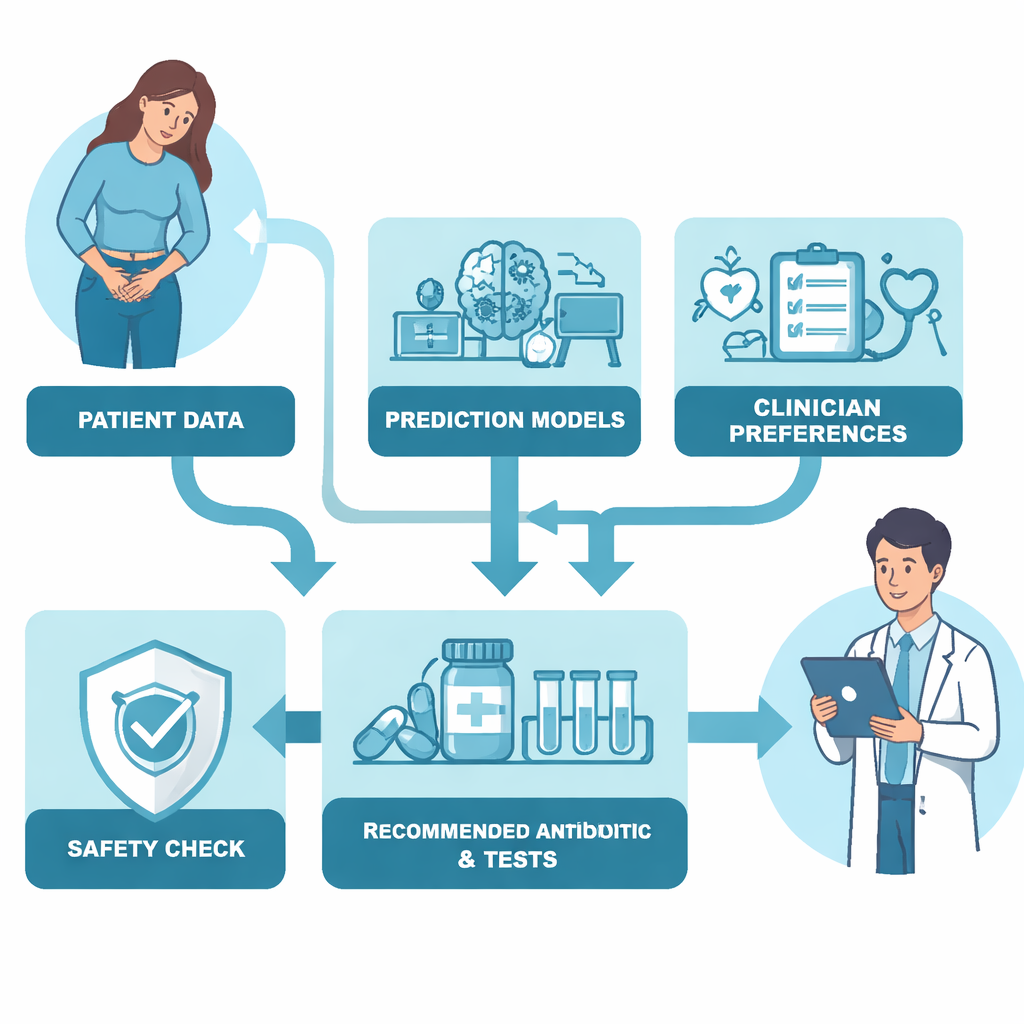
Końcowy algorytm połączył te dwa składniki: prognozy oparte na danych i wartości przypisywane przez klinicystów. Dla każdego pacjenta obliczał „wartość leczenia” dla każdego antybiotyku, uwzględniając przewidywane szanse na skuteczność leku, ryzyko poważnych działań niepożądanych, kategorię Access/Watch/Reserve oraz formę podania. Kluczowe było wbudowanie mechanizmu bezpieczeństwa, opartego na tym, jak ciężko chory pacjent wyglądał na oddziale ratunkowym. Wraz ze wzrostem ciężkości choroby algorytm automatycznie przywiązywał większą wagę do stosowania silnego uderzenia w zakażenie i dostępności opcji dożylnej. Innymi słowy, u pacjentów z łagodniejszym przebiegiem preferował leki wąskospektralne i doustne, ale wraz ze wzrostem ciężkości stanu coraz chętniej proponował silniejsze, dożylne antybiotyki, by zapobiegać nieskuteczności terapii.
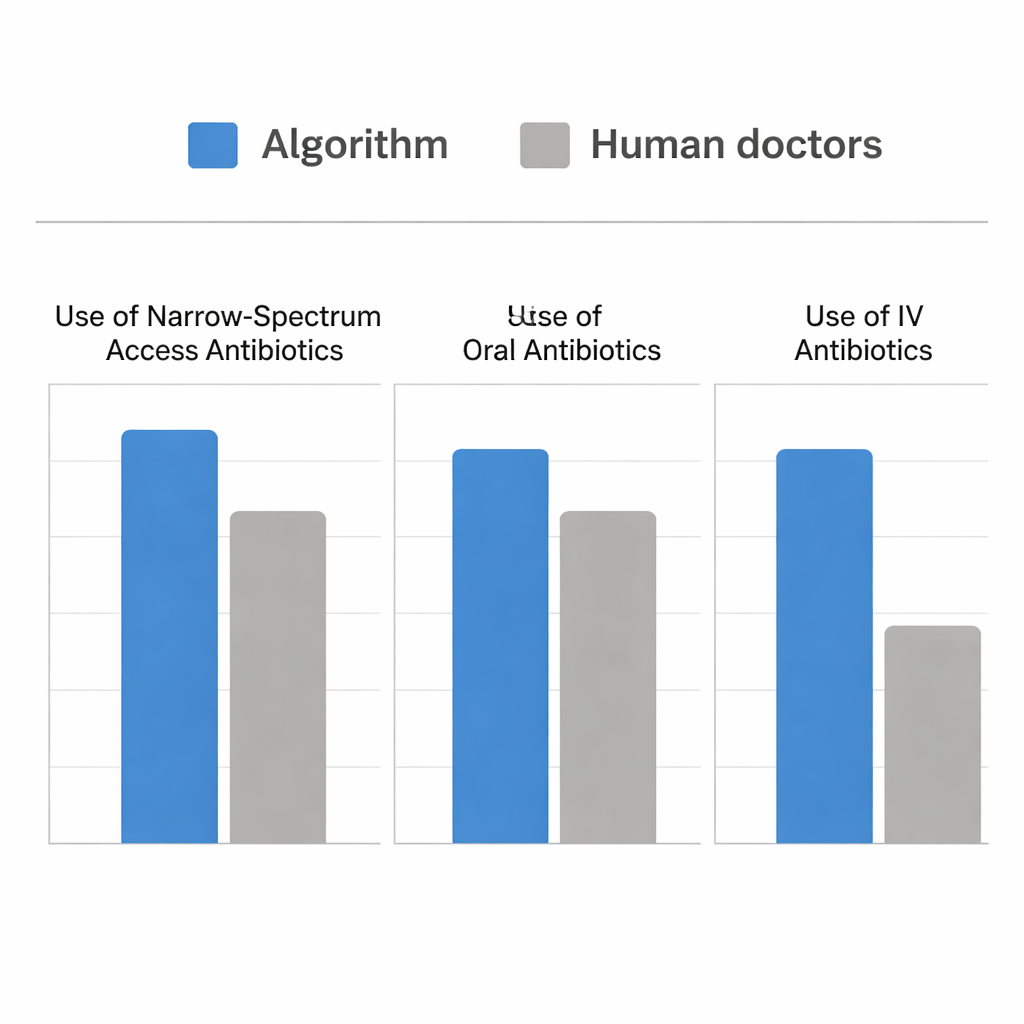
Jak algorytm wypadł w porównaniu z lekarzami
Zespół przeprowadził symulację na podstawie rzeczywistych przypadków z oddziału ratunkowego, w których pacjenci mieli ZUM i posiewy moczu. Porównano antybiotyki podane przez lekarzy z tymi, które algorytm wybrałby w momencie wysłania posiewu. Oba podejścia były podobnie skuteczne w wyborze leku pokrywającego bakterie pacjenta. Jednak algorytm dokonywał tego, wybierając znacznie więcej wąskospektralnych leków z kategorii Access i znacznie więcej terapii doustnych, przy mniejszym odsetku podań dożylnych. U cięższych pacjentów algorytm zachowywał się podobnie do ludzkich przepisywaczy, odpowiednio przesuwając wybór w kierunku leków dożylnych i silniejszych. Różnił się natomiast w rozpoznawaniu dodatkowych możliwości — zwłaszcza u pacjentów o umiarkowanym nasileniu choroby — bezpiecznego leczenia doustnymi lekami z kategorii Access, takimi jak nitrofurantoina czy ampicylina-sulbaktam, zamiast domyślnego sięgania po szersze opcje.
Co to znaczy dla codziennej opieki
Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że system nie zastępuje lekarzy; działa raczej jak kalkulator złożonych kompromisów ryzyka i korzyści, o które klinicyści już dbają, ale których nie są w stanie precyzyjnie obliczać w głowie. Łącząc priorytety samych lekarzy z dużą skalą dowodów o skuteczności antybiotyków, algorytm może sugerować terapie równie skuteczne dla poszczególnych pacjentów, lecz łagodniejsze dla organizmu i zdrowsze dla populacji — preferując tabletki zamiast kroplówek, gdy jest to bezpieczne, oraz węższe leki zamiast tych zarezerwowanych, gdy tylko możliwe. Jeśli narzędzie zostanie zwalidowane w innych warunkach, takie systemy mogą pomóc szpitalom i systemom opieki zdrowotnej zbliżyć się do globalnych celów odpowiedzialnego stosowania antybiotyków, bez poświęcania bezpieczeństwa osób przyjmowanych w stanie krytycznym z infekcją.
Cytowanie: Howard, A., Green, P.L., Zhong, Y. et al. Algorithmic antibiotic decision-making in urinary tract infection using prescriber-informed prediction of treatment utility. npj Digit. Med. 9, 136 (2026). https://doi.org/10.1038/s41746-026-02369-z
Słowa kluczowe: zakażenie dróg moczowych, stewardship antybiotykowy, wspomaganie decyzji klinicznych, oporność na środki przeciwdrobnoustrojowe, uczenie maszynowe w medycynie