Clear Sky Science · pl
DARE-FUSE: uczenie prowadzone przez dowody z wyrównaniem domenowym do jednoczesnej segmentacji i klasyfikacji guzów mózgu w MRI
Dlaczego ważne są inteligentniejsze badania mózgu
Guzy mózgu należą do jednych z najbardziej niepokojących diagnoz w medycynie, a rezonans magnetyczny (MRI) jest podstawowym narzędziem, którym lekarze określają, gdzie guz się zaczyna i kończy. Nawet doświadczeni radiolodzy mogą mieć trudności z precyzyjnym wyznaczeniem granic guza i oceną jego zmian w czasie, zwłaszcza gdy krawędzie zlewają się z obrzękniętą tkanką mózgową. W artykule wprowadzono DARE-FUSE — nowy system sztucznej inteligencji zaprojektowany do bardziej niezawodnego odczytu badań MRI mózgu, rysowania ostrzejszych granic guza i przedstawiania wyraźniejszych wyjaśnień swoich decyzji, aby wspierać chirurgów, onkologów i pacjentów.
Rozmyte krawędzie i przepełnione poradnie
W rzeczywistych szpitalach badania MRI mózgu bywają chaotyczne. Guzy często zlewają się z otaczającym je obrzękiem, implanty metalowe mogą zniekształcać obraz, a różne placówki stosują nieco odmienne ustawienia skanów. Radiolodzy muszą ręcznie przeglądać setki obrazów, zaznaczać guz warstwa po warstwie, a następnie ocenić, jak się zachowuje. Ta praca jest czasochłonna, męcząca i podatna na rozbieżności między ekspertami. Istniejące narzędzia AI potrafią pomagać w zaznaczaniu guzów lub oznaczaniu skanów jako „guz” lub „brak guza”, ale większość systemów wykonuje te zadania oddzielnie, a wiele z nich słabnie, gdy obrazy pochodzą z nowych ośrodków lub zawierają subtelne, nieregularne wzrosty na obrzeżach.
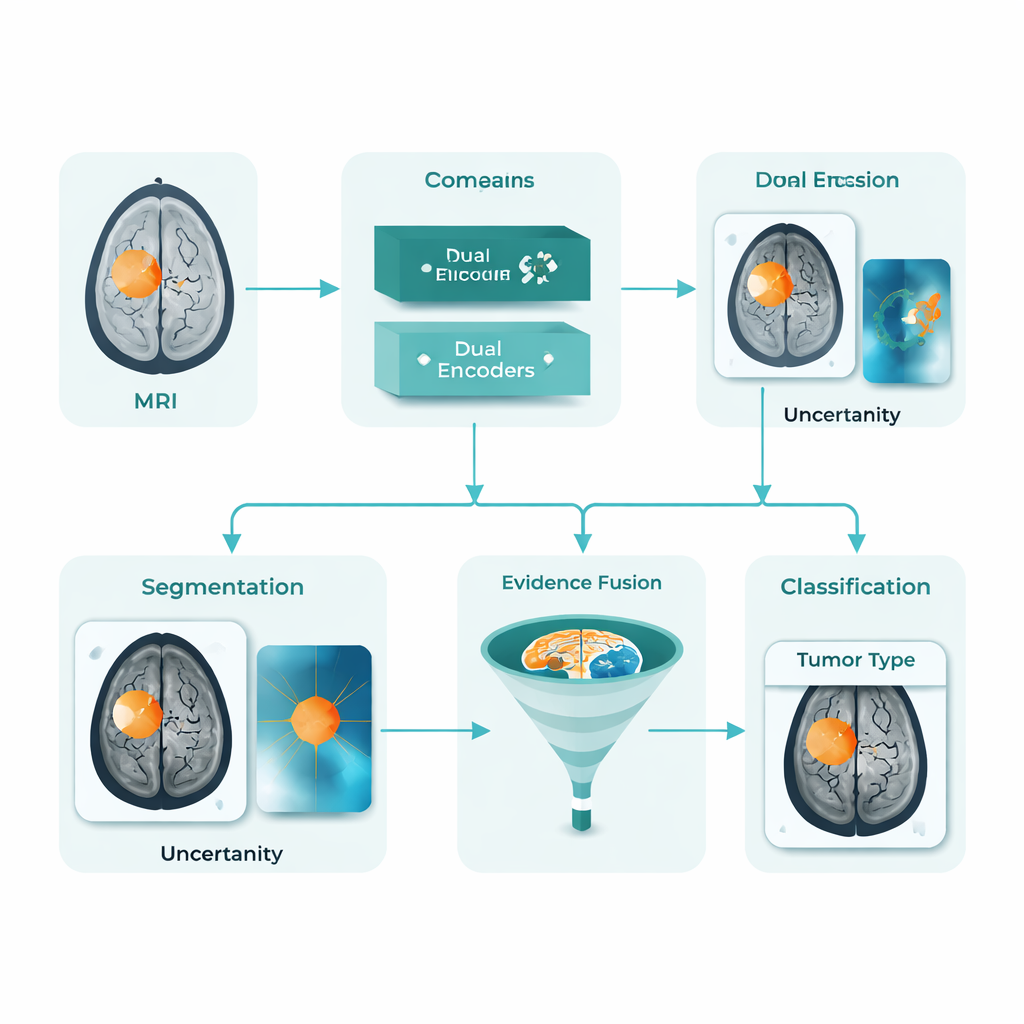
Zunifikowany asystent AI do map guza i etykiet
DARE-FUSE rozwiązuje kilka z tych problemów jednocześnie. Zbudowano go jako pojedynczy proces, który jednocześnie wyznacza guz na każdej warstwie MRI (segmentacja) i klasyfikuje całe obrazy do grup diagnostycznych (klasyfikacja). W jego rdzeniu działają dwa współpracujące „względy”: jedna sieć nastawiona na szczegóły kształtów i krawędzi, a druga na globalne wzorce rozróżniające różne typy guzów. Specjalny moduł wyrównania utrzymuje zgodność tych widoków między szpitalami i skanerami, tak aby cechy wyuczone na jednym zbiorze nie pogarszały wydajności na innym. System także ocenia własną niepewność, sygnalizując obszary, gdzie mniej pewny jest co do dokładnego obrysu guza — co jest kluczowe dla bezpiecznego użycia klinicznego.
Wykorzystanie wskazówek z map cieplnych i rekonstrukcji „bez guza”
Zamiast polegać na pojedynczym sygnale, DARE-FUSE uczy się z wielu rodzajów dowodów. Jeden odgałęzienie generuje mapy cieplne, pokazujące, które części mózgu najbardziej wspierają decyzję klasyfikacyjną AI. Inne odgałęzienie używa modelu generatywnego, aby wyobrazić sobie, jak ten sam skan mógłby wyglądać, gdyby guz został usunięty, a następnie porównuje tę „wersję bez guza” z oryginałem. Różnice między nimi uwypuklają subtelne zmiany strukturalne i krawędzie, które mogą nie wyróżniać się wyraźnie na standardowej mapie cieplnej. Moduł fuzji łączy te wskazówki w ciągłą mapę „priorytetu guza”: regiony, gdzie kilka źródeł się zgadza, traktowane są jako rdzeń guza, podczas gdy mniej pewne obszary dodawane są ostrożniej i obniżane wagowo, gdy niepewność modelu jest wysoka. Taki połączony priorytet kieruje końcowym konturem, pomagając uniknąć zarówno pominiętych kieszonek guza, jak i fałszywych wysp w zdrowej tkance.
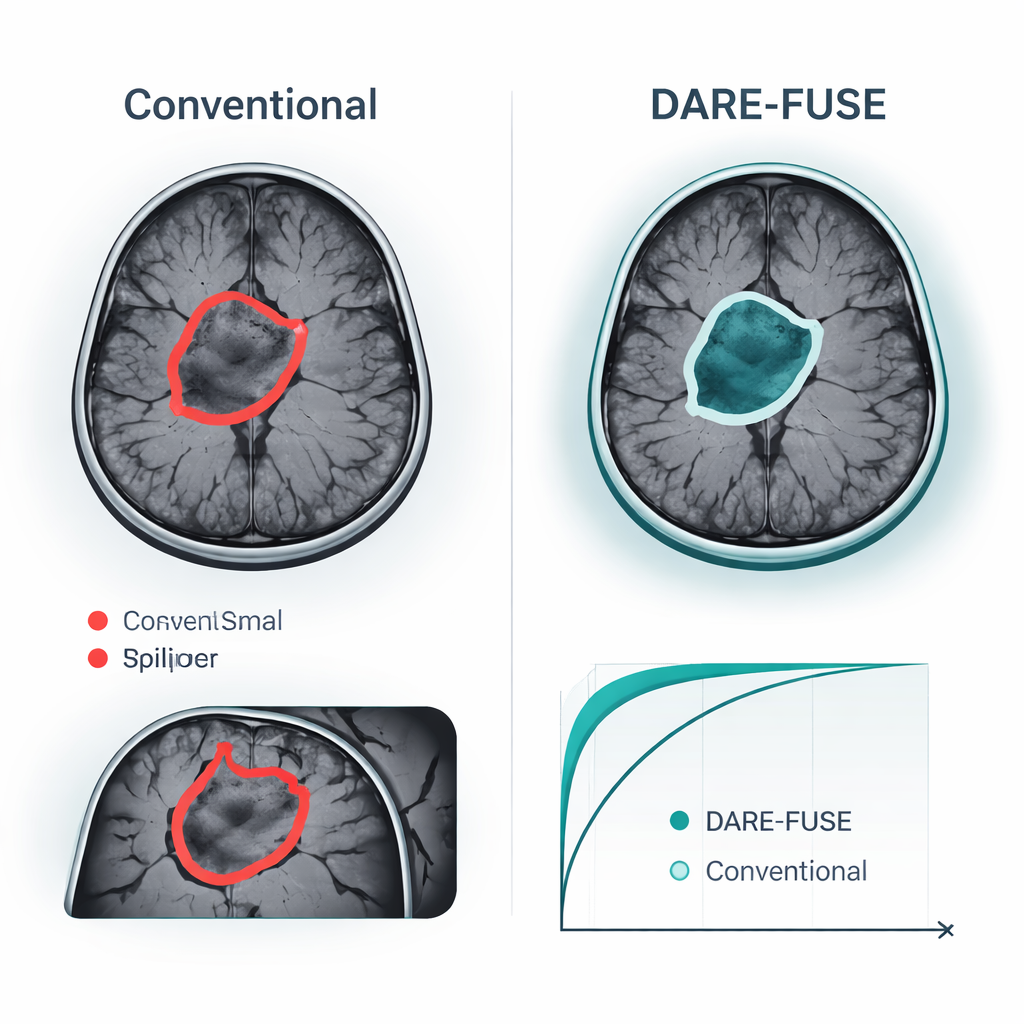
Udokumentowane korzyści na publicznych zbiorach danych o guzach mózgu
Autorzy przetestowali DARE-FUSE na sześciu dużych, wieloośrodkowych wyzwaniach dotyczących guzów mózgu (seria BraTS) oraz na czterech publicznych kolekcjach MRI używanych do klasyfikacji na poziomie obrazu. We wszystkich edycjach BraTS system dorównał lub przewyższył najlepsze ostatnie modele uczenia głębokiego, osiągając nieco większe pokrycie między przewidywanymi maskami guza a rysunkami ekspertów oraz konsekwentnie mniejsze błędy w mierzonej powierzchni guza. Zyski te były najbardziej widoczne w trudnych przypadkach: małych guzach, krawędziach o niskim kontraście i złożonych, nieregularnych kształtach. W zadaniach klasyfikacyjnych — decydowaniu, czy skan pokazuje np. glejaka, oponiaka, guz przysadki czy brak guza — DARE-FUSE także wyprzedzał silne podstawy transformatorowe i słabo nadzorowane pod względem dokładności oraz standardowej miary dyskryminacji (AUC). Co ważne, gdy badacze sztucznie zmniejszyli liczbę szczegółowych adnotacji, nowy system degradował się łagodnie i zachował przewagę nad pół-nadzorowanymi i słabo nadzorowanymi konkurentami.
Co to może znaczyć dla pacjentów
Dla pacjentów i klinicystów główną obietnicą DARE-FUSE nie jest widowiskowy nowy algorytm, lecz bardziej niezawodne, interpretowalne wsparcie obrazowe. W praktyce system mógłby proponować obrys guza, wyróżniać obszary, w których jest mniej pewny, oraz wyświetlać mapy cieplne wyjaśniające, które rejony obrazu wpływają na jego klasyfikację. Lekarze mogliby zaakceptować obszary o niskiej niepewności jako wyjściowy kontur, a następnie skupić uwagę na oznaczonych fragmentach zamiast odrysowywać wszystko od nowa. Dokładniejsze i bardziej spójne pomiary objętości i kształtu guza mogłyby poprawić planowanie leczenia, celowanie radioterapii i monitorowanie odpowiedzi w czasie. Autorzy podkreślają, że ich narzędzie jest asystentem — a nie zastępstwem — dla eksperckiego osądu, jednak wyniki wskazują na systemy AI, które potrafią zarówno widzieć guzy wyraźniej, jak i komunikować poziom swojej pewności w sposób, na którym klinicyści mogą działać.
Cytowanie: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
Słowa kluczowe: MRI guza mózgu, segmentacja obrazów medycznych, uczenie głębokie w radiologii, wspomaganie decyzji klinicznych, Sztuczna inteligencja uwzględniająca niepewność