Clear Sky Science · pl
HMC-transducer: hierarchiczny mamba‑CNN transducer dla niezawodnej segmentacji guzów wątroby
Dlaczego lepsze mapy guzów są ważne
W przypadku pacjentów z rakiem wątroby lub nerek lekarze polegają na tomografii komputerowej (TK), by zdecydować, czy możliwe są operacja, radioterapia lub inne terapie. Kluczowym etapem jest precyzyjne obrysowanie każdego guza w trzech wymiarach — zadanie wolne, pracochłonne i niejednolite, gdy wykonywane ręcznie. Ten artykuł przedstawia nowy rodzaj systemu sztucznej inteligencji, który może automatycznie wyznaczać te guzy dokładniej i spójniej niż wcześniejsze metody, co potencjalnie pomaga klinicystom szybciej i pewniej planować leczenie.
Widzieć pełny obraz w skanach 3D
Guzów wątroby trudno jest wyraźnie odrysować, ponieważ wykazują dużą zmienność rozmiarów i kształtów oraz często zlewają się z otaczającą tkanką. Tradycyjne narzędzia głębokiego uczenia zwane konwolucyjnymi sieciami neuronowymi (CNN) świetnie wychwytują drobne szczegóły na obrazach, ale mają problemy ze zrozumieniem relacji na dużą skalę — jak struktura w jednej części skanu odnosi się do innej, odległej części. Nowsze modele zwane Transformatorami potrafią uchwycić szeroki kontekst, lecz stają się niezwykle kosztowne przy przetwarzaniu dużych objętości 3D TK, co ogranicza ich praktyczność w rzeczywistych szpitalach. Autorzy argumentują, że aby osiągnąć sukces, system musi być jednocześnie ukierunkowany na szczegóły i świadomy całości, bez wymagań poziomu mocy superkomputera.
Nowy hybrydowy „mózg” dla obrazów medycznych
Aby sprostać tym wymaganiom, badacze zaprojektowali HMC‑Transducer — architekturę hybrydową łączącą CNN z nowszą rodziną modeli zwanych modelami stanu (state space models), w szczególności jednym z nich o nazwie Mamba. Części oparte na CNN koncentrują się na ostrej lokalnej informacji, takiej jak wyraźne krawędzie guzów. Elementy Mamba śledzą przepływ informacji w całym skanie 3D przy koszcie obliczeniowym liniowym, unikając gwałtownego wzrostu zasobów typowego dla Transformerów. Specjalnie zaprojektowany blok „kierunkowo-świadoma 3D Mamba” przetwarza skan wzdłuż trzech osi — głowa‑stopa, lewo‑prawo i przód‑tył — tak aby model respektował rzeczywistą strukturę anatomiczną, zamiast spłaszczać objętość do jednowymiarowego ciągu liczb.
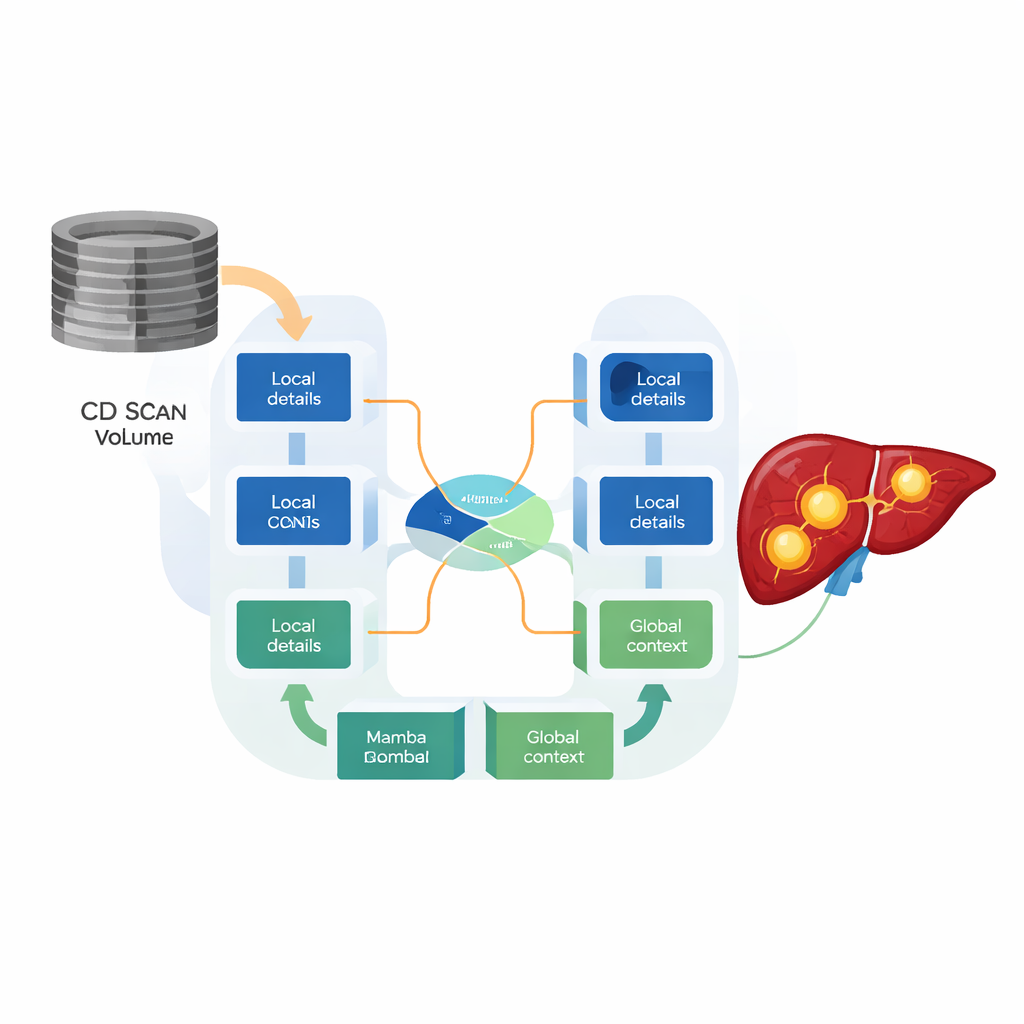
Pozwolić modelowi zdecydować, co gdzie się liczy
Istotną innowacją jest sposób łączenia tych dwóch typów cech. Zamiast po prostu dodawać lub nakładać wyniki CNN i Mamba, HMC‑Transducer wykorzystuje mechanizm bramkowanej fuzji, który uczy się dla każdego małego regionu skanu, ile zaufać lokalnym detalom, a ile globalnemu kontekstowi. W obszarach o wyraźnych, ostrych granicach bramka może opierać się na cechach CNN; tam, gdzie guzy są rozmyte, naciekające albo leżą blisko dużych naczyń krwionośnych, może przyznać większą wagę szerszemu spojrzeniu dostarczanemu przez Mambę. Eksperymenty pokazują, że takie adaptacyjne łączenie daje bardziej precyzyjne i stabilne segmentacje niż same CNN czy modele oparte na Mambie, a także wyraźne ulepszenia w porównaniu z wcześniejszymi hybrydowymi projektami, które fuzję cech wykonywały w sposób stały, nieadaptacyjny.
Testowane w różnych narządach, na różnych skanerach i w różnych szpitalach
Zespół ocenił podejście na trzech głównych publicznych zestawach danych: LiTS17 i MSD‑Liver dla guzów wątroby oraz KiTS21 dla guzów nerek. W tych benchmarkach HMC‑Transducer konsekwentnie osiągał większe pokrycie z mapami guzów narysowanymi przez ekspertów niż silne metody bazowe, w tym powszechnie używany nnU‑Net oraz czołowe modele Transformer i Mamba. Model także lepiej uogólniał, gdy trenowano go na jednym zbiorze wątroby, a testowano na innym zebranym w różnych szpitalach — scenariusz odzwierciedlający rzeczywiste wdrożenie z różnymi skanerami i protokołami obrazowania. W testach bezpośrednich duże „modele bazowe” takie jak SAM i jego medyczne warianty, używane bez specjalistycznego dopasowania, były znacznie gorsze, co podkreśla, że do decyzji na poziomie pikseli w medycynie wciąż potrzebne są zadaniowo‑specyficzne, starannie dopracowane systemy.
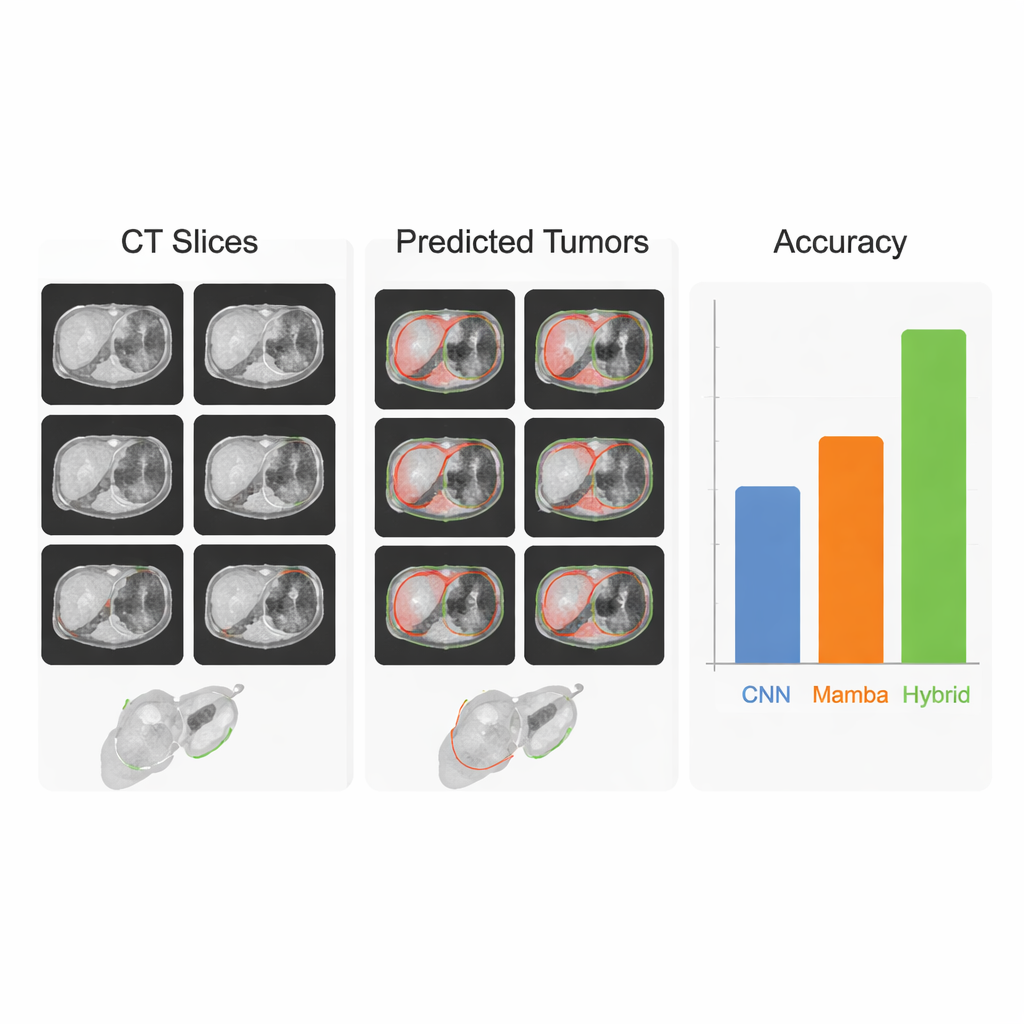
Z wyników laboratoryjnych do wsparcia klinicznego
Dla osoby niezwiązanej z dziedziną kluczowa konkluzja jest taka, że praca ta przybliża oprogramowanie do mapowania guzów do tego, czego naprawdę potrzebują lekarze: narzędzia, które są jednocześnie godne zaufania i wydajne. Łącząc dwa komplementarne sposoby „widzenia” — jeden doskonały w drobnych detalach, drugi w szerokim obrazie — HMC‑Transducer rysuje guzy wątrobowe i nerkowe dokładniej i bardziej niezawodnie niż wcześniejsze systemy, przy jednoczesnym działaniu na standardowym, zaawansowanym sprzęcie szpitalnym. Choć przed rutynowym zastosowaniem klinicznym potrzebne są dalsze kroki, w tym szersze testy na innych narządach i rodzajach obrazowania, podejście to stanowi obiecujący postęp w kierunku zautomatyzowanych map guzów 3D, które mogą wspierać szybsze diagnozy, precyzyjniejsze operacje i bardziej spersonalizowaną opiekę onkologiczną.
Cytowanie: Zhu, J., Xu, C., Lei, C. et al. HMC-transducer: hierarchical mamba-CNN transducer for robust liver tumor segmentation. npj Digit. Med. 9, 176 (2026). https://doi.org/10.1038/s41746-026-02361-7
Słowa kluczowe: segmentacja guzów wątroby, AI w obrazowaniu medycznym, uczenie głębokie, analiza tomografii komputerowej, hybrydowe sieci neuronowe