Clear Sky Science · pl
Zastosowanie i perspektywy sztucznej inteligencji w obrazowaniu diagnostycznym raka prostaty
Dlaczego mądrzejsze skany mają znaczenie dla zdrowia mężczyzn
Rak prostaty jest jednym z najczęstszych nowotworów u mężczyzn, a wczesne wykrycie może decydować o tym, czy problem będzie stosunkowo niewielki, czy zagrażający życiu. Niniejszy przegląd wyjaśnia, jak sztuczna inteligencja (SI) wpleciona zostaje w nowoczesne badania obrazowe, aby szybciej wykrywać raka prostaty, oceniać jego złośliwość i śledzić skuteczność leczenia. Dla czytelników daje to wgląd w to, jak komputery stają się cichymi partnerami w pracowni obrazowej, pomagając lekarzom podejmować szybsze, bardziej spójne decyzje, a jednocześnie rodząc nowe pytania dotyczące danych, sprawiedliwości i zaufania.
Od niewyraźnych cieni do obrazów bogatych w dane
Lekarze korzystają z kilku narzędzi obrazowych, aby poszukiwać raka prostaty. Ultrasonografia jest szybka i tania, lecz ma trudności z odróżnieniem nowotworu od niegroźnego powiększenia czy stanu zapalnego. Rezonans magnetyczny (MRI) daje szczegółowy obraz tkanek miękkich i stał się testem z wyboru przy klinicznie istotnym raku prostaty, choć jego interpretacja zajmuje czas, a nawet eksperci często się nie zgadzają. Badania PET/CT z izotopami wiążącymi się z białkiem PSMA na komórkach nowotworowych świetnie wykrywają przerzuty do kości i węzłów chłonnych, ale mogą nie zauważyć bardzo małych ognisk i są kosztowne. SI nie zastępuje tych urządzeń; działa na obrazach, które one generują. Algorytmy najpierw oczyszczają i segmentują skany, a potem wydobywają subtelne wzory jasności, tekstury i kształtu. Te niewidoczne wskazówki, połączone z wynikami badań laboratoryjnych jak stężenie PSA, służą do uczenia modeli, które potrafią wskazać podejrzane obszary, oszacować ryzyko raka i zasugerować miejsca biopsji lub sposoby oceny odpowiedzi na leczenie.
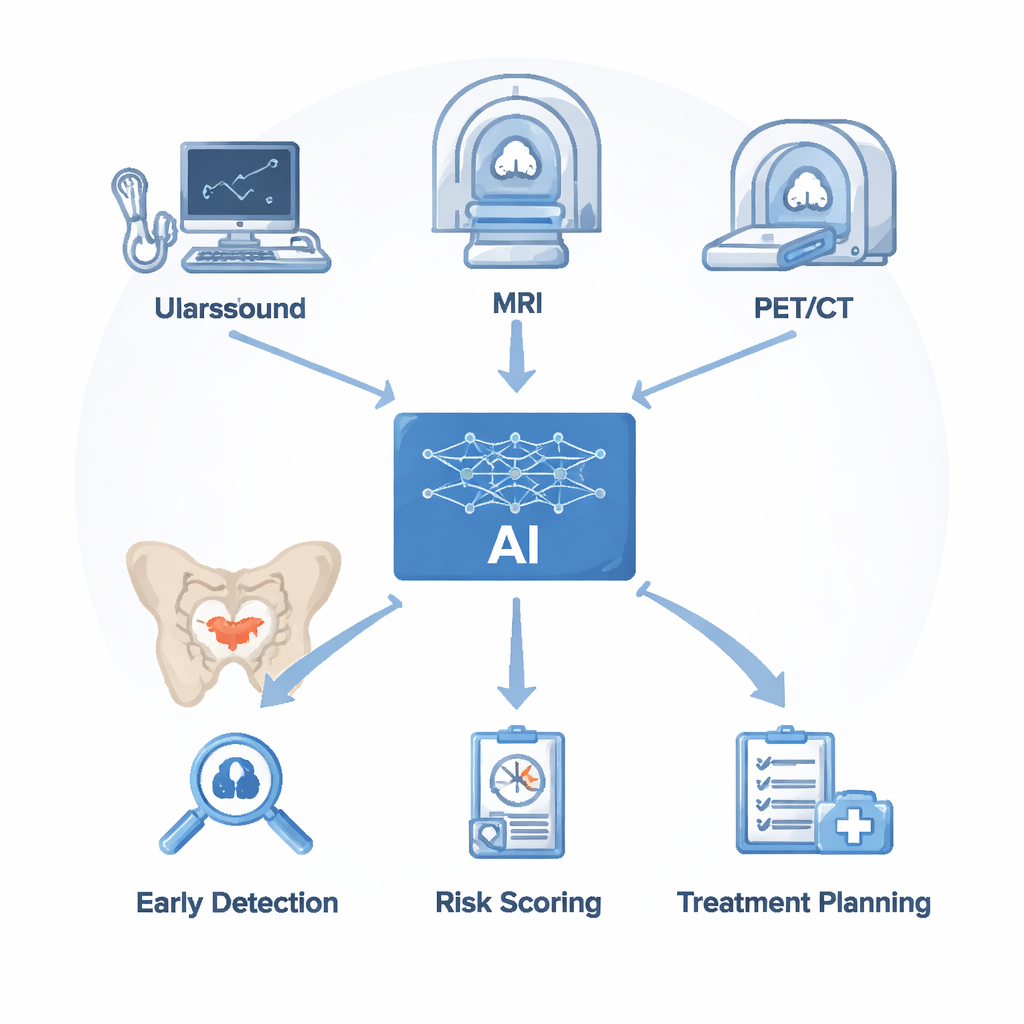
Nauczanie komputerów widzenia tego, co przeoczają radiolodzy
W ultrasonografii systemy SI uczą się na setkach przykładów, aby wychwycić obszary nowotworowe, które mogą stapiać się z tłem. Modele głębokiego uczenia potrafią automatycznie zlokalizować prostatę i w czasie rzeczywistym podświetlić prawdopodobne guzy, czasem dorównując lub przewyższając doświadczonych sonografistów, przy zachowaniu szybkości i zmniejszeniu liczby pominiętych drobnych zmian. Podejścia radiomiczne idą krok dalej, zamieniając obrazy ultrasonograficzne w duże zbiory liczb opisujących wzory tkankowe zbyt złożone dla oka ludzkiego. Modele uczenia maszynowego oparte na tych cechach wyraźnie przewyższały tradycyjne USG i samo PSA, zwłaszcza u mężczyzn z poziomami PSA mieszczącymi się w mylącej „strefie szarej”, gdzie starsze metody często błędnie klasyfikują niemal połowę przypadków. Podobne pomysły napędzają SI na MRI, gdzie zaawansowane sieci automatycznie obrysowują prostatę i jej strefy wewnętrzne, skracając ręczne konturowanie z około 20 minut do nieco ponad minuty i znacząco poprawiając zgodność między różnymi czytelnikami.
Dokładniejsze oszacowania ryzyka i inteligentniejsze śledzenie leczenia
SI błyszczy zwłaszcza wtedy, gdy łączy informacje z wielu sekwencji MRI pokazujących anatomię, ruch wody i przepływ krwi. Modele oparte na transformatorach, zaadaptowane z przetwarzania języka, łączą te dane, by tworzyć mapy prawdopodobieństwa klinicznie istotnych guzów. W testach na dużych grupach pacjentów takie systemy dorównywały lub przewyższały starszych radiologów, szczególnie w wykrywaniu drobnych guzów poniżej centymetra, które ludzie często przeoczają. W dynamicznym MRI z kontrastem modele analizujące szereg czasowy potrafią czytać zmieniające się krzywe jasności barwnika, oceniając, jak „przeciekliwe” są naczynia guza — wskaźnik powiązany z bardziej agresywną chorobą i wyższym ryzykiem nawrotu. W PSMA PET/CT trójwymiarowe sieci trenowane na skanach całego ciała automatycznie wykrywają przerzuty kostne i w węzłach chłonnych, mierzą całkowite obciążenie nowotworem i odnoszą je do czasu wolnego od progresji. Inne narzędzia SI porównują skany wykonane przed i krótko po hormonoterapii lub chemioterapii, przewidując wynik leczenia w ciągu kilku miesięcy znacznie wcześniej niż tradycyjne reguły oparte na prostych zmianach wychwytu.
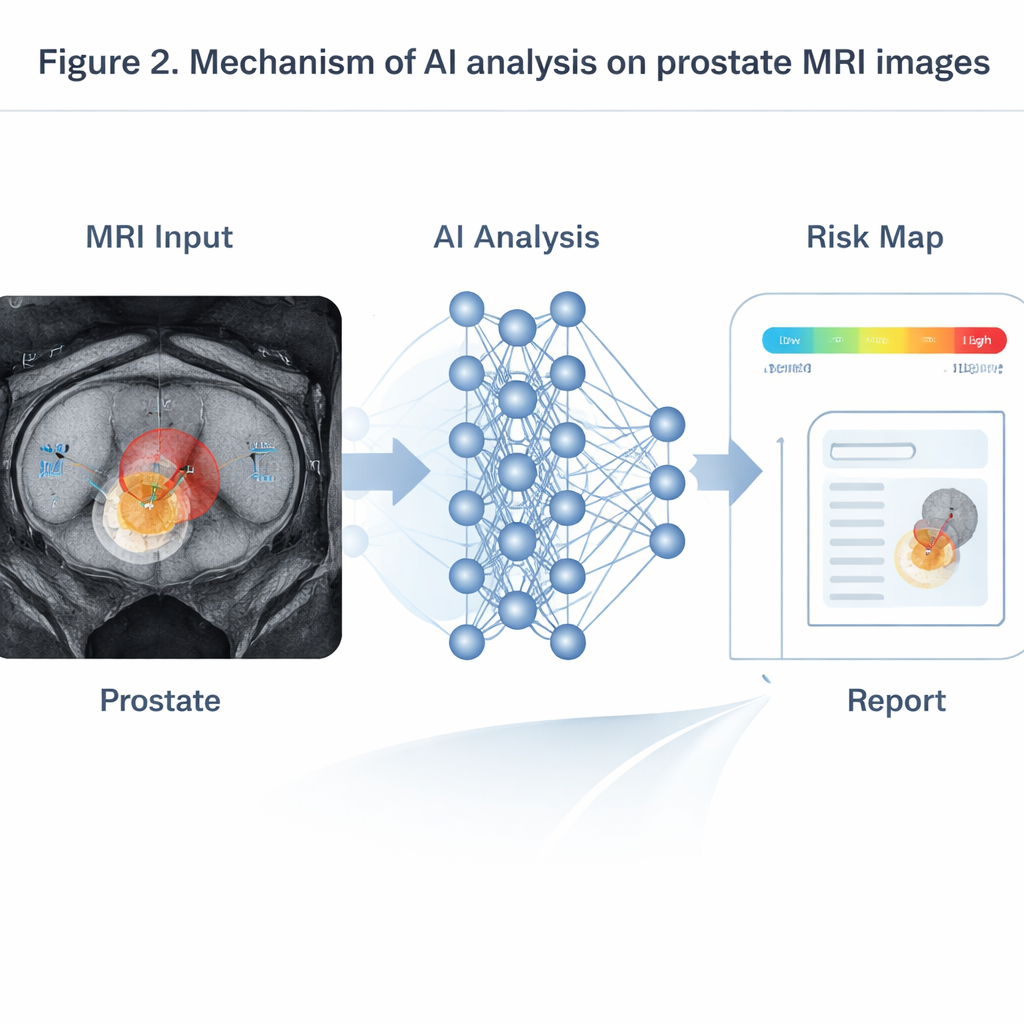
Przeszkody: luki w danych, czarne skrzynki i uczciwe użycie
Pomimo tych postępów rzeczywiste wdrożenie napotyka poważne przeszkody. Wysokiej jakości, dobrze oznakowane dane obrazowe są wciąż ograniczone i skoncentrowane na dużych szpitalach akademickich, podczas gdy skany z mniejszych ośrodków i zróżnicowanych populacji są niedoreprezentowane. Subtelne różnice między markami aparatów, ustawieniami i jakością obrazu mogą sprawić, że modele wytrenowane w jednym miejscu nie będą działać w innym. Wiele potężnych systemów SI działa jako „czarne skrzynki”, dostarczając jedynie wynik ryzyka bez jasnego uzasadnienia, co podważa zaufanie lekarzy — zwłaszcza gdy komputer nie zgadza się z doświadczeniem. Przegląd porusza też kwestie prywatności, ograniczeń w udostępnianiu danych oraz ryzyko, że modele będą działać gorzej dla niektórych grup, co może poszerzać nierówności zdrowotne, jeśli nie będą starannie monitorowane i korygowane.
Budowanie godnych zaufania partnerów w klinice
Patrząc w przyszłość, autorzy wyobrażają sobie SI jako zaufanego współpracownika, a nie tajemniczego wyrocznię. Opisują wysiłki na rzecz budowy dużych, współdzielonych zbiorów danych między szpitalami przy jednoczesnym zachowaniu prywatności poprzez techniki takie jak uczenie federowane, gdzie wymieniane są jedynie aktualizacje modelu — a nie surowe dane pacjentów. Nowe narzędzia „wyjaśnialnej SI” mają pokazywać, które obszary obrazu wpłynęły na decyzję i powiązać je z rozpoznaną patologią, dając lekarzom konkretne powody do zgody lub niezgody. Zamiast modeli uniwersalnych, powstaną systemy dostosowane do konkretnych zadań: przesiewania w zatłoczonych przychodniach, prowadzenia biopsji, monitorowania leczenia czy kontrolowania pacjentów wysokiego ryzyka. Łączenie obrazowania z danymi genetycznymi i klinicznymi może dodatkowo dopracować rokowanie i spersonalizować terapię. Dla pacjentów główny wniosek jest zachęcający: jeśli wyzwania techniczne, etyczne i regulacyjne zostaną rozwiązane właściwie, obrazowanie wspierane przez SI może oznaczać wcześniejsze wykrycie, mniej niepotrzebnych biopsji, szybsze odpowiedzi i bardziej dopasowane plany leczenia raka prostaty.
Cytowanie: Wang, X., Zhong, S., Fang, K. et al. Application and prospect of artificial intelligence in diagnostic imaging of prostate cancer. npj Digit. Med. 9, 168 (2026). https://doi.org/10.1038/s41746-026-02354-6
Słowa kluczowe: obrazowanie raka prostaty, sztuczna inteligencja, MRI i ultrasonografia, PSMA PET/CT, radiomika