Clear Sky Science · pl
Maskowane autoenkodowanie, uogólnialne wstępne uczenie i zintegrowani eksperci dla lepszej segmentacji glejaków
Dlaczego inteligentniejsze skany mają znaczenie przy nowotworach mózgu
Guzy mózgu zwane glejakami należą do najgroźniejszych nowotworów, a mimo to lekarze wciąż poświęcają dużo czasu na ręczne obrysowywanie granic guza na skanach MRI. To dokładne wyznaczanie granic kieruje operacją i radioterapią, ale może trwać 15–20 minut na pacjenta i trzeba je powtarzać w czasie. W badaniu przedstawiono system sztucznej inteligencji MAGPIE, który uczy się na dziesiątkach tysięcy skanów mózgu bez etykiet od ludzi, a następnie wymaga zaledwie garstki przypadków z eksperckim oznaczeniem, by wiarygodnie mapować glejaki. Dla pacjentów może to oznaczać szybsze i bardziej spójne planowanie leczenia nawet w szpitalach, które nie dysponują dużymi, ręcznie skatalogowanymi zbiorami danych.
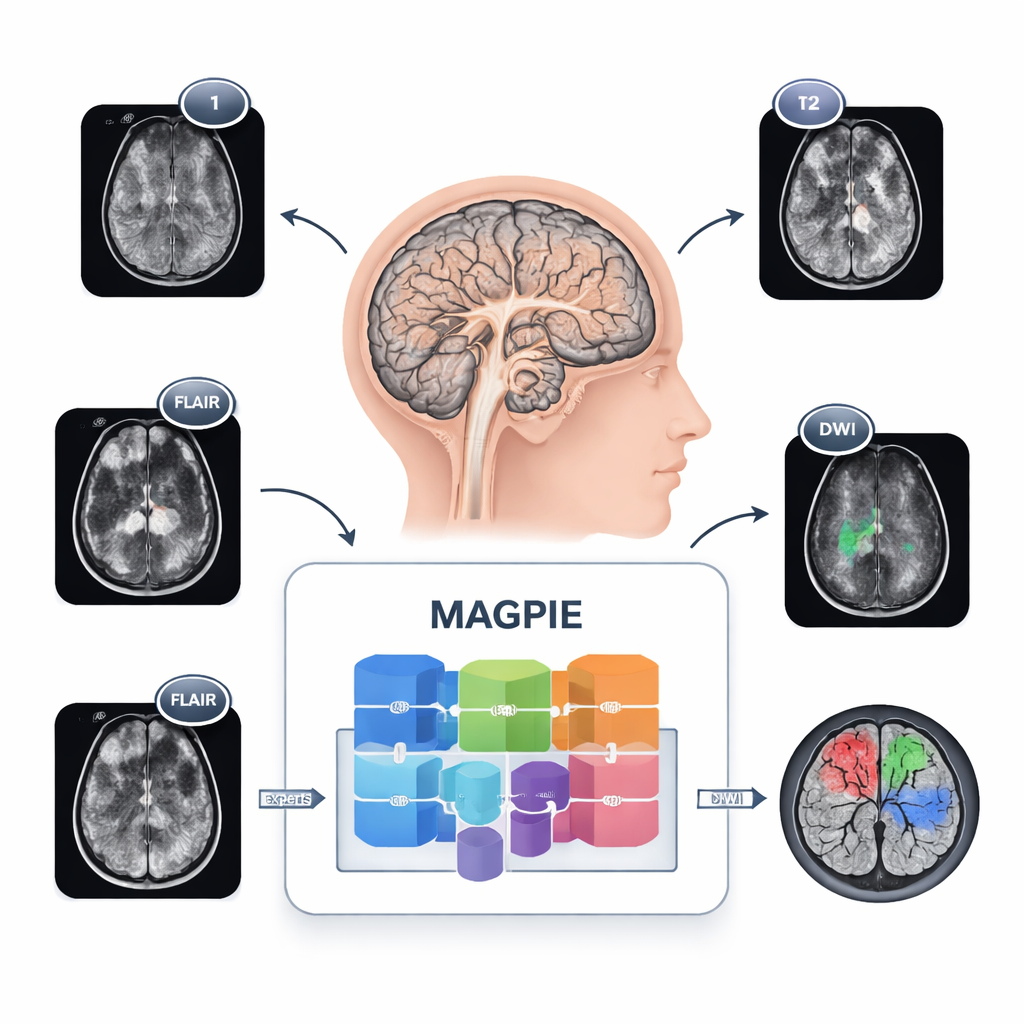
Widzenie guzów w nowy sposób
Glejaki trudno odwzorować, ponieważ nie tworzą regularnych kul. Komórki nowotworowe rozprzestrzeniają się wzdłuż włókien mózgu, tworząc rozmyte granice i drobne satelitarne ogniska, które trudno dostrzec. Różne placówki używają też różnych ustawień MRI i kombinacji sekwencji, więc narzędzie wytrenowane w jednym miejscu może zawieść w innym. MAGPIE rozwiązuje te problemy jednocześnie. Najpierw został wystawiony na 43 505 nieoznakowanych skanów MRI mózgu pochodzących z wielu badań i typów skanerów. W tej fazie uczył się ogólnych wzorców tkanki zdrowej i chorej, próbując odtwarzać brakujące fragmenty obrazów oraz porównując różne zmodyfikowane widoki tego samego mózgu, co zmuszało go do skupienia się na stabilnych, istotnych cechach zamiast kruchego poziomu pikseli.
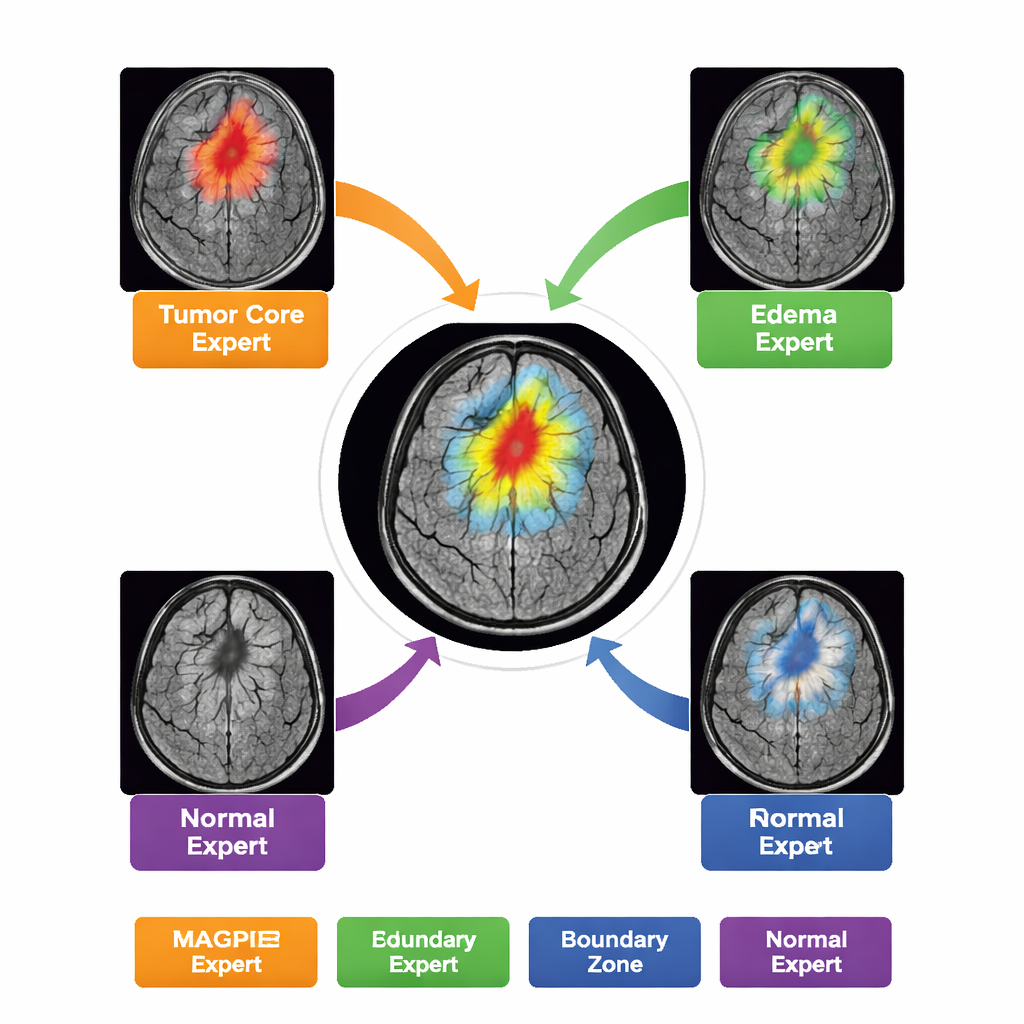
Puszczenie pracy w ręce wielu ekspertów
Zamiast działać jako pojedynczy, monolityczny model, MAGPIE zawiera „mieszankę ekspertów” wewnątrz. Analizując nowy skan, aktywuje tylko niewielki podzbiór ośmiu wyspecjalizowanych pod-sieci dla każdego regionu obrazu. W trakcie treningu eksperci ci naturalnie dzielą się zadaniami: niektórzy stają się czuli na jasny, aktywnie rosnący brzeg guza; inni skupiają się na martwym jądrze; jeszcze inni uczą się rozmytej strefy obrzęku wokół guza; a część koncentruje się głównie na normalnym tle mózgu i granicach anatomicznych. Autorzy pokazują to, mierząc, jak silnie aktywność każdego eksperta pokrywa się z różnymi strefami guza zaznaczonymi przez radiologów. Ten podział pracy poprawia dokładność, jednocześnie utrzymując koszty obliczeniowe na rozsądnym poziomie — dla dowolnego fragmentu obrazu aktywna jest tylko około połowa parametrów modelu.
Radzenie sobie z nieporządnymi, rzeczywistymi skanami
Protokoły kliniczne MRI są dalekie od jednolitości. U niektórych pacjentów dostępne są cztery sekwencje, u innych mniej; urządzenia różnych producentów generują nieco odmienne obrazy. Konstrukcja MAGPIE traktuje każdą sekwencję MRI jak oddzielny „token” i uczy się, ile wagi przypisać każdej z nich w locie, zamiast oczekiwać stałego zestawu wejść w ustalonej kolejności. To podejście niezależne od kanałów pozwala systemowi dostosować się, gdy np. brakuje sekwencji z kontrastem, ale dostępna jest FLAIR. Model używa też zaawansowanych mechanizmów uwagi, które pozwalają mu jednocześnie „widzieć daleko”, wychwytując rozprzestrzenianie się wzdłuż dróg istoty białej, oraz „widzieć precyzyjnie”, wykrywając bardzo małe zmiany o rozmiarze kilku milimetrów.
Więcej wyników przy znacznie mniejszej liczbie etykiet
Po wstępnym przetrenowaniu badacze dostroili MAGPIE na zaledwie 20 w pełni oznaczonych przypadkach glejaków i porównali go ze standardowymi modelami trenowanymi od zera w tych samych warunkach. Na znaczącym benchmarku nowotworów mózgu (BraTS21) MAGPIE osiągnął wynik Dice — powszechnie stosowany miarę nakładania w obrazowaniu medycznym — na poziomie około 61%, przewyższając najlepszą wersję trenowaną od zera o około 2,6 punktu procentowego i wyprzedzając silną wcześniejszą metodę samonadzorowaną bez przejawów szkodliwego „negatywnego transferu”. Na trudnych danych spoza rozkładu — skanach z różnych chorób, typów skanerów i ustawień obrazowych — również spisywał się lepiej, osiągając ponad 70% Dice na jednym zbiorze zmian w istocie białej bez dodatkowego dostrajania. Kluczowe jest to, że taki poziom wydajności zwykle wymaga rzędu 400 oznaczonych przypadków; MAGPIE osiąga go przy użyciu tylko około 5% tego wysiłku.
Co to może znaczyć dla pacjentów i placówek
Dla osób niebędących ekspertami główny przekaz jest taki, że MAGPIE zamienia górę nieoznakowanych skanów MRI w potężnego asystenta, który potrzebuje bardzo niewiele eksperckiego treningu, by stać się klinicznie użyteczny. Może obrysowywać złożone guzy mózgu z realistycznymi granicami, wykrywać małe satelitarne ogniska, które inne systemy pomijają, i działać niezawodnie, gdy skany pochodzą z nieznanych urządzeń lub brakuje w nich niektórych sekwencji. Taka kombinacja może skrócić czas adnotacji radiologów o około 95%, obniżyć próg wdrożenia zaawansowanej AI w mniejszych szpitalach oraz wspierać bardziej precyzyjne planowanie zabiegów chirurgicznych i radioterapii. Choć potrzebna jest dalsza walidacja na rzadkich typach guzów i przypadkach o niskim stopniu złośliwości, badanie pokazuje, jak starannie zaprojektowane uczenie samonadzorowane może przybliżyć wydajną i odporną segmentację guzów mózgu do codziennej praktyki klinicznej.
Cytowanie: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
Słowa kluczowe: segmentacja glejaków, rezonans magnetyczny mózgu, uczenie samonadzorowane, mieszanka ekspertów, AI w obrazowaniu medycznym