Clear Sky Science · pl
Wieloośrodkowa ocena interpretowalnej sztucznej inteligencji w diagnostyce choroby wieńcowej na podstawie biomarkerów PET
Dlaczego liczy się AI w skanowaniu serca
Choroba wieńcowa, czyli gromadzenie się złogów miażdżycowych mogących ograniczać przepływ krwi do serca, pozostaje jedną z głównych przyczyn zawałów i zgonów na świecie. Współczesne badania obrazowe, takie jak skany PET/CT, potrafią ujawnić przepływ krwi, funkcję serca oraz zwapnienia w tętnicach, ale ogrom informacji może przytłoczyć nawet doświadczonych czytelników. W tym badaniu sprawdzono, jak interpretowalny model sztucznej inteligencji może złożyć te elementy w jeden, łatwy w użyciu wskaźnik, który pomaga lekarzom dokładniej wykrywać groźne zwężenia — i jednocześnie jasno pokazywać, które wyniki wpływają na jego decyzję.
Łączenie wielu sygnałów sercowych w jedną całość
Podczas badania PET/CT serca lekarze mogą ocenić, jak dobrze krew przepływa przez mięsień sercowy w spoczynku i podczas wysiłku, jak mocno serce pompuje oraz ile wapnia — wskaźnika długoterminowego nagromadzenia blaszek — znajduje się w tętnicach wieńcowych. Tradycyjnie klinicyści analizują te pomiary pojedynczo, a następnie łączą je mentalnie, aby ocenić prawdopodobieństwo zwężeń. Ta mentalna integracja jest trudna i bywa niejednolita, a nie istnieje uniwersalnie uzgodniona metoda ważenia przepływu, defektów perfuzyjnych i wyników skoringu wapnia razem. Badacze postanowili zbudować narzędzie AI, które połączy dziesięć rutynowo dostępnych pomiarów z badań obrazowych oraz płeć pacjenta w jedną wartość prawdopodobieństwa obecności istotnych zwężeń tętnic.
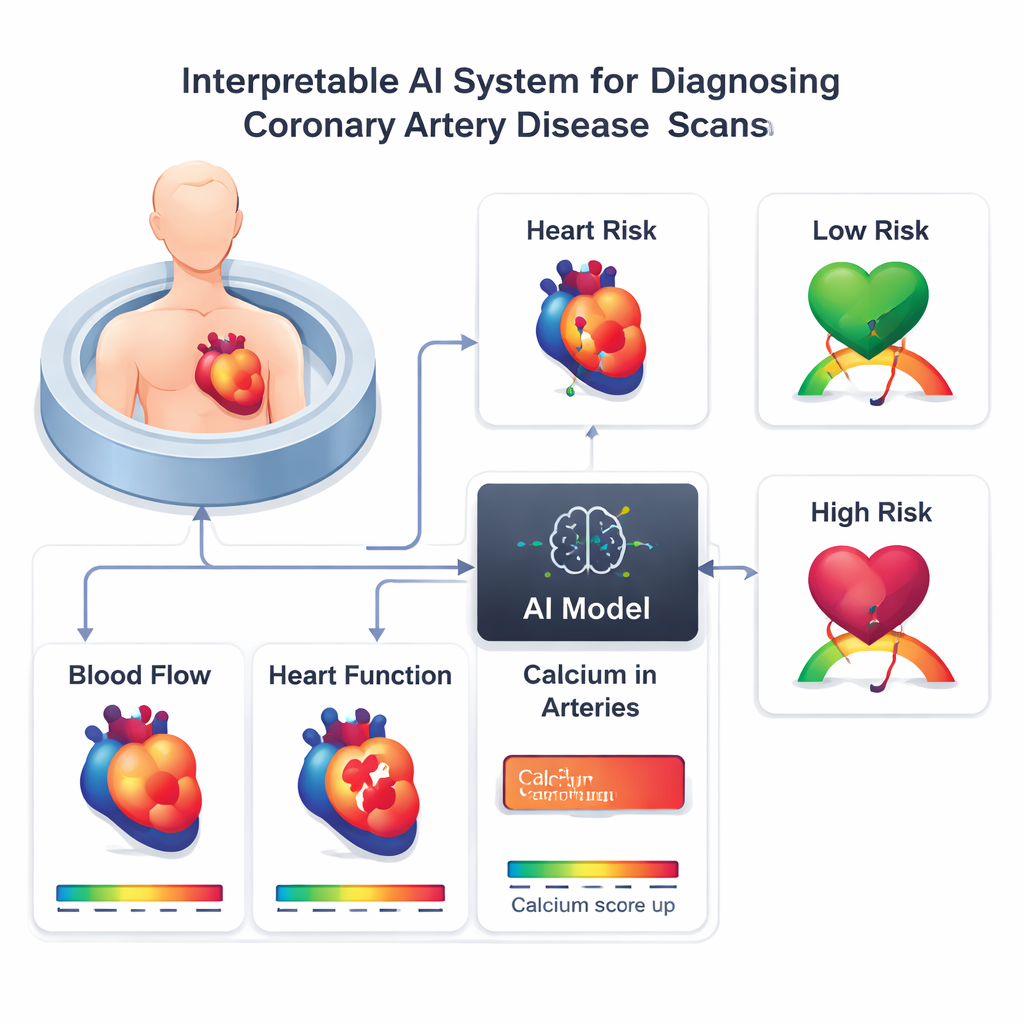
Jak przeprowadzono badanie
Zespół korzystał z dużego międzynarodowego rejestru obejmującego 17 348 pacjentów, u których wykonano badania PET/CT serca. Z tej grupy skupili się na 1 664 osobach z czterech ośrodków, które nie miały wcześniejszych zawałów ani pomostowań i które przeszły inwazyjną koronarografię — badanie rentgenowskie z kontrastem używane jako złoty standard do potwierdzania zwężeń. Dane z jednego szpitala (386 pacjentów) posłużyły do trenowania i dopracowania modelu AI, podczas gdy dane z pozostałych trzech szpitali (1 278 pacjentów) zostały odłożone do zewnętrznego testu. Model AI oparty na technice uczenia maszynowego XGBoost używał dziesięciu cech pochodzących ze skanów, w tym przepływu krwi w warunkach wysiłku, rezerwy przepływu, wielkości defektów perfuzyjnych, wyników skoringu wapnia automatycznie mierzonych z obrazów CT, siły skurczu oraz miary zmian rozmiaru serca pod wpływem stresu.
Jak dobrze działała AI
W zewnętrznej grupie testowej, gdzie około połowa pacjentów rzeczywiście miała chorobę wieńcową z istotnymi zwężeniami, model AI wyraźnie przewyższył zarówno pojedyncze pomiary, jak i doświadczonych lekarzy. Według powszechnie stosowanej miary dokładności — pola pod krzywą ROC — AI osiągnęło wartość 0,83, w porównaniu do 0,80 dla eksperckich ocen klinicznych, 0,79 dla głównego wskaźnika perfuzji, 0,75 dla rezerwy przepływu i 0,69 dla samego wapnia. Gdy badacze dostosowali próg tak, by AI oznaczało podobny odsetek pacjentów jako „prawidłowych” co tradycyjne progi, AI wykrywało więcej pacjentów wysokiego ryzyka z zaawansowaną chorobą wielonaczyniową. Jego działanie było stabilne u mężczyzn i kobiet, u pacjentów młodszych i starszych oraz u osób z otyłością i bez niej, co sugeruje szeroką przydatność podejścia.
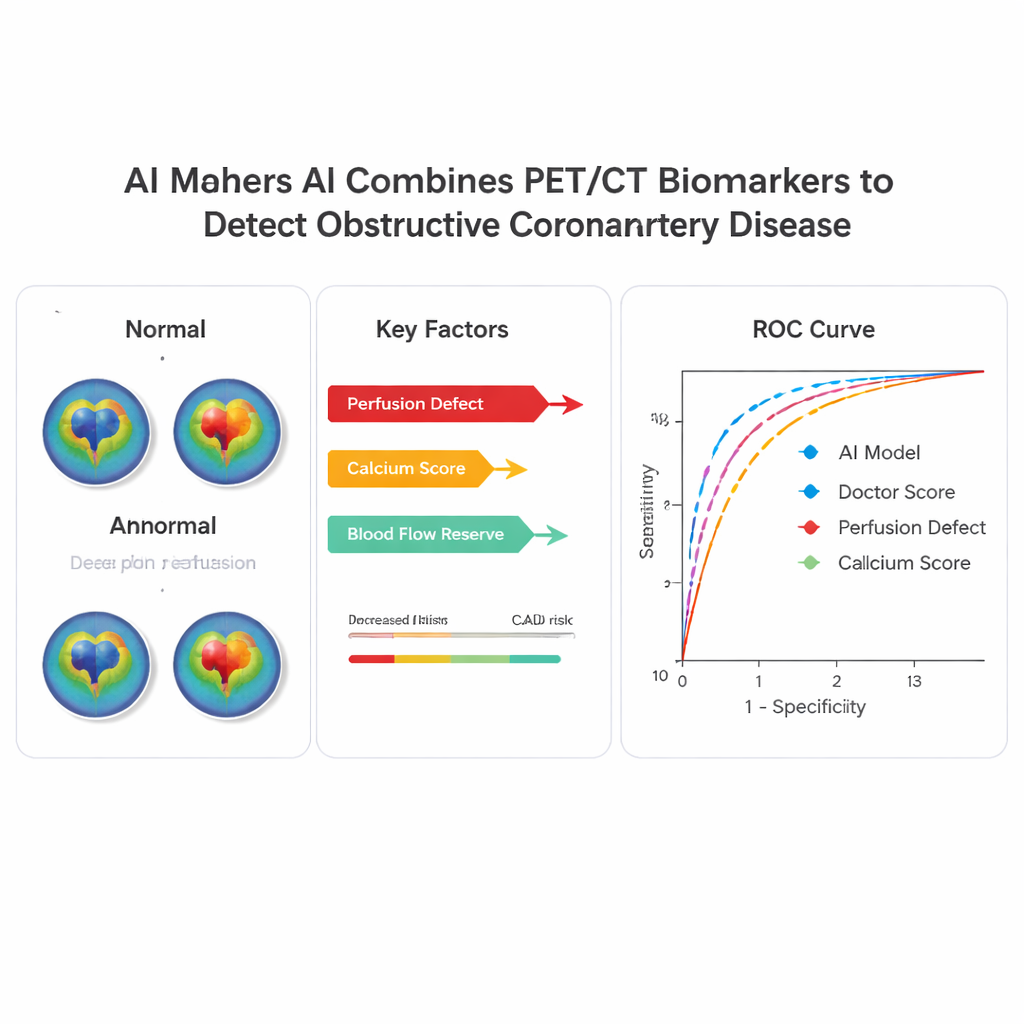
Ujawnianie logiki AI
Jednym z głównych zastrzeżeń dotyczących zaawansowanych algorytmów w medycynie jest to, że mogą zachowywać się jak „czarne skrzynki”, dając prognozy bez wyjaśnień. Aby temu zapobiec, autorzy zastosowali technikę analizy SHAP, aby pokazać, które cechy skanu najsilniej wpływały na każde indywidualne przewidzenie. W całym badaniu najważniejszymi czynnikami były ilość mięśnia sercowego o zmniejszonym przepływie, ogólny ciężar wapnia oraz rezerwa przepływu. Na przykład u jednego zaprezentowanego pacjenta z ciężko obniżonym przepływem i wynikami angiografii wskazującymi wysokie ryzyko, AI przypisało wysokie prawdopodobieństwo choroby głównie ze względu na niską rezerwę przepływu. U innego pacjenta z granicznymi wynikami perfuzji, ale prawidłowym przepływem i zerowym wapniem, AI prawidłowo wskazało niskie prawdopodobieństwo choroby, w przeciwieństwie do bardziej alarmującej oceny lekarza. Takie wyjaśnienia dotyczące pojedynczych przypadków mogą pomóc klinicystom zaufać i zweryfikować decyzje wspierane przez AI.
Co to oznacza dla pacjentów
Praca ta przedstawia pierwszy wieloośrodkowy, zewnętrznie przetestowany system AI, który łączy standardowe pomiary z PET/CT serca i automatyczny skoring wapnia w celu diagnostyki choroby wieńcowej. Model dostarcza pojedynczą, interpretowalną ocenę ryzyka, która często przewyższa dokładnością ekspertów, wskazując jednocześnie konkretne cechy skanu stojące za każdą oceną. Chociaż narzędzie nie jest jeszcze zatwierdzone do rutynowego użycia klinicznego i potrzebne są dalsze badania prospektywne, wyznacza kierunek ku przyszłości, w której wyniki badań obrazowych serca będą streszczane w przejrzyste, spersonalizowane wskaźniki ryzyka, pomagające lekarzom pewniej decydować, kto wymaga inwazyjnych badań lub intensywnego leczenia — a kto może bezpiecznie ich uniknąć.
Cytowanie: Zhang, W., Kwiecinski, J., Shanbhag, A. et al. Multicenter evaluation of interpretable AI for coronary artery disease diagnosis from PET biomarkers. npj Digit. Med. 9, 154 (2026). https://doi.org/10.1038/s41746-026-02338-6
Słowa kluczowe: choroba wieńcowa, kardiologiczny PET CT, sztuczna inteligencja, skoring wapnia, przepływ krwi w mięśniu sercowym