Clear Sky Science · pl
Uczenie wielozadaniowe uwzględniające strukturę z generalizacją domenową dla odpornej analizy kręgów na tomografiach komputerowych kręgosłupa
Dlaczego lepsze skany kręgosłupa mają znaczenie
Ból pleców, złamania i guzy kręgosłupa dotykają miliony osób, a odczytywanie tomografii komputerowych kręgosłupa jest żmudną pracą dla radiologów. Każde badanie może zawierać dziesiątki kręgów i subtelne oznaki uszkodzeń, które łatwo przeoczyć — zwłaszcza gdy obrazy pochodzą z wielu różnych szpitali i aparatów. W tym badaniu przedstawiono nowy system sztucznej inteligencji (AI), zwany VertebraFormer, zaprojektowany do automatycznego wyznaczania obrysu każdego kręgu, przypisywania jego prawidłowego miejsca w kręgosłupie oraz wskazywania podejrzanych zmian, przy jednoczesnym zachowaniu niezawodności w szerokim zakresie rzeczywistych badań.
Jeden system dla wielu problemów kręgosłupa
Zamiast tworzyć oddzielne algorytmy dla każdego zadania, badacze opracowali zunifikowany model, który jednocześnie wykonuje trzy zadania: rysuje dokładne obrysy wszystkich kręgów, numeruje je od szyi w dół do odcinka lędźwiowego oraz wskazuje obszary mogące odpowiadać złamaniom, przerzutom nowotworowym lub innym uszkodzeniom. VertebraFormer oparty jest na nowoczesnej architekturze „transformera”, początkowo spopularyzowanej w przetwarzaniu języka i obrazów, która szczególnie dobrze wykrywa wzorce rozciągające się na duże odległości. To ma kluczowe znaczenie dla kręgosłupa, gdzie kształt pojedynczego kręgu nabiera sensu tylko w kontekście całej kolumny.
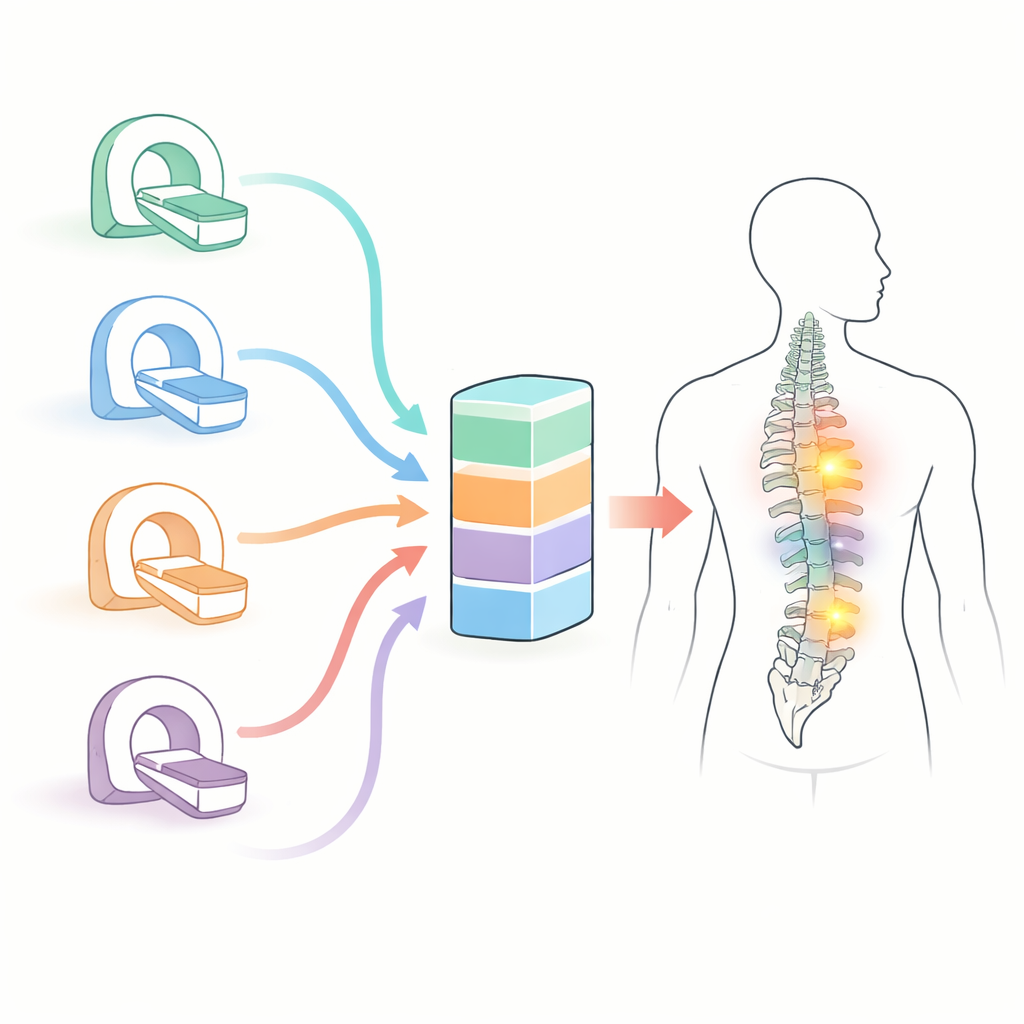
Różnorodny benchmark rzeczywistych badań
Aby sprawdzić, czy ich system zda egzamin poza jednym laboratorium czy szpitalem, zespół zebrał nowy benchmark nazwany MultiSpine. Łączy on sześć różnych zestawów danych, w tym duże publiczne kolekcje i prywatne kohorty szpitalne, obejmujące odcinki szyjny, piersiowy i lędźwiowy, a w niektórych przypadkach zarówno TK, jak i MRI. Badania pozyskano na skanerach różnych marek przy różnych protokołach obrazowania, a eksperci-radiolodzy anotowali obrysy kręgów, ich oznaczenia anatomiczne oraz — gdy dostępne — obszary patologii. Autorzy podjęli również nadzwyczajne środki, by upewnić się, że nie ma ukrytych duplikatów między zestawami, uważnie śledząc identyfikatory badań i stosując „perceptual hashing” do wykrywania niemal identycznych obrazów.
Jak AI uczy się struktury kręgosłupa i zmian
W VertebraFormer wspólny enkoder najpierw przekształca trójwymiarowe badanie kręgosłupa w zestaw „łat” i uczy się, jak te fragmenty odnoszą się do siebie w całej kolumnie. Na tej wspólnej bazie osadzone są trzy wyspecjalizowane gałęzie. Jedna rekonstruuje szczegółową trójwymiarową maskę wszystkich kręgów. Druga koncentruje się po kolei na każdym kręgu, wykorzystując jego położenie i otoczenie, aby zdecydować, czy to np. T11 czy L3. Trzecia gałąź generuje mapy cieplne, które najsilniej świecą tam, gdzie prawdopodobne jest wystąpienie zmiany. Co istotne, model zawiera też jednostkę „dynamicznej modulacji”, która wyczuwa styl obrazowania — różnice między skanerami, protokołami, a nawet TK i MRI — i subtelnie dostosowuje wewnętrzne przetwarzanie, dążąc do utrzymania dokładności nawet wobec nieznanych typów badań.
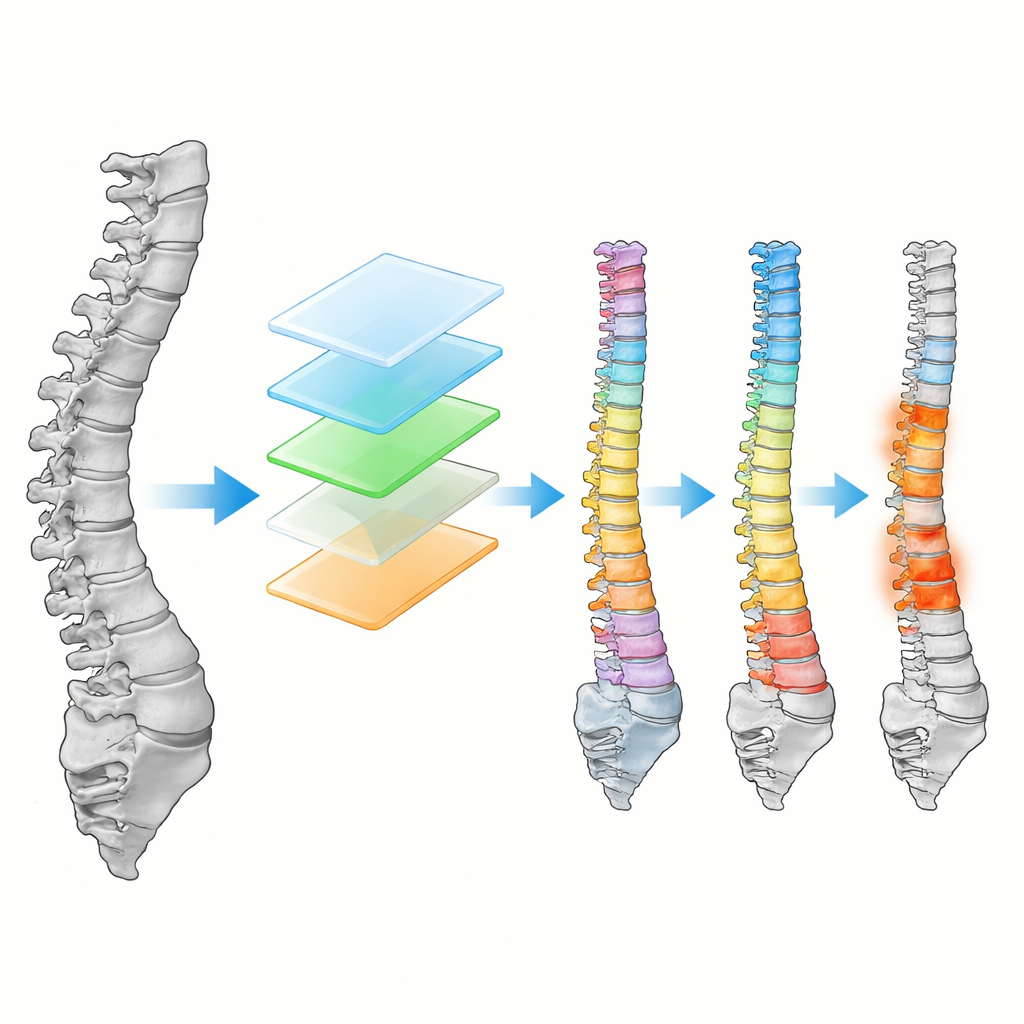
Sprawdzanie odporności
Badacze porównali VertebraFormer z wiodącymi modelami analizy kręgosłupa na zbiorze MultiSpine. System konsekwentnie osiągał wyższą dokładność w wyznaczaniu obrysów kręgów, prawidłowym numerowaniu oraz wykrywaniu zmian. W trudniejszym teście „zero-shot” model trenowano na kilku zestawach, a następnie oceniano na całkowicie nieznanym, co naśladuje wdrożenie w nowym szpitalu. I tutaj VertebraFormer przewyższał alternatywy i wykazywał jedynie umiarkowany spadek wydajności. Zespół przeanalizował projekt poprzez badania ablacjne, wykazując, że każdy dodany komponent — gałąź identyfikacyjna, detektor zmian i szczególnie blok modulacji domeny — wnosił mierzalne korzyści. Pomimo zaawansowania model przetwarza około 14 pełnych wolumenów 3D na sekundę na nowoczesnym sprzęcie, przewyższając równoważnie szybki wielosieciowy pipeline we wszystkich trzech zadaniach.
Radzenie sobie z zaszumionymi i przesuniętymi danymi
Rzeczywiste badania kliniczne są dalekie od ideału, więc autorzy poddali model symulowanym zaburzeniom takim jak dodatkowy szum, przesunięcia intensywności, grubsze plastry oraz artefakty spowodowane metalem. VertebraFormer pozostał stabilny przy umiarkowanych degradacjach i zawiódł dopiero w ekstremalnych warunkach. Pokazali też, że gdy informacje o domenie są błędnie określone, wydajność spada, co potwierdza, że mechanizm modulacji jest istotny, a nie jedynie dekoracyjny. Równocześnie alternatywne strategie adaptacji w locie, takie jak dostosowywanie statystyk cech czy minimalizowanie niepewności predykcji podczas testowania, pomogły odzyskać część wydajności, gdy etykiety domen były niewiarygodne lub niedostępne.
Co to oznacza dla pacjentów i klinicystów
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że VertebraFormer łączy wiele elementów analizy obrazów kręgosłupa w jedno, szybsze i bardziej niezawodne narzędzie AI. Dzięki uczeniu się ogólnej struktury kręgosłupa, adaptacji do różnych skanerów i szpitali oraz jednoczesnemu wykrywaniu anatomii i choroby, zmniejsza potrzebę stosowania wielu oddzielnych systemów i może dostarczać radiologom wyraźne obrysy, spójne numerowanie oraz intuicyjne mapy cieplne podejrzanych obszarów. Choć nadal wymaga prospektywnego testowania w realnych przepływach klinicznych oraz szerszego szkolenia na rzadkich przypadkach i obrazach multimodalnych, praca ta stanowi ważny krok w kierunku zautomatyzowanych ocen kręgosłupa, które są dokładne, interpretowalne i wystarczająco odporne, by wspierać lekarzy tam, gdzie wykonywane są badania.
Cytowanie: Du, J., Ge, H., Zhang, R. et al. Structure-aware multi-task learning with domain generalization for robust vertebrae analysis in spinal CT. npj Digit. Med. 9, 217 (2026). https://doi.org/10.1038/s41746-025-02288-5
Słowa kluczowe: TK kręgosłupa, segmentacja kręgów, detekcja zmian patologicznych, sztuczna inteligencja w obrazowaniu medycznym, generalizacja domenowa