Clear Sky Science · pl
Fibroblasty związane z rakiem o wysokiej ekspresji COL3A1 organizują metaboliczne i immunologiczne mikrośrodowisko, by nadawać oporność na chemioterapię w raku piersi
Dlaczego niektóre guzy piersi ignorują chemioterapię
Chemioterapia może ratować życie w raku piersi, jednak u wielu pacjentek guzy przestają reagować lub nigdy dobrze nie odpowiadają na leczenie. W tym badaniu autorzy spojrzeli poza same komórki nowotworowe na ich otoczenie i zapytali: które pobliskie komórki pomagają guzom przetrwać terapię i w jaki sposób? Odpowiedź skupia się na specjalnej grupie komórek wspierających, które przeorganizowują zarówno odżywianie guza, jak i miejscowy układ odpornościowy, by chronić komórki nowotworowe przed chemioterapią.
Ukryci pomocnicy wokół guza
Guzy piersi to nie tylko komórki nowotworowe; to zróżnicowane społeczności obejmujące naczynia krwionośne, komórki odpornościowe i komórki tkanki łącznej zwane fibroblastami. Gdy fibroblasty osiedlają się w guzie, nazywa się je fibroblastami związanymi z rakiem (CAFs) i mogą one hamować lub wspierać rozwój nowotworu. Łącząc kilka zaawansowanych metod profilowania genetycznego na próbkach od pacjentek — analizy pojedynczych komórek, przestrzenne i masowe — oraz eksperymenty laboratoryjne i na zwierzętach, badacze wyizolowali podgrupę CAF o wysokiej ekspresji cząsteczki COL3A1, składnika szkieletu tkanki. Pacjentki, których guzy zawierały więcej tych fibroblastów o wysokim COL3A1, częściej miały słabszą odpowiedź na chemioterapię i gorsze przeżycie.
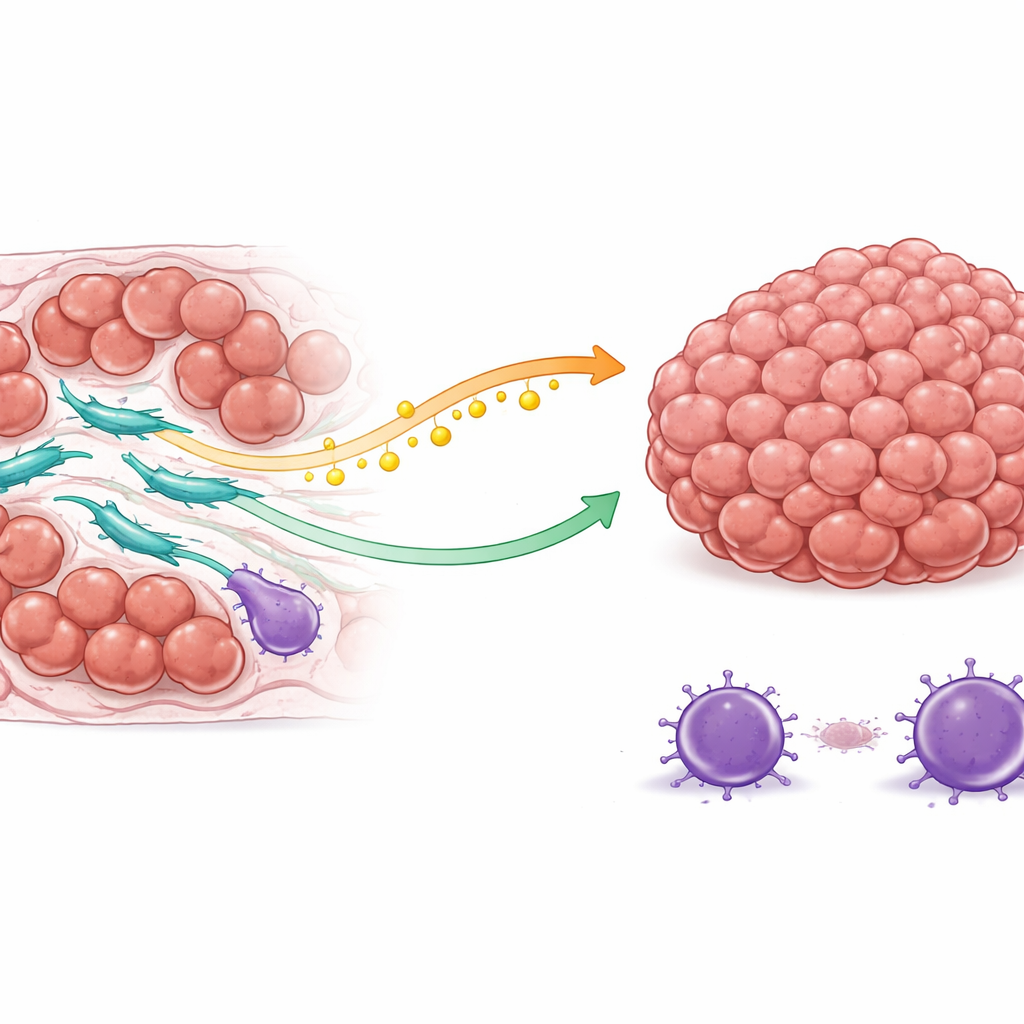
Dwutorowa tarcza: paliwo i ochrona
Zespół odkrył, że fibroblasty o wysokim COL3A1 chronią komórki nowotworowe na dwa główne sposoby. Po pierwsze modyfikują metabolizm lipidów. Te fibroblasty zwiększają aktywność enzymu produkującego kwas oleinowy, rodzaj tłuszczu. Zamiast zatrzymywać to paliwo, uwalniają je do mikrośrodowiska guza. Komórki nowotworowe pobierają kwas oleinowy przez białko powierzchniowe i w odpowiedzi uruchamiają wewnętrzną ścieżkę sygnałową sprzyjającą przeżyciu i odporności na sygnały śmierci. W efekcie, gdy chemioterapia próbuje wywołać programy autodestrukcji w komórkach nowotworowych, te komórki są lepiej przygotowane, by im się oprzeć i nadal się dzielić.
Modelowanie nieprzyjaznego immunologicznego otoczenia
Po drugie, fibroblasty o wysokim COL3A1 przekształcają miejscowy krajobraz immunologiczny na korzyść guza. Dzięki złożonym interakcjom sygnałowym przyciągają limfocyty regulatorowe, typ komórek odpornościowych tłumiących ataki immunologiczne, a jednocześnie zniechęcają lub osłabiają cytotoksyczne limfocyty T, które normalnie atakowałyby nowotwór. Mapowanie przestrzenne rzeczywistych guzów pacjentek wykazało, że te fibroblasty zwykle lokują się blisko zarówno komórek nowotworowych opornych na leki, jak i komórek immunosupresyjnych, podczas gdy skuteczne komórki zabójcze są odsunięte dalej. Takie rozmieszczenie tworzy osłoniętą strefę, gdzie komórki nowotworowe napotykają mniej zagrożeń ze strony układu odpornościowego i jednocześnie stają się trudniejsze do zabicia lekami.
Dowody z badań komórkowych, na myszach i od pacjentek
Aby sprawdzić związek przyczynowo-skutkowy, badacze obniżyli poziom COL3A1 w CAF hodowanych w laboratorium. Gdy komórki raka piersi uprawiano obok tych zmodyfikowanych fibroblastów, tworzyły mniej inwazyjnych struktur, były łatwiej niszczone przez chemioterapeutyk paklitaksel i wykazywały więcej cech programowanej śmierci komórkowej. U myszy wszczepionych mieszankami komórek raka piersi i CAF, zablokowanie COL3A1 w fibroblastach spowolniło wzrost guza podczas chemioterapii i obniżyło poziomy enzymu syntezującego tłuszcze oraz receptora na komórkach nowotworowych związanych z kwasem oleinowym. W grupie 72 pacjentek leczonych chemioterapią przed operacją wyższe poziomy COL3A1 i powiązanych elementów metabolizmu lipidów silnie korelowały ze słabszą odpowiedzią na leczenie i krótszym czasem do nawrotu choroby.
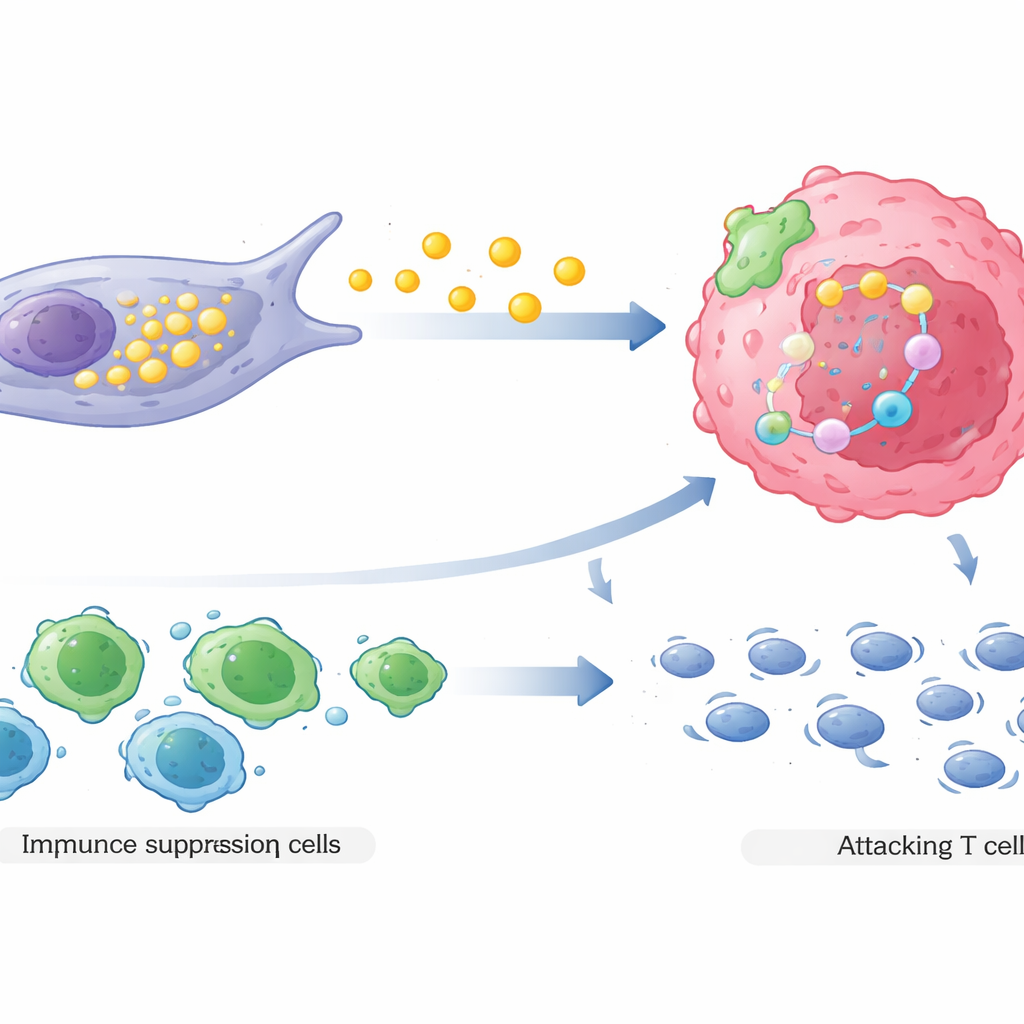
Co to oznacza dla przyszłego leczenia
W skrócie, badanie pokazuje, że określony zestaw komórek wspierających w guzach piersi działa jak jednostka ochronna: dostarcza komórkom nowotworowym dietę opartą na tłuszczach oraz przyciąga sojuszników immunologicznych, którzy tłumią obronę organizmu. Działania te razem zmniejszają skuteczność chemioterapii. Pomiar obfitości fibroblastów o wysokim COL3A1 poprawia zdolność lekarzy do przewidywania, kto zareaguje na leczenie, a ścieżki, których używają — produkcja tłuszczów, sygnalizacja przeżyciowa w komórkach nowotworowych i tłumienie immunologiczne — oferują nowe cele terapeutyczne. W przyszłości terapie, które unieszkodliwią lub przeprogramują te fibroblasty, mogłyby być połączone ze standardową chemioterapią, by zapobiegać rozwijaniu się oporności przez guzy.
Cytowanie: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
Słowa kluczowe: rak piersi, oporność na chemioterapię, mikrośrodowisko guza, fibroblasty związane z rakiem, metabolizm lipidów