Clear Sky Science · pl
Integracja biopsji płynnej i sygnatur mutacyjnych w celu rozwoju onkologii precyzyjnej
Dlaczego badanie krwi w poszukiwaniu „odcisku palca” nowotworu ma znaczenie
Nowotwór często określa się jako chorobę DNA, jednak każdy guz jest genetycznie inny i może zmieniać się w czasie. Utrudnia to lekarzom wybór właściwego leczenia oraz rozpoznanie, kiedy nowotwór nawraca lub staje się oporny na leki. Ten artykuł opisuje obiecujące podejście łączące proste badanie krwi, zwane biopsją płynną, z szczegółowymi wzorcami uszkodzeń DNA znanymi jako sygnatury mutacyjne. Razem mogą pozwolić lekarzom śledzić zachowanie guza w trakcie choroby pacjenta i dopasowywać terapie precyzyjniej niż kiedykolwiek wcześniej. 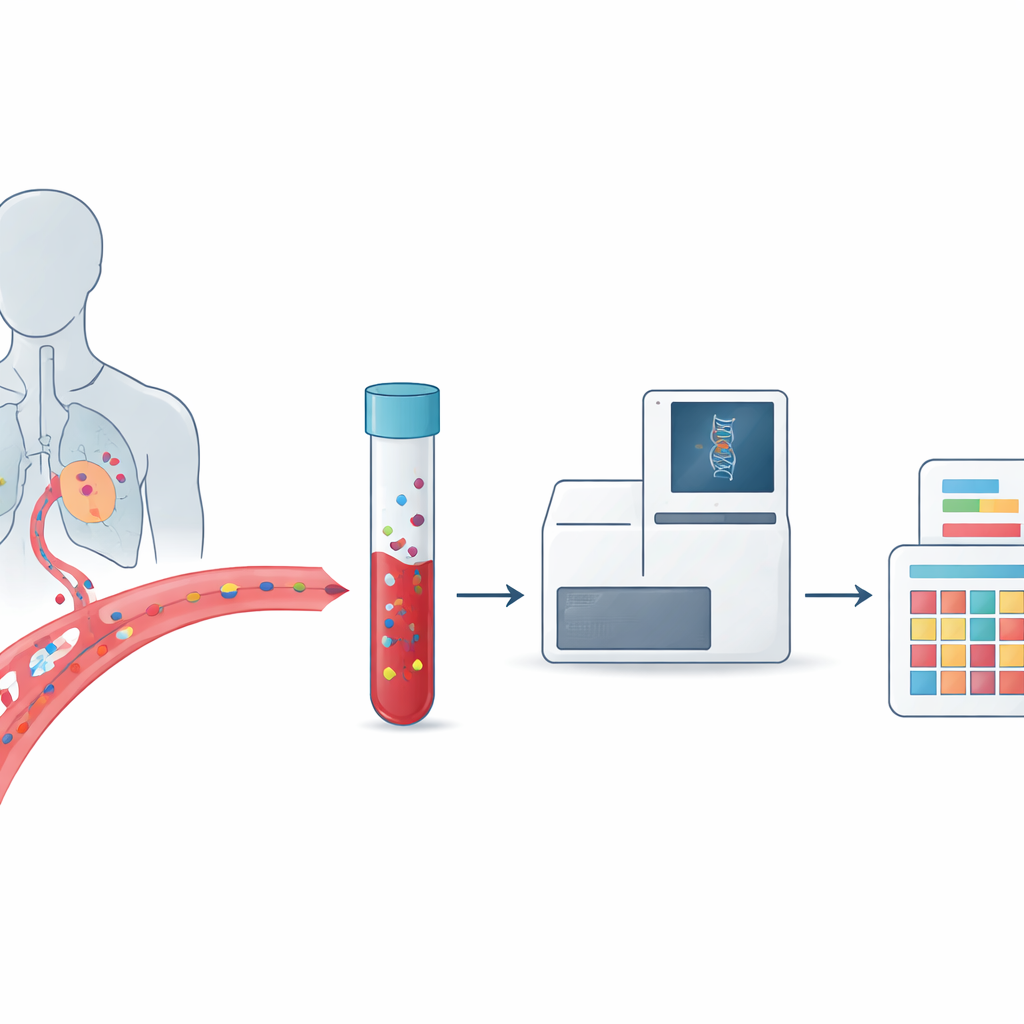
Szukając śladów nowotworu w próbce krwi
Tradycyjne biopsje nowotworowe wymagają pobrania fragmentu tkanki guza podczas zabiegu lub igłą, co może być bolesne, ryzykowne i trudne do powtórzenia. Biopsja płynna podchodzi do zagadnienia inaczej: poszukuje śladów nowotworu, które guzy uwalniają do krwiobiegu i innych płynów ustrojowych. Do tych śladów należą całe komórki nowotworowe oraz krótkie fragmenty DNA uwolnione przy obumieraniu komórek nowotworowych. Ponieważ próbki krwi można pobierać regularnie i obejmują materiał z wielu miejsc guza, biopsja płynna daje ruchomy obraz tego, jak nowotwór rośnie, się rozprzestrzenia i reaguje na terapię, zamiast pojedynczego zdjęcia w czasie.
Od pojedynczych mutacji do ogólnych wzorców uszkodzeń
Większość obecnych testów z biopsji płynnej koncentruje się na wykrywaniu konkretnych mutacji w krótkiej liście genów, które wskazują na możliwość zastosowania leków celowanych. Jednak nie wszystkie guzy noszą takie „leczone” zmiany, a nowotwory z wieloma różnymi mutacjami łatwo uchodzą poza zakres stałych paneli genowych. W ciągu ostatniej dekady potężne narzędzia sekwencjonowania DNA ujawniły, że mutacje w genomie nowotworu nie są losowe: tworzą rozpoznawalne wzorce kształtowane przez czynniki takie jak dym tytoniowy, promieniowanie ultrafioletowe, uszkodzenia naprawy DNA czy sama chemioterapia. Te powtarzające się wzorce, zwane sygnaturami mutacyjnymi, działają jak odciski palca procesów, które uszkadzały DNA w ciągu życia guza.
Czytanie historii i słabości guza
Sygnatury mutacyjne mogą ujawnić, gdzie nowotwór mógł się zacząć i które wewnętrzne systemy naprawcze są uszkodzone. Na przykład raki płuca u palaczy często wykazują wzorzec związany z ekspozycją na dym tytoniowy, podczas gdy niektóre raki jelita grubego niosą sygnatury niewydolności naprawy błędów parowania (mismatch repair), defektu, który sprawia też, że są wysoce wrażliwe na niektóre immunoterapie. Inne sygnatury wskazują na problemy w szlaku naprawy DNA zwanym rekombinacją homologiczna, co może uczynić guzy szczególnie podatnymi na leki platynowe i inhibitory PARP. Badania eksperymentalne na komórkach i modelach zwierzęcych potwierdziły, że wiele chemikaliów środowiskowych i terapii przeciwnowotworowych pozostawia charakterystyczne ślady mutacyjne odpowiadające tym obserwowanym u pacjentów, wzmacniając związek między sygnaturą a przyczyną. 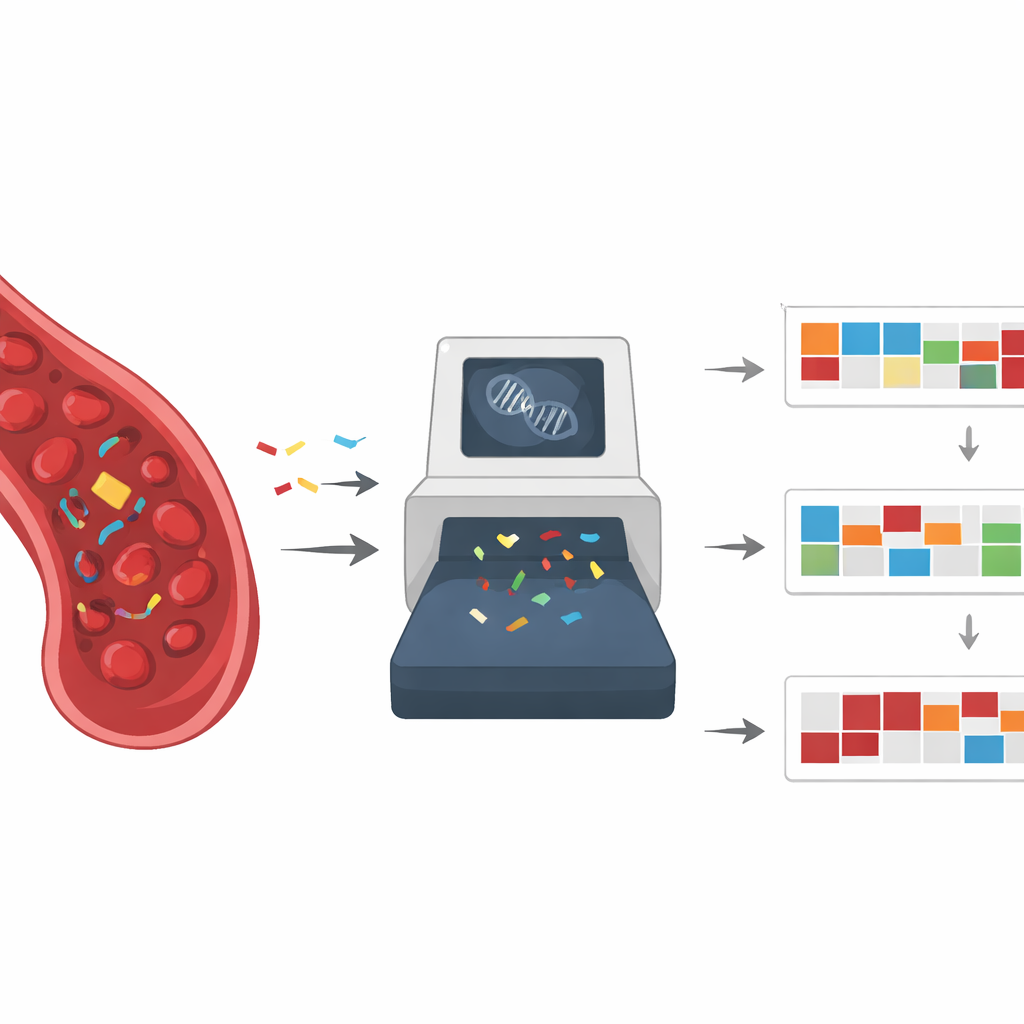
Połączenie monitorowania z krwi z „odciskiem palca” DNA
Kluczową ideą artykułu jest scalenie biopsji płynnej z sygnaturami mutacyjnymi w jedną ramę postępowania. Dzięki szerokiemu, obejmującemu cały genom sekwencjonowaniu fragmentów DNA guza we krwi, lekarze mogliby jednocześnie identyfikować pojedyncze mutacje i ogólne wzorce uszkodzeń, które je wywołały. Mogłoby to poprawić wczesne wykrywanie nowotworów, pomóc ustalić tkankę pochodzenia w trudnych przypadkach i dopracować wybór terapii, nawet gdy klasyczne mutacje napędowe są nieobecne. Powtarzane pobrania krwi przez miesiące lub lata mogłyby ujawnić, kiedy guz przełącza się na nowy proces mutacyjny, na przykład wywołany ciągłą ekspozycją na lek, co sygnalizowałoby narastającą oporność lub ryzyko drugiego nowotworu związanego z terapią.
Przeszkody na drodze do codziennego stosowania
Mimo obietnic, podejście to napotyka praktyczne wyzwania. Niektóre guzy uwalniają do krwi bardzo mało DNA, co utrudnia wykrycie sygnałów. Wiele znanych sygnatur wciąż nie ma jasnego wyjaśnienia biologicznego, a część wzorców może być częściowo kształtowana przez techniczne specyfiki różnych platform sekwencjonowania. Zmiany związane z wiekiem w komórkach tworzących krew mogą wprowadzać własne mutacje do DNA krążącego we krwi, dodatkowo zacierając obraz. Obecne metody wyodrębniania sygnatur z osocza często opierają się na złożonych narzędziach uczenia maszynowego, które wymagają dużych zbiorów treningowych i były w większości testowane w badaniach retrospektywnych, a nie w prospektywnych badaniach klinicznych.
Co to może oznaczać dla przyszłej opieki nad chorymi na raka
Autorzy dochodzą do wniosku, że integracja biopsji płynnej z sygnaturami mutacyjnymi mogłaby ostatecznie przekształcić opiekę onkologiczną z serii jednorazowych decyzji w proces stale aktualizowany. Zamiast polegać wyłącznie na biopsji tkankowej wykonanej przy rozpoznaniu, klinicyści mogliby w przyszłości używać rutynowych badań krwi do śledzenia ewoluującego „pisma” uszkodzeń DNA w guzie pacjenta. Mogłoby to zaostrzyć metody przesiewowe, poprawić diagnostykę, ukierunkować wybór i sekwencjonowanie terapii oraz wykrywać oporność zanim stanie się widoczna w badaniach obrazowych. Realizacja tej wizji będzie wymagać ustandaryzowanych metod, rygorystycznej walidacji i inteligentniejszych modeli komputerowych, lecz koncepcja wskazuje drogę ku przyszłości, w której leczenie nowotworu nie opiera się tylko na aktualnych mutacjach guza, lecz także na siłach, które je stworzyły.
Cytowanie: Carrasco, R., Dreij, K. Integrating liquid biopsy and mutational signatures to advance precision oncology. npj Precis. Onc. 10, 114 (2026). https://doi.org/10.1038/s41698-026-01337-w
Słowa kluczowe: biopsja płynna, sygnatury mutacyjne, wolne DNA, onkologia precyzyjna, ewolucja nowotworu