Clear Sky Science · pl
Predykcja niedoboru homologicznej rekombinacji i odpowiedzi na leczenie przy użyciu modelu bazowego opartego na tomografii komputerowej: badanie przedkliniczne
Dlaczego to ma znaczenie dla pacjentów i lekarzy
Leczenia nowotworów, które uszkadzają DNA — takie jak niektóre chemioterapie i nowe leki ukierunkowane — mogą działać niezwykle skutecznie w guzach, których systemy naprawcze są już wadliwe. Problem polega na tym, by ustalić, które guzy kryją takie słabości, bez polegania na wielokrotnych, inwazyjnych biopsjach. W tym badaniu sprawdzono, czy rutynowe medyczne skany myszy, interpretowane przez zaawansowany model sztucznej inteligencji, mogą ujawnić podatność guza i przewidzieć, jak dobrze odpowie na nowy eksperymentalny lek.
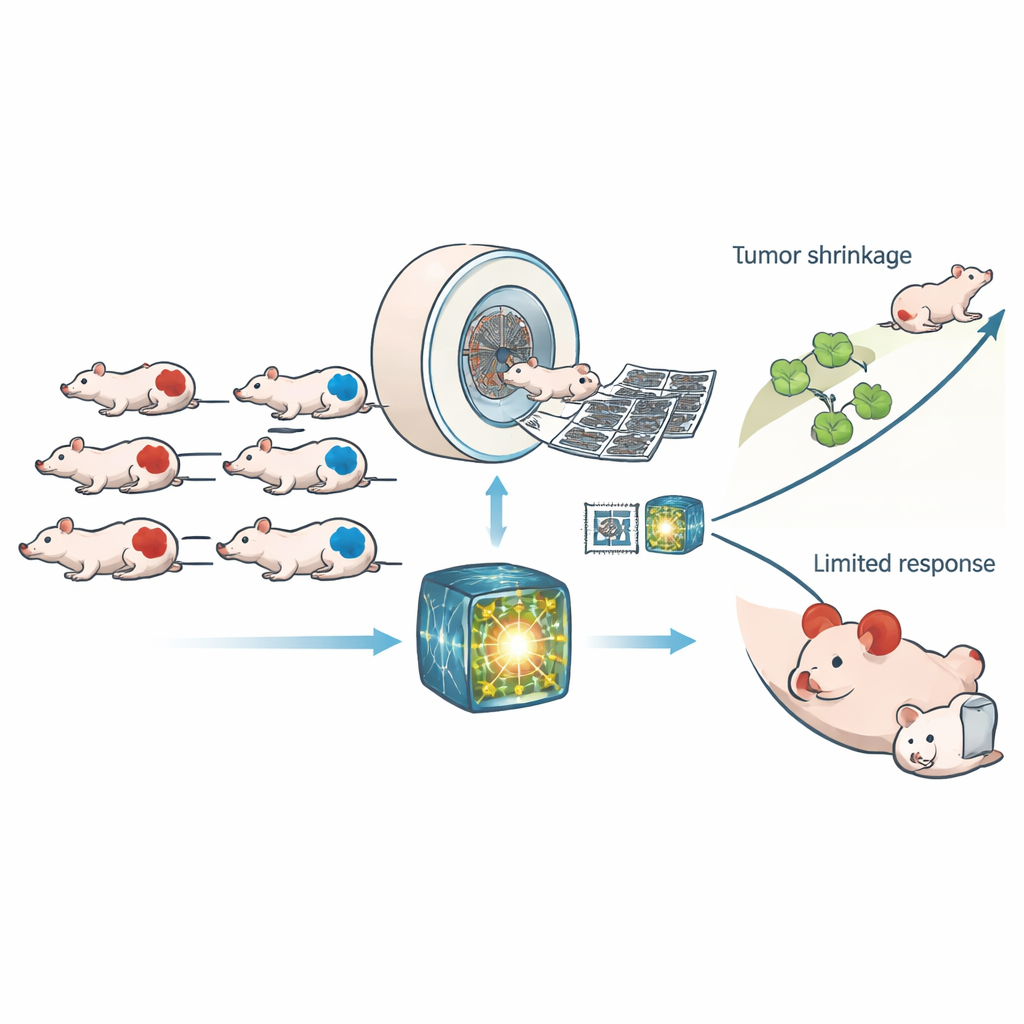
Ukryte słabe ogniwo w komórkach nowotworowych
Wiele guzów ma defekty w kluczowej ścieżce naprawy DNA zwanej homologiczną rekombinacją. Gdy ta ścieżka zawodzi, komórki gromadzą uszkodzenia materiału genetycznego — stan nazywany niedoborem homologicznej rekombinacji, czyli HRD. HRD sprzyja powstawaniu nowotworów, ale jednocześnie staje się piętą achillesową: leki dodatkowo uszkadzające DNA mogą doprowadzić te już obciążone komórki do śmierci skuteczniej niż komórki zdrowe. Obecnie identyfikacja HRD opiera się zwykle na badaniach genetycznych lub specjalistycznych testach laboratoryjnych, które są kosztowne, czasochłonne i często wymagają pobrania fragmentu guza. Autorzy zapytali, czy obrazowanie — ten sam rodzaj trójwymiarowych skanów rentgenowskich powszechnie stosowanych w klinikach — może zapewnić szybkie, nieinwazyjne okno na HRD.
Inteligentne skany zamiast kolejnych biopsji
Naukowcy pracowali z 307 myszami przenoszącymi ludzkie przeszczepy nowotworów, które były albo z HRD, albo miały prawidłową zdolność naprawczą. Wszystkie zwierzęta przeszły wysokorozdzielcze skany tomografii komputerowej (TK) przed i po otrzymaniu albo leczenia kontrolnego, albo CP-506 — eksperymentalnego leku aktywowanego w obszarach o niskim natlenieniu w guzie, powodującego usieciowanie nici DNA. Zamiast polegać na kilku ręcznie zaprojektowanych miarach obrazu, zespół użył nowoczesnego „modelu bazowego” wytrenowanego na dużych zestawach danych TK pochodzących od ludzi, aby wydobyć z każdego skanu tysiące subtelnych wzorców. Następnie prosty klasyfikator został wytrenowany na tych wzorcach, by zdecydować, czy guz ma HRD, a te same wyuczone cechy posłużyły do przewidywania, ile uszkodzeń DNA i opóźnienia wzrostu spowoduje CP-506.
Jak dobrze model obrazowy poradził sobie z zadaniem
Model bazowy wyraźnie przewyższył zarówno tradycyjną radiomikę, jak i standardową sieć głębokiego uczenia trenowaną od zera. Na nowych skanach testowych rozróżniał guzy HRD od nie-HRD z polem pod krzywą wynoszącym około 0,88 — poziom dokładności, który utrzymywał się przy różnych ustawieniach energii TK. Gdy obie metody AI zgadzały się co do typu guza, wydajność była jeszcze wyższa. Obrazowy wynik HRD wygenerowany przez model dobrze korelował z rzeczywistym stanem genetycznym w kilku liniach raka prostaty i jelita grubego, choć jedna linia o nietypowym zachowaniu naprawczym pozostała trudniejsza do skategoryzowania. Co ważne, cechy TK powiązane z HRD nie były jedynie artefaktami statystycznymi: przewidywały one również, ile trwałych uszkodzeń DNA wywołał CP-506 48 godzin po leczeniu oraz jak długo zajęło guzą odrośnięcie do czterokrotnej objętości w równoległym eksperymencie.
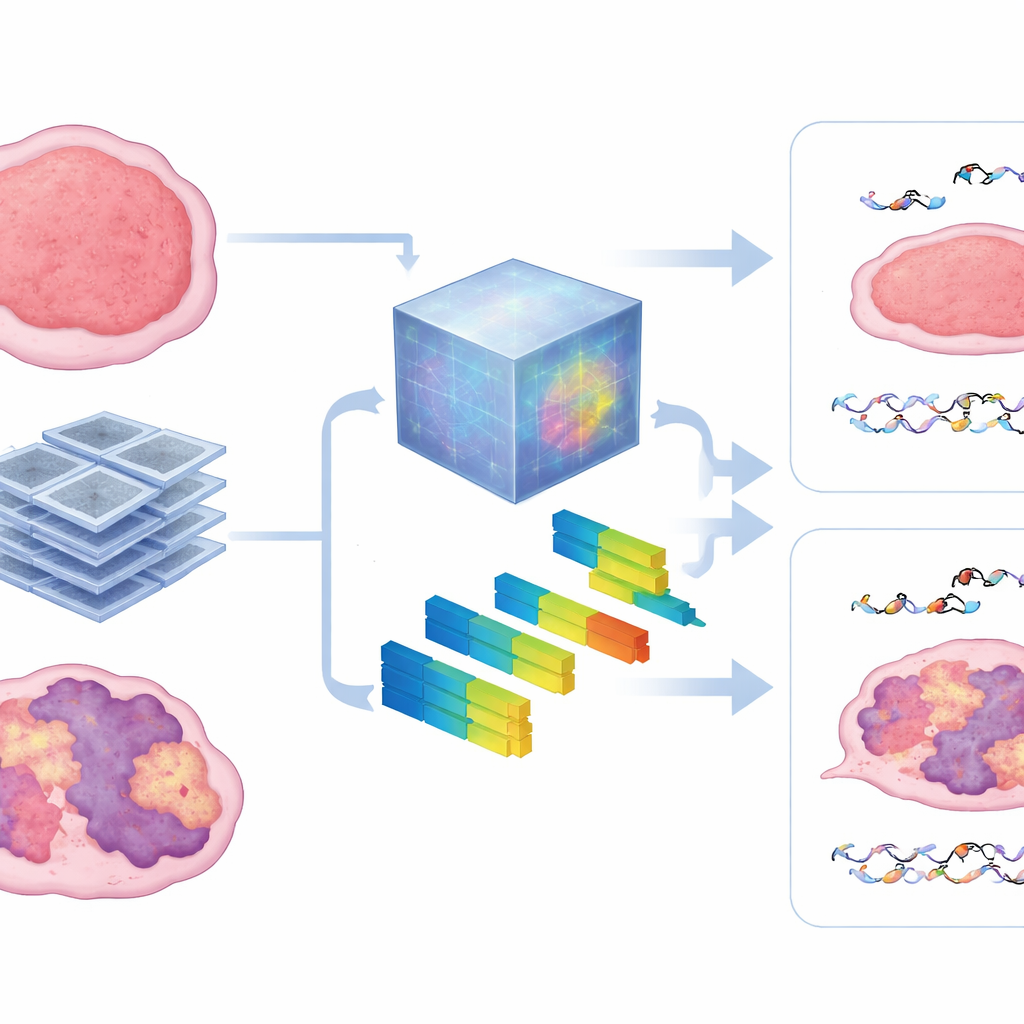
Co skany ujawniają wewnątrz guza
Aby zajrzeć do czarnej skrzynki, autorzy porównali wzorce wyuczone przez model bazowy ze standardowymi cechami radiomicznymi opisującymi teksturę i intensywność obrazu. Stwierdzili, że model w dużej mierze opierał się na miarach heterogeniczności — na tym, jak łatkowy, gruboziarnisty lub nieregularny wydawał się guz w TK. Guzy z mocniejszymi sygnałami HRD miały tendencję do bardziej zdezorganizowanych tekstur, a te same cechy pomagały prognozować zarówno mikroskopowe uszkodzenia DNA, jak i makroskopową kontrolę guza. Podejście pozostało odporne, gdy dostępnych było mniej danych treningowych, co sugeruje, że takie wstępnie wytrenowane modele mogą pokonać główną przeszkodę w badaniach na zwierzętach, gdzie zebranie dużych zbiorów obrazów jest trudne.
Z eksperymentów na myszach do przyszłej opieki nad pacjentami
To przedkliniczne badanie pokazuje, że pojedynczy skan TK, zinterpretowany przez potężne, wstępnie wytrenowane AI, może uchwycić sygnały wadliwej naprawy DNA i przewidzieć, jak silnie guz odpowie na lek uszkadzający DNA. Dla laika wniosek jest taki, że standardowo wyglądające skany wkrótce mogą pełnić podwójną funkcję — lokalizować guz i ujawniać jego kruchość — bez dodatkowych procedur. Zanim metoda stanie się częścią rutynowej opieki, musi zostać przetestowana i zwalidowana u pacjentów. Jeśli te wysiłki zakończą się sukcesem, odciski palców HRD oparte na TK i AI mogą pomóc lekarzom dokładniej dobierać pacjentów do terapii takich jak CP-506 i pokrewnych, poprawiając wyniki przy jednoczesnym oszczędzaniu niektórym pacjentom nieefektywnych, toksycznych leków.
Cytowanie: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
Słowa kluczowe: niedobór homologicznej rekombinacji, obrazowanie nowotworów, radiomika, modele bazowe, terapia uszkadzająca DNA