Clear Sky Science · pl
Opracowanie i walidacja modelu opartego na sztucznej inteligencji do rozpoznawania zmian przydatkowych: łagodnych, borderline i złośliwych
Dlaczego to ważne dla zdrowia kobiet
Zmiany w jajnikach i pozostałych przydatkach są częstym znaleziskiem w badaniu ultrasonograficznym miednicy, jednak rozróżnienie, które z nich są niegroźne, a które mogą świadczyć o wczesnym nowotworze, wciąż bywa trudne, nawet dla ekspertów. W badaniu przedstawiono nowy system sztucznej inteligencji (SI), nazwany Clinical‑OMTA, który analizuje obrazy ultradźwiękowe i pomaga lekarzom przyporządkować zmiany do trzech kluczowych kategorii — łagodnych, borderline i złośliwych — tak aby kobiety otrzymywały odpowiednie leczenie, unikając jednocześnie zbędnych operacji.
Trzy rodzaje zmian, trzy zupełnie różne decyzje
Nie wszystkie zmiany przydatkowe są takie same. Guzy łagodne często można obserwować lub usunąć prostym zabiegiem chirurgicznym. Guzy złośliwe to groźne nowotwory wymagające specjalistycznego leczenia chirurgicznego i chemioterapii. Guzy borderline mieszczą się gdzieś pośrodku: mogą nawracać, ale często dotyczą młodszych kobiet, które chcą zachować płodność, dlatego chirurdzy starają się usuwać jedynie to, co konieczne. Niestety w badaniu USG wszystkie trzy kategorie mogą wyglądać bardzo podobnie. Guzy borderline szczególnie łatwo udają zarówno niegroźne torbiele, jak i agresywne nowotwory, co utrudnia podejmowanie decyzji terapeutycznych i zwiększa stres pacjentek oraz klinicystów.
Przekształcanie złożonych skanów w jaśniejsze odpowiedzi
Ultrasonografia jest zazwyczaj pierwszym i najszerzej dostępnym badaniem przy zmianach przydatkowych, ale interpretacja ziarnistych, silnie zmiennych obrazów wymaga dużego doświadczenia. Istniejące systemy punktacji i kalkulatory ryzyka, takie jak szeroko stosowany model ADNEX, łączą określone cechy ultrasonograficzne z prostymi danymi klinicznymi, na przykład wiekiem i markerem krwi (CA125), jednak wciąż opierają się na obserwatorach opisujących obrazy. Ostatnie prace nad głębokim uczeniem — odgałęzieniem SI, które uczy się wzorców bezpośrednio z pikseli — dają szansę ograniczenia tej subiektywności poprzez szkolenie komputerów do rozpoznawania subtelnych sygnatur obrazowych różnych typów guzów.
Asystent SI szkolony w wielu szpitalach
W oparciu o wcześniejsze prace autorzy zaprojektowali Clinical‑OMTA, model SI o dwutorowej architekturze, który najpierw oddziela zmiany łagodne od niełagodnych, a następnie rozróżnia guzy borderline od złośliwych. System przetwarza obrazy ultrasonograficzne w skali szarości i może opcjonalnie przyjmować wiek oraz wartości CA125. Aby nauczyć i przetestować model, zespół zgromadził duży, zróżnicowany zbiór danych: 2381 kobiet z 23 szpitali w całych Chinach, badanych przy użyciu 38 modeli aparatów USG. Większość przypadków miała potwierdzenie histopatologiczne po operacji; mniejsza grupa jednoznacznie łagodnych torbieli była potwierdzona co najmniej sześciomiesięcznym monitorowaniem ultrasonograficznym. Dane podzielono na zestawy treningowe, wewnętrzne testowe oraz dwie całkowicie niezależne zewnętrzne kohorty testowe, obejmujące zarówno obrazy statyczne, jak i krótkie skany wideo jajników. 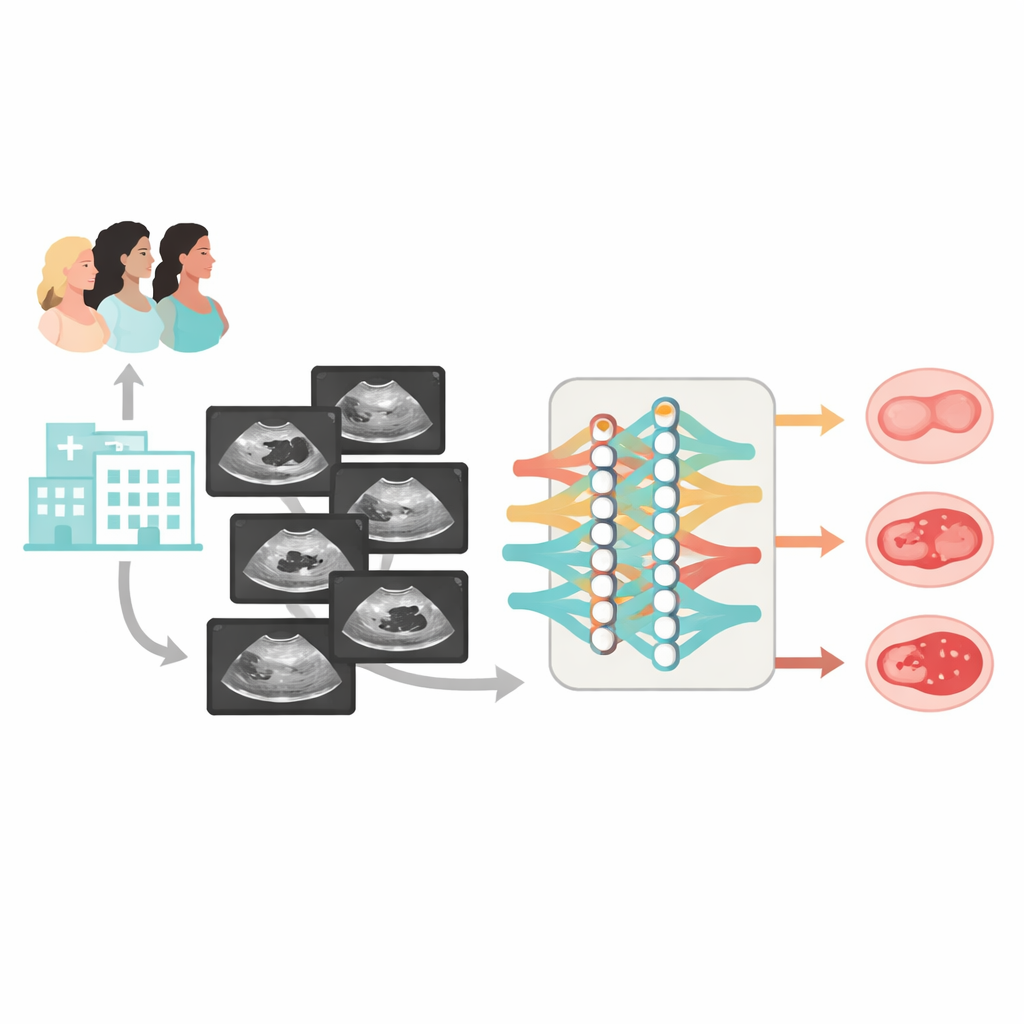
Jak SI sprawdziła się w warunkach rzeczywistych
W zewnętrznych testach obrazów Clinical‑OMTA prawidłowo odróżniała zmiany łagodne, borderline i złośliwe z dokładnością porównywalną zarówno do modelu ADNEX, jak i do oceny eksperta ultrasonografisty. Jej wydajność była stabilna niezależnie od marki aparatu USG, metody badania (przez brzuch czy przez pochwę) oraz w dwóch zewnętrznych szpitalach, co sugeruje, że model nie jest nadmiernie dopasowany do jednego konkretnego urządzenia lub ośrodka. System dobrze radził sobie także z klipami wideo, nie tylko ze statycznymi klatkami. Co ciekawe, dodanie wieku i wartości CA125 nie poprawiło decyzji w stosunku do użycia samych obrazów USG, potwierdzając wcześniejsze badania pokazujące, że ten marker krwi wnosi niewiele, gdy dostępne są obrazy wysokiej jakości. 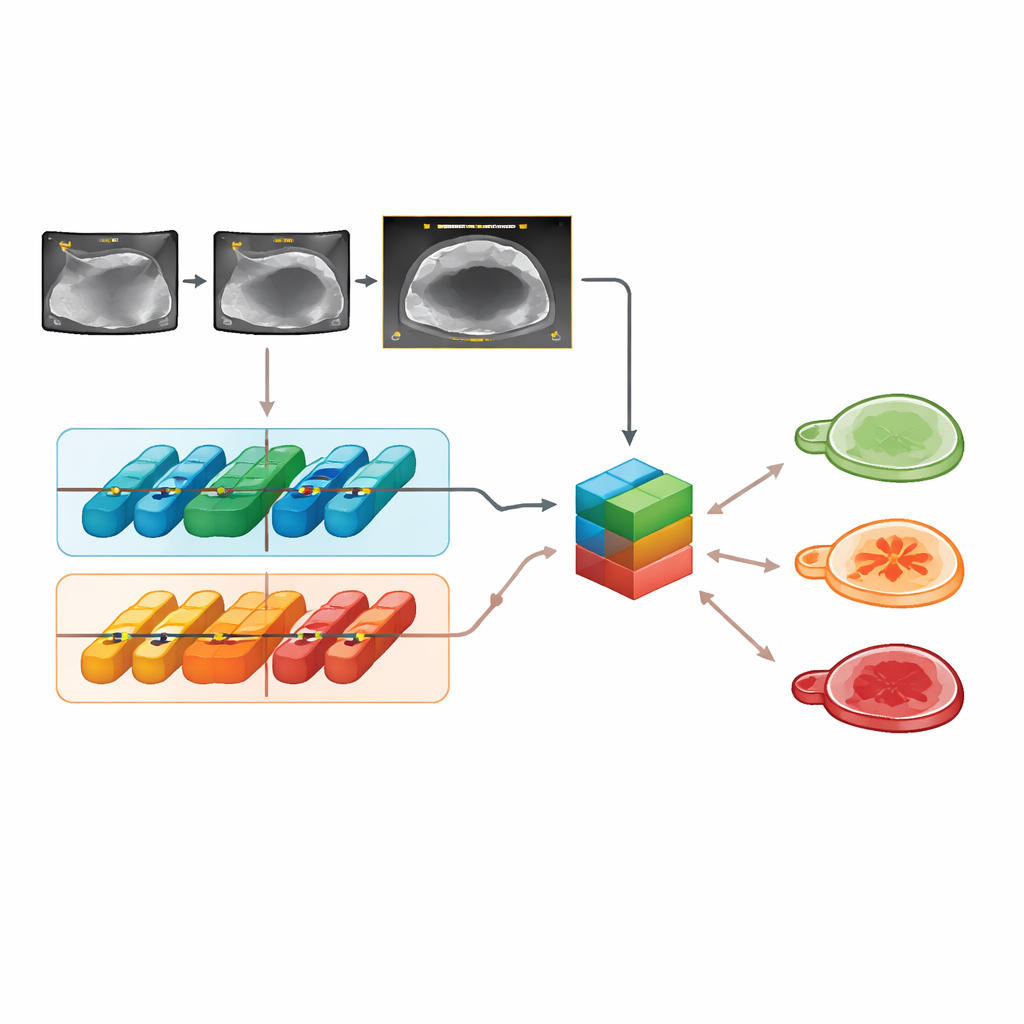
Wsparcie dla mniej doświadczonych lekarzy — i ograniczenia
Następnie badacze poprosili 11 radiologów — początkujących, średnio zaawansowanych i bardzo doświadczonych — aby sklasyfikowali te same przypadki najpierw samodzielnie, a potem z pomocą wyjścia SI i nakładek typu heat‑map, które podświetlają obszary obrazu uznane przez model za istotne. Dzięki wsparciu Clinical‑OMTA dokładność młodszych lekarzy wzrosła o około 18–20 punktów procentowych, a czytający o średnim doświadczeniu również znacząco się poprawili, osiągając poziom bliski ekspertom. Zgodność między oceniającymi, wcześniej tylko umiarkowana lub słaba, wzrosła do bardzo wysokiego poziomu przy użyciu narzędzia. Jednocześnie autorzy zauważają, że tak silna zgodność może odzwierciedlać „błąd automatyzacji” (automation bias), gdy klinicyści nadmiernie polegają na SI, szczególnie w najbardziej niejednoznacznych przypadkach borderline. Dlatego podkreślają, że mapy cieplne są narzędziami badawczymi, a nie samodzielnymi wyjaśnieniami, i że wskazówki SI należy ostrożnie integrować w szkoleniu klinicznym oraz procesie podejmowania decyzji.
Co to oznacza dla pacjentek
Podsumowując, Clinical‑OMTA pokazuje, że system SI szkolony na zróżnicowanych danych ultrasonograficznych może dorównywać ekspertom w klasyfikacji zmian przydatkowych na łagodne, borderline i złośliwe, jednocześnie znacząco podnosząc umiejętności i spójność mniej doświadczonych radiologów. Ponieważ działa na różnych aparatach i w różnych ośrodkach, model mógłby w przyszłości zostać wbudowany w skanery lub używany jako samodzielne oprogramowanie wspierające lekarzy w przeciążonych lub słabiej wyposażonych placówkach. Autorzy zastrzegają, że przed rutynowym zastosowaniem potrzebne są dalsze badania prospektywne i międzynarodowe, szczególnie w środowiskach z niższej klasy sprzętem lub operatorami niebędącymi specjalistami. Mimo to praca ta wskazuje na przyszłość, w której więcej kobiet, niezależnie od miejsca leczenia, może skorzystać z interpretacji obrazów ultrasonograficznych jajników na poziomie eksperckim i bardziej dopasowanej, terminowej opieki.
Cytowanie: Wu, Y., Dai, W., Li, X. et al. Development and validation of an artificial intelligence-based model for diagnosing benign, borderline, and malignant adnexal masses. npj Precis. Onc. 10, 106 (2026). https://doi.org/10.1038/s41698-026-01320-5
Słowa kluczowe: ultrasonografia jajników, sztuczna inteligencja, zmiany przydatkowe, guzy jajnika o granicznej złośliwości, wsparcie decyzji klinicznych