Clear Sky Science · pl
DDX41 ułatwia ucieczkę immunologiczną zależną od PD-L1 w OSCC poprzez tworzenie faz i aktywację szlaku STING
Dlaczego to badanie ma znaczenie
Rak jamy ustnej jest powszechny i często śmiertelny, częściowo dlatego, że guzy uczą się ukrywać przed mechanizmami obronnymi organizmu. To badanie ujawnia wcześniej nieznany sposób, w jaki płaskonabłonkowy rak jamy ustnej (OSCC) chroni się przed atakiem układu odpornościowego. Praca koncentruje się na molekule zwanej DDX41 i pokazuje, jak pomaga komórkom nowotworowym włączać inny białko, PD-L1, które skutecznie nakazuje komórkom odpornościowym wycofać się. Zrozumienie tej ukrytej komunikacji między komórkami nowotworowymi a układem odpornościowym może otworzyć nowe drogi do lepszych diagnoz i terapii.
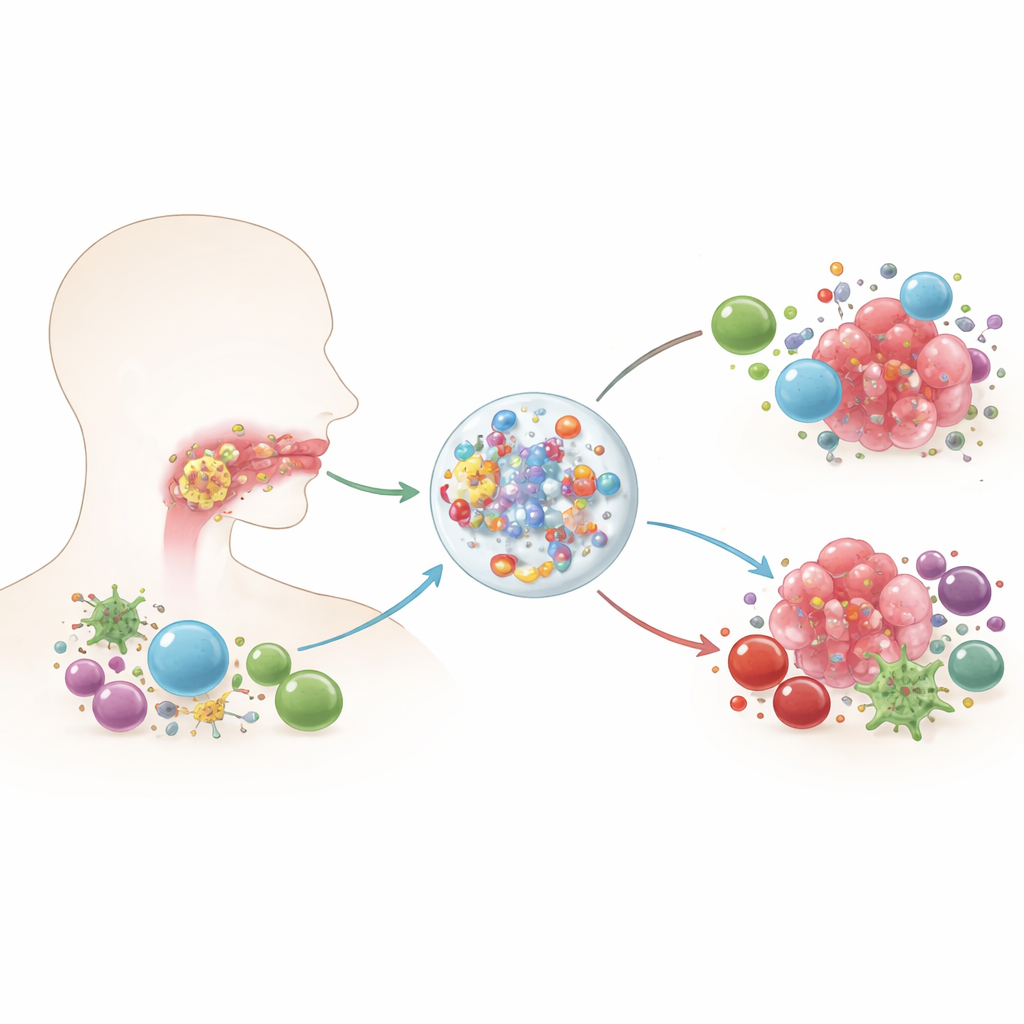
Problemowe białko w guzach jamy ustnej
Naukowcy najpierw postawili podstawowe pytanie: czy DDX41 jest nadmiernie aktywne w raku? Przeglądając duże publiczne bazy danych dotyczące nowotworów, odkryli, że wiele typów guzów, w tym nowotwory głowy i szyi, wykazuje wyższe poziomy DDX41 niż tkanki normalne. Skupiając się na OSCC, zaobserwowali podobny wzorzec: próbki guzów od pacjentów wykazywały wyraźnie podwyższony poziom DDX41 w porównaniu z pobliską zdrową tkanką jamy ustnej. Pacjenci, których guzy miały więcej DDX41, zwykle mieli gorsze rokowania w czasie, co sugeruje, że to białko wiąże się z agresywnym przebiegiem choroby i niższym przeżyciem. Testy mierzące DDX41 wykazały też potencjał w rozróżnianiu tkanki nowotworowej od nienowotworowej jamy ustnej.
Jak DDX41 wspiera wzrost i rozsiew guza
Aby wyjść poza korelacje, zespół manipulował poziomami DDX41 w hodowanych w laboratorium komórkach OSCC. Gdy obniżono DDX41, komórki nowotworowe dzieliły się wolniej, zmieniały kształt i miały mniejszą zdolność migracji oraz inwazji przez sztuczne bariery — zachowania odzwierciedlające zmniejszoną zdolność do rozprzestrzeniania się. Podniesienie poziomu DDX41 wywoływało efekt odwrotny, przyspieszając wzrost i ruchliwość. U myszy wszczepionych komórkami OSCC pozbawionymi DDX41 guzy rosły mniejsze i wolniejsze, mimo że zwierzęta pozostawały ogólnie zdrowe. Razem te eksperymenty wskazują, że DDX41 nie jest tylko biernym obserwatorem, lecz aktywnym czynnikiem napędzającym progresję guza.
Ukryty przełącznik ucieczki przed układem odpornościowym
Badanie następnie sprawdziło, jak DDX41 zmienia relację guza z układem odpornościowym. Przy użyciu profilowania genowego i pomiarów białek autorzy wykazali, że DDX41 aktywuje łańcuch sygnalizacyjny znany jako szlak STING–TBK1–NF-κB wewnątrz komórek nowotworowych. Ten szlak ostatecznie zwiększa produkcję PD-L1, molekuły na powierzchni komórek nowotworowych, która wiąże się z receptorami na limfocytach T i osłabia ich zdolność do zabijania. Gdy poziomy DDX41 zostały obniżone, kluczowe białka sygnalizacyjne i PD-L1 spadły, a hodowane in vitro limfocyty T stały się bardziej aktywne i skuteczniejsze w atakowaniu komórek nowotworowych. W guzach mysich wyłączenie DDX41 zmniejszyło PD-L1, zwiększyło liczbę i aktywność zwalczających nowotwór limfocytów CD8⁺ oraz zmniejszyło odsetek supresyjnych komórek odpornościowych znanych jako mieloidalne komórki supresorowe.
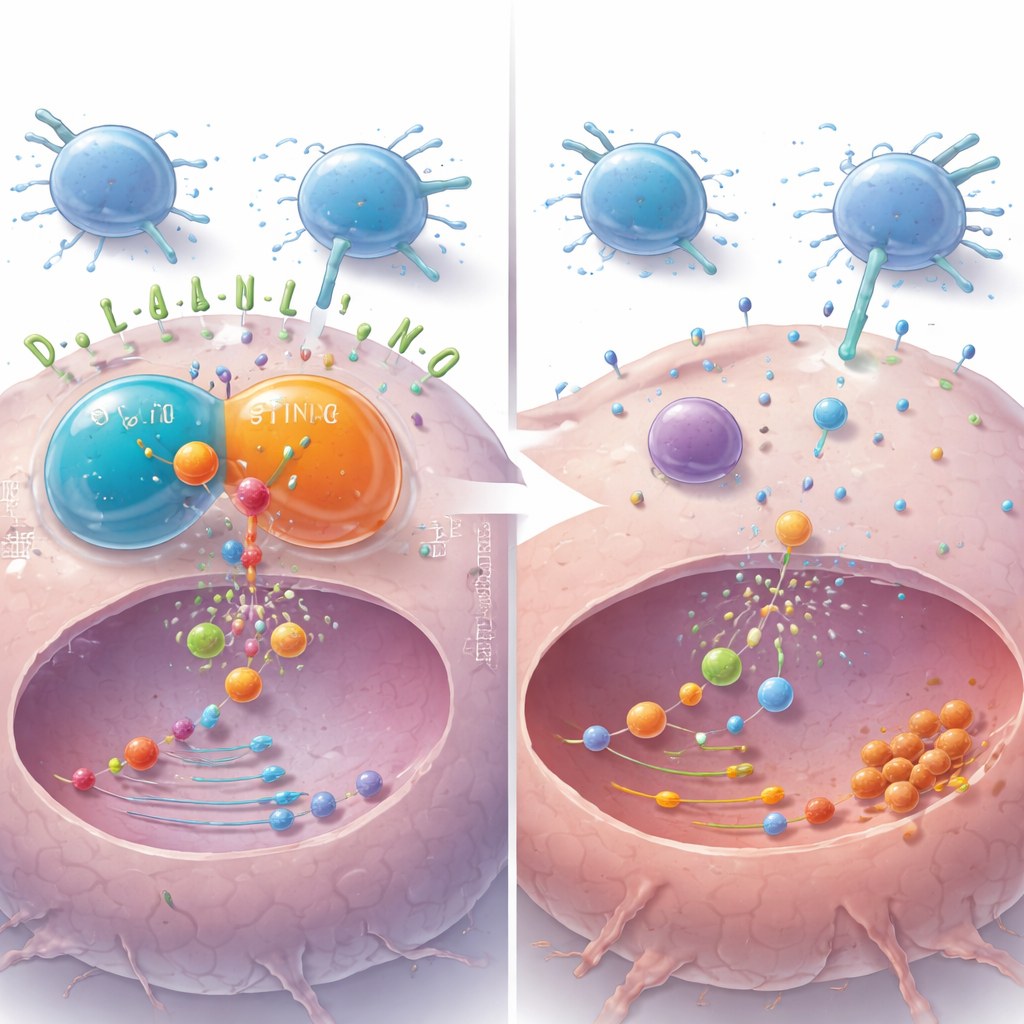
Krople guza, które przeprogramowują sygnały
Uderzającym elementem tej pracy jest odkrycie, że DDX41 działa poprzez maleńkie, przypominające ciecz krople wewnątrz komórek. Zaobserwowano, że białko tworzy mikroskopijne, kuliste kondensaty zachowujące się jak krople, łączące się i wymieniające materiały. DDX41 fizycznie kojarzył się z innym białkiem, STING, i razem tworzyły wspólne krople w płynnym wnętrzu komórki. Gdy badacze wprowadzili do komórek nowotworowych fragmenty DNA — naśladując nieprawidłowe DNA, które może pojawić się w raku — te krople nasiliły się, a sygnalizacja wzdłuż szlaku STING–TBK1–NF-κB zwiększyła się, co ostatecznie podwyższyło poziom PD-L1. Chemikalia zaburzające takie krople lub blokujące elementy szlaku osłabiały ten efekt, podkreślając, że stan kropli pomaga organizować i wzmacniać sygnały sprzyjające ucieczce przed układem odpornościowym.
Co to oznacza dla pacjentów
W próbkach guzów od osób z OSCC wysoki poziom DDX41 szedł w parze z bardziej aktywnymi białkami sygnalizacyjnymi, wyższym PD-L1, większą liczbą supresyjnych komórek odpornościowych i mniejszą liczbą pomocnych limfocytów CD8⁺. To tworzy spójny obraz: DDX41 rozpoznaje nieprawidłowe DNA w komórkach nowotworowych, tworzy z STING krople, które wzmacniają kaskadę sygnałową, a przez to zwiększają PD-L1, wyciszając atak układu odpornościowego. Dla pacjentów te wyniki sugerują, że DDX41 może służyć zarówno jako marker bardziej niebezpiecznych raków jamy ustnej, jak i potencjalny nowy cel terapeutyczny. Terapie blokujące DDX41 lub jego oparte na kroplach partnerstwo ze STING mogłyby obniżyć PD-L1, ożywić limfocyty T i zwiększyć skuteczność istniejących immunoterapii.
Cytowanie: Tian, Z., Cui, H., Sun, S. et al. DDX41 facilitates PD-L1-mediated immune escape in OSCC via the phase separation and activation STING pathway. npj Precis. Onc. 10, 126 (2026). https://doi.org/10.1038/s41698-026-01308-1
Słowa kluczowe: płaskonabłonkowy rak jamy ustnej, ucieczka nowotworu przed układem odpornościowym, PD-L1, szlak STING, DDX41