Clear Sky Science · pl
Analiza pojedynczych komórek na dużą skalę i perturbacje in silico ujawniają dynamiczną ewolucję HCC: od inicjacji do ukierunkowania terapeutycznego
Dlaczego wewnętrzne życie raka wątroby ma znaczenie
Rak wątrobowokomórkowy, najczęstsza postać nowotworu wątroby, jest wyjątkowo trudny w leczeniu. Wielu pacjentów słabo reaguje na dostępne leki, a guzy często nawracają lub dają przerzuty. Jednym z głównych powodów jest to, że każdy guz to chaotyczna mieszanka różnych komórek, które zmieniają się w czasie i nieustannie komunikują się z otoczeniem. W tym badaniu zastosowano zaawansowane metody odczytu genów w skali pojedynczych komórek i przestrzenną transkryptomikę, aby obserwować tę ewolucję komórka po komórce — od wczesnego wzrostu guza po zaawansowaną, oporną na leczenie postać — i wskazać słabe punkty, które mogą wykorzystać nowe terapie.
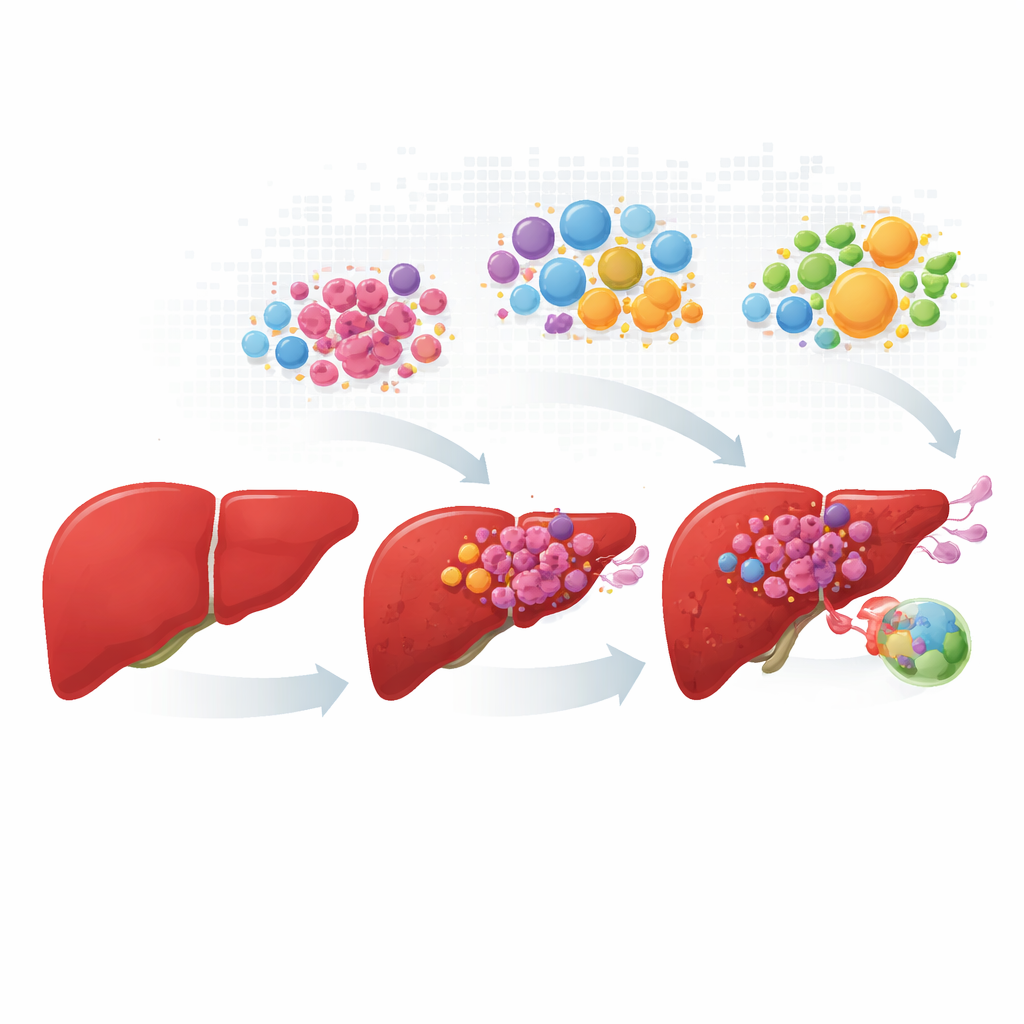
Śledzenie komórek nowotworowych od wczesnych zmian do rozprzestrzeniania
Naukowcy zebrali i zharmonizowali dane od ponad stu pacjentów, obejmujące prawidłową wątrobę, guzy pierwotne, zmiany w naczyniach krwionośnych oraz przerzuty do węzłów chłonnych. Zamiast traktować każdy guz jako jednorodną masę, profilowali setki tysięcy poszczególnych komórek, a następnie mapowali ich położenie w rzeczywistych skrawkach tkanki. Komórki nowotworowe wątroby rozdzieliły się na cztery powtarzające się „osobowości”. Jedna grupa zachowywała wiele normalnych funkcji wątroby i zadań metabolicznych; pozostałe trzy wykazywały wzrost napędzany stresem, wysoką aktywność szlaku wzrostowego MYC lub zachowania inwazyjne powiązane z zapaleniem. Te cztery stany pojawiały się w różnych proporcjach wraz z postępem choroby, a szybko proliferujące i inwazyjne komórki dominowały w zmianach naczyniowych i w przerzutach do węzłów chłonnych.
Cztery „osobowości” guza o różnych perspektywach
Te cztery stany komórek nowotworowych to nie były tylko kategorie teoretyczne — korelowały z przebiegiem choroby u pacjentów. Guzy bogate w stan przypominający wątrobę, o wysokiej aktywności metabolicznej, wiązały się z lepszym przeżyciem, podczas gdy guzy zdominowane przez pozostałe trzy, agresywne stany miały gorsze rokowania. Nawet „dobry” stan miał jednak drugie dno: był silnie wzbogacony u pacjentów, którzy nie odnosili korzyści z leku sorafenib, prawdopodobnie dlatego, że komórki te zachowują mechanizmy detoksykacji zdolne do inaktywacji leków. Odtwarzając trajektorie rozwojowe komórek, zespół pokazał, że komórki inwazyjne i zapalne mogą rozgałęziać się w kierunku bardziej zróżnicowanych lub bardziej proliferacyjnych stanów, co sugeruje, że komórki guza potrafią zmieniać tożsamość i potencjalnie unikać terapii ukierunkowanych na pojedynczy stan.
Obsada wspierająca: współwinni immunologiczni i zrębowi
Komórki nowotworowe nie działają samotnie. Badanie ujawniło wyspecjalizowane komórki odpornościowe i komórki podporowe, które albo walczą z guzem, albo potajemnie mu pomagają. Wśród makrofagów — komórek pełniących funkcję sprzątaczy i wartowników tkanki — niektóre typy produkowały sygnały zapalne wspierające odpowiedź przeciwnowotworową, podczas gdy inne były metabolicznie przeprogramowane, tłumiły pomocne sygnały i promowały powstawanie naczyń oraz inwazję. Te „szkodliwe” makrofagi rozszerzały się w próbkach zaawansowanych zmian. Podobnie niektóre typy komórek śródbłonka wyścielających naczynia oraz fibroblastów tworzących tkankę łączną utworzyły odrębne podzbiory powiązane z gorszym rokowaniem. W chorobie zaawansowanej specyficzny podtyp śródbłonka i dwa typy fibroblastów tworzyły silnie powiązane centra, które przebudowywały zewnątrzkomórkowy ruszt, napędzały neowaskularyzację i korelowały z najbardziej agresywnymi stanami komórek nowotworowych.
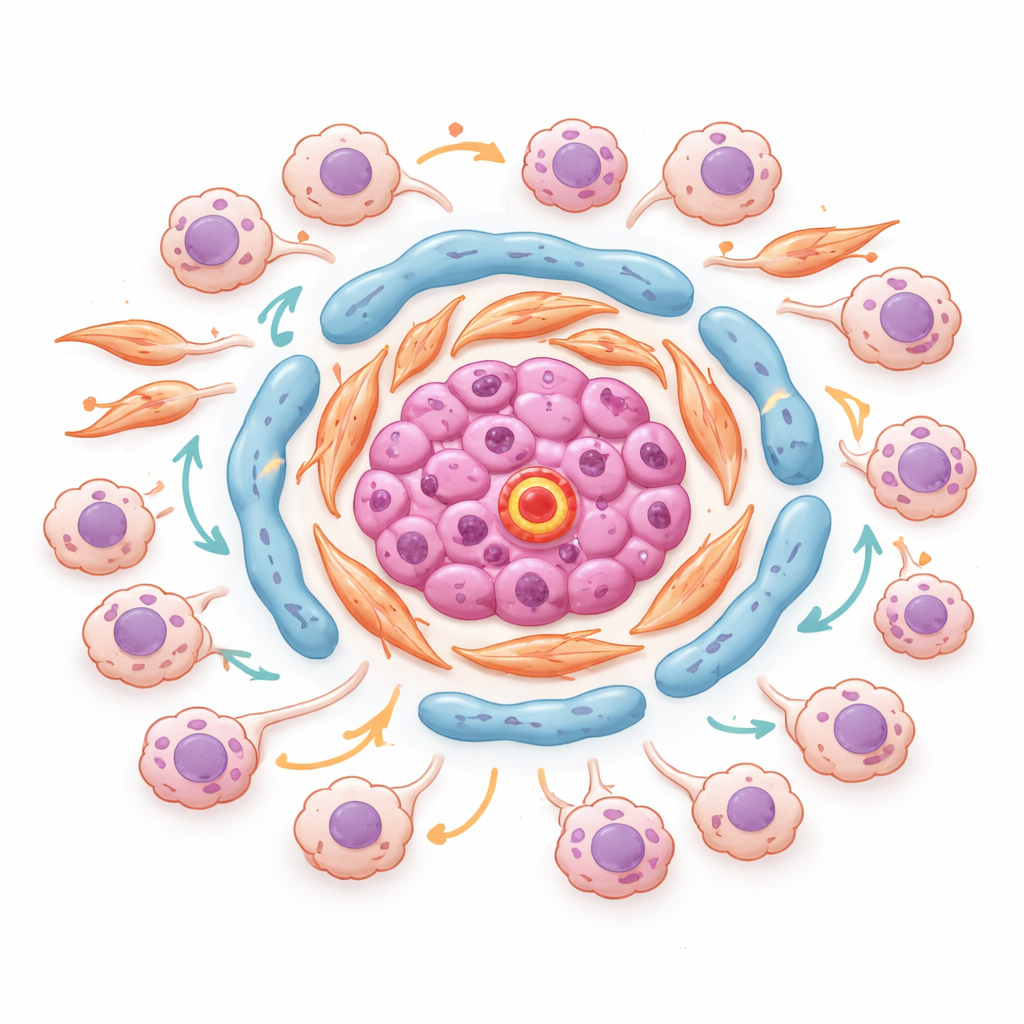
Odnajdywanie niebezpiecznych sąsiedztw w obrębie guza
Dzięki transkryptomice przestrzennej, która mierzy aktywność genów nie tracąc mapy położenia każdego punktu w tkance, autorzy zidentyfikowali zorganizowane „sąsiedztwa” wewnątrz guzów. W jednym reprezentatywnym guzie komórki śródbłonka bogate w cząsteczkę zwaną ESM1 skupiały się z fibroblastami łaknącymi lipidów i produkującymi macierz w centrum wysp zrębowych. Wokół tych rdzeni kumulowały się komórki nowotworowe napędzane stresem i inwazyjne, w regionach o silnych sygnałach TGF‑beta i niskim natlenieniu. Kluczowe czynniki transkrypcyjne kontrolujące odpowiedź komórek na stres i zapalenie były wspólne dla tych stanów nowotworowych i najbardziej aktywne dokładnie tam, gdzie komórki guza stykały się z tymi zrębowymi centrami. To sugeruje, że specyficzne mikro‑niche na granicach guz–zrąb aktywnie sprzyjają zmianie stanu komórek nowotworowych, nasilają agresję i oporność na leczenie.
Znajdowanie wspólnego słabego punktu dla nowych terapii
Aby przejść od opisu do interwencji, zespół użył modelu uczenia maszynowego wytrenowanego na milionach komórek, aby symulować „wirtualne wyłączenia” genów i przewidzieć, które zmiany mogą skierować szkodliwe komórki z powrotem ku zdrowszym stanom. Porównując makrofagi, komórki śródbłonka i komórki nowotworowe, znaleźli niewielki zestaw genów, których usunięcie pomagało normalizować wszystkie trzy typy. Wśród nich wyróżniał się HSP90B1: linie komórkowe nowotworowe silnie od niego zależą, jest on nadprodukcjonowany w guzach wątroby, zwłaszcza w tych opornych na leki ukierunkowane i immunoterapię, a jego wysokie poziomy prognostycznie wiążą się z gorszym przeżyciem. HSP90B1 koduje chaperonę zajmującą się radzeniem sobie ze stresem w fabryce fałdowania białek komórki, wspierając wiele receptorów powierzchniowych i szlaków sygnałowych. Ponieważ selektywne leki przeciwko tej chaperonie już istnieją i mogą również modyfikować środowisko immunologiczne, badanie proponuje HSP90B1 jako obiecujący cel do pokonania oporności, szczególnie w połączeniu z obecnymi terapiami raka wątroby.
Co to oznacza dla pacjentów i terapii
Podsumowując, praca ta pokazuje, że rak wątroby to nie pojedyncza choroba, lecz dynamiczne ekosystemy stanów komórkowych i nisz, które przesuwają się wraz z wzrostem i rozprzestrzenianiem guza. Łącząc konkretne „osobowości” komórek nowotworowych, komórki wspierające i przestrzenne sąsiedztwa z wynikami pacjentów i odpowiedzią na leki, badanie oferuje mapę drogową do precyzyjniejszego leczenia: dobierania terapii do dominujących stanów komórkowych, zakłócania zrębowych centrów sprzyjających agresji oraz celowania w wspólne zależności, takie jak HSP90B1, od których zależy wiele komórek guza i mikrośrodowiska. Choć konieczne są dalsze badania laboratoryjne i kliniczne, atlas stworzony przez zespół dostarcza szczegółowego planu, jak przemienić wewnętrzną złożoność guza z przeszkody w szansę na mądrzejsze i trwalsze terapie raka wątroby.
Cytowanie: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Słowa kluczowe: rak wątrobowokomórkowy, analiza pojedynczych komórek, mikrośrodowisko guza, transkryptomika przestrzenna, HSP90B1