Clear Sky Science · pl
Platforma wirtualnego przesiewu napędzana przez AI identyfikuje nowe kandydaty na inhibitory NSUN2 do terapii ukierunkowanej przeciw rakowi: komputerowe podejście do odkrywania leków
Nowe sposoby przechytrzenia opornych nowotworów
Wiele nowotworów staje się śmiertelnych nie tylko dlatego, że się pojawiają, lecz także dlatego, że uczą się unikać naszych najlepszych leków. W tym badaniu zbadano obiecujące nowe podejście do wyłączenia kluczowego wspomagacza wzrostu guza, wykorzystując sztuczną inteligencję do przesiewu ponad stu milionów potencjalnych związków na komputerze, zanim którykolwiek z nich zostanie zmieszany w prawdziwej probówce.
Ukryty przełącznik wewnątrz komórek nowotworowych
Głęboko wewnątrz naszych komórek enzym o nazwie NSUN2 działa jak chemiczny marker dla RNA — cząsteczki, która pomaga przekształcać geny w białka. Poprzez dodawanie drobnych chemicznych znaków do RNA, NSUN2 może uczynić komunikaty związane ze wzrostem bardziej stabilnymi i łatwiejszymi do odczytania. Wiele nowotworów, w tym płuca, żołądek, trzustka i piersi, zwiększa poziomy NSUN2, co wzmacnia ich zdolność do dzielenia się, rozprzestrzeniania i oporności na leki ukierunkowane. Mimo jego znaczenia istnieje bardzo niewiele kandydatów na leki, które bezpiecznie obniżałyby aktywność NSUN2, zwłaszcza odwracalnych związków, które nie uszkadzają trwale enzymu.
Puszczenie AI na morze cząsteczek
Tradycyjne odkrywanie leków miałoby trudności z przetestowaniem milionów cząsteczek przeciw NSUN2 w laboratorium, ponieważ każdy eksperyment wymaga złożonych mieszanek RNA i pomocniczych reagentów. Zamiast tego badacze zbudowali całkowicie cyfrowy proces. Zaczęli od przewidzianego trójwymiarowego kształtu ludzkiego NSUN2 wygenerowanego przez AlphaFold — system AI, który zrewolucjonizował przewidywanie struktur. Aby upewnić się, że model jest wiarygodny, wyrównali go z blisko spokrewnionym enzymem, którego struktura jest znana z badań rentgenowskich. Krytyczna wnęka, w której NSUN2 wiąże swój naturalny kofaktor, okazała się silnie zachowana, co dało zespołowi pewność, że wirtualne dokowanie potencjalnych leków w tym miejscu będzie sensowne.
Od setek milionów do garstki
Mając ustaloną kieszeń docelową, zespół sięgnął do obszernej publicznej bazy danych dostępnych do kupienia cząsteczek. Najpierw dokowali zestaw treningowy związków w kieszeni NSUN2 i użyli uzyskanych wyników, aby nauczyć model uczenia maszynowego, które kształty są najbardziej obiecujące. Ten model następnie szybko przesiał około 350 milionów cząsteczek i oznaczył około 101 milionów jako prawdopodobne „trafienia”. Aby jeszcze bardziej zawęzić listę, najlepszą część ponownie dokowano przy użyciu dokładniejszych obliczeń i ostatecznie wybrano jedynie najlepsze 12 000 z silnie przewidywanym wiązaniem. Następnie poddano je serii komputerowych testów bezpieczeństwa, które oszacowały, jak organizm może wchłaniać, rozprowadzać, rozkładać i tolerować każdy kandydat. Po tych filtrach pozostało tylko 34 związków, które wyglądały na jednocześnie silne i „lekopodobne”.
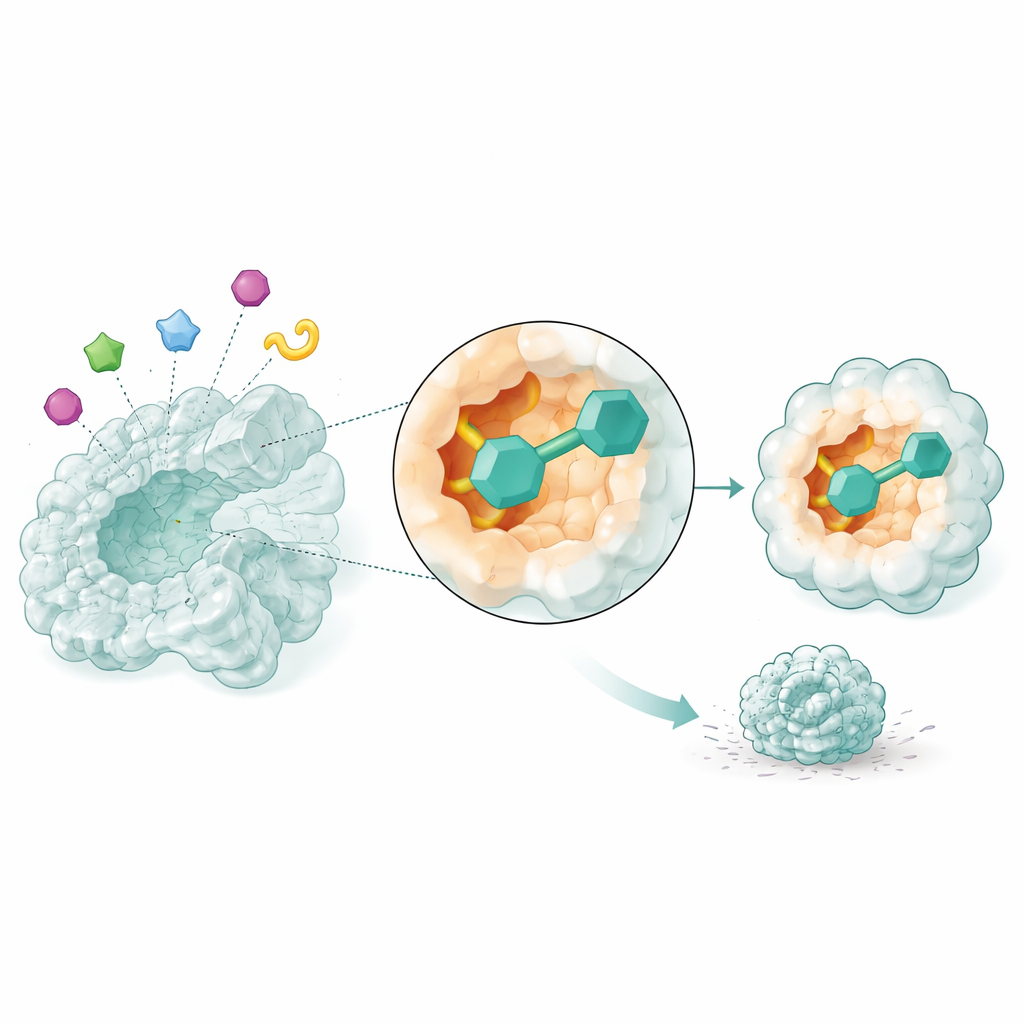
Obserwacja kandydatów w ruchu
Statyczne migawki nie wystarczają, by wiedzieć, czy lek naprawdę utrzyma się przy swoim celu. Dlatego badacze użyli symulacji dynamiki molekularnej, które modelują ruch atomów w czasie, aby obserwować, jak trzy najbardziej obiecujące kandydaty oddziałują z NSUN2 przez 50 miliardowych części sekundy. Dwa związki, zidentyfikowane jedynie przez kody z bazy danych, utworzyły szczególnie stabilne kompleksy: struktura enzymu pozostała zwarta, jego kluczowe regiony były stabilne zamiast wiotkich, a małe cząsteczki utrzymały ciasne dopasowanie w kieszeni przy tworzeniu trwałych kontaktów. Te symulacje sugerują, że te dwa związki mogłyby niezawodnie blokować aktywność NSUN2 w rzeczywistych komórkach.
Co to może oznaczać dla przyszłych terapii
Chociaż wszystkie wyniki w tej pracy pochodzą z obliczeń i wciąż wymagają potwierdzenia w laboratorium, badanie dostarcza krótką listę realistycznych punktów wyjścia do nowych leków blokujących NSUN2. Ponieważ NSUN2 pomaga komórkom nowotworowym stabilizować sygnały wzrostu i przeżycia, takie leki mogłyby osłabić guzy i potencjalnie przywrócić ich wrażliwość na istniejące terapie ukierunkowane, szczególnie w raku płuca, który stał się oporny. Równie ważne jest to, że badanie pokazuje uniwersalny przepis na wykorzystanie AI i modeli opartych na fizyce do szybkiego i taniego przeszukiwania ogromnych przestrzeni chemicznych, oferując potężną skrótową drogę ku następnej generacji precyzyjnych terapii przeciwnowotworowych.
Cytowanie: Yu, S., Peng, Q., Wei, W. et al. AI-driven virtual screening platform identifies novel NSUN2 inhibitor candidates for targeted cancer therapy: a computational drug discovery approach. npj Precis. Onc. 10, 98 (2026). https://doi.org/10.1038/s41698-026-01296-2
Słowa kluczowe: NSUN2, epitranskryptomika, wirtualny przesiew AI, odkrywanie leków przeciwnowotworowych, metylacja RNA