Clear Sky Science · pl
Zróżnicowanie klonotypowe receptorów T oraz ich specjalizacja w nowotworach układu pokarmowego
Dlaczego te badania mają znaczenie dla pacjentów onkologicznych
Immunoterapia nowotworów zrewolucjonizowała leczenie wielu osób, ale nie działa jednakowo u wszystkich. Badanie analizuje głęboko „kody kreskowe” komórek odpornościowych — receptory komórek T — wewnątrz guzów układu pokarmowego, w tym raka jelita grubego i raka żołądka. Odczytując te kody na dużą skalę, autorzy pokazują, jak układ odpornościowy rozpoznaje guzy, jak to rozpoznawanie różni się między typami nowotworów i jak zmienia się, gdy rak jelita grubego daje przerzuty. Te wnioski mogą pomóc lekarzom lepiej przewidywać przebieg choroby i projektować bardziej precyzyjne, spersonalizowane immunoterapie.
Odcisk palca układu odpornościowego w guzach
Limfocyty T są ukierunkowanymi obrońcami organizmu, z których każda nosi unikatowy receptor pozwalający rozpoznać określone nieprawidłowe komórki, w tym nowotworowe. Zespół sekwencjonował receptory komórek T z 415 próbek guza pobranych od 145 pacjentów z rakiem jelita grubego, żołądka i wątroby, łącząc to z szczegółowymi danymi klinicznymi. Analizowali kilka łańcuchów receptorowych definiujących dwie kluczowe rodziny T: konwencjonalne komórki αβ, które napędzają większość odpowiedzi adaptacyjnych, oraz γδ, działające bardziej jak strażnicy szybkiej reakcji. Stwierdzili, że komórki αβ miały tendencję do tworzenia dużych, bardzo zróżnicowanych klonów, podczas gdy γδ tworzyły mniejsze, bardziej wyspecjalizowane grupy. Pacjenci z zaawansowaną chorobą, naciekiem naczyń krwionośnych lub przerzutami mieli bardziej złożone wzory receptorów T, co sugeruje, że postęp guza popycha układ odpornościowy do szerszej, bardziej skomplikowanej walki.
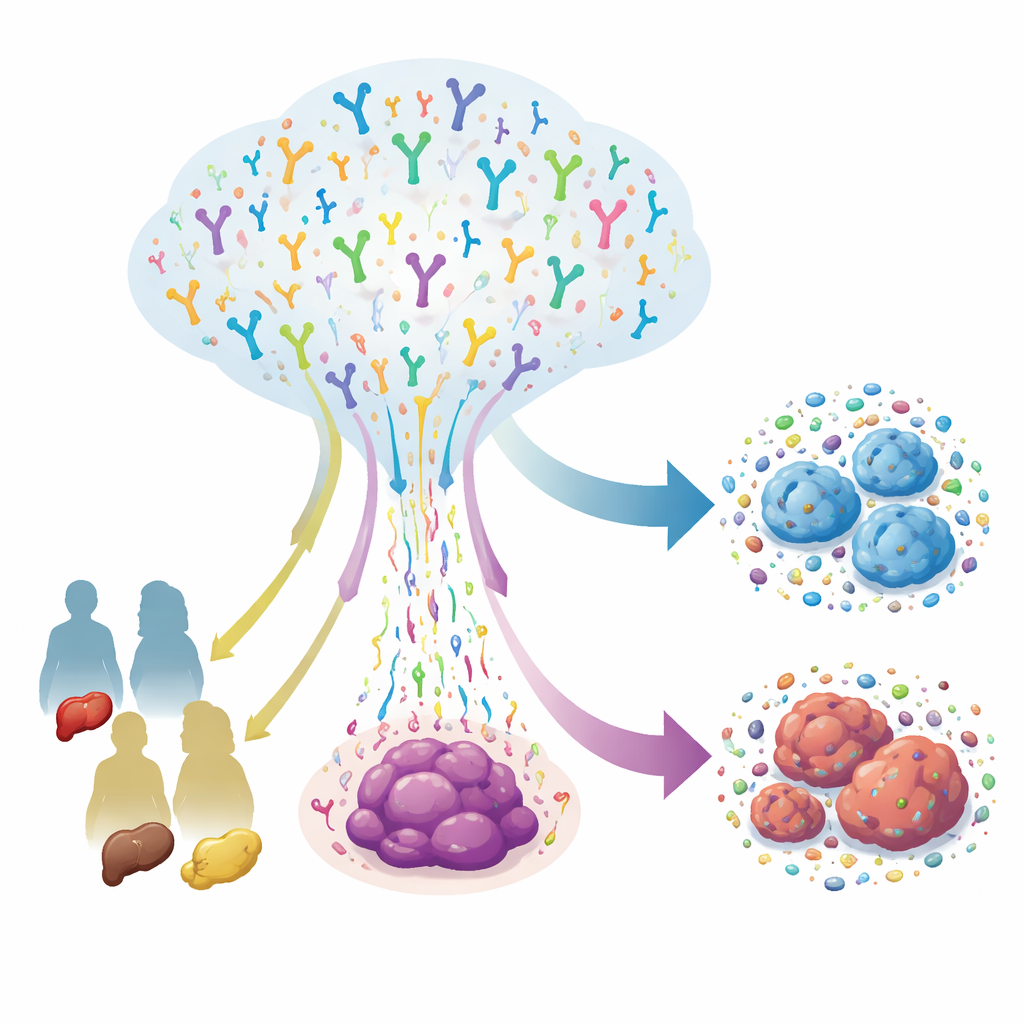
Różne nowotwory, różne strategie układu odpornościowego
Mimo że wszystkie te guzy powstają w układzie pokarmowym, nie przyciągają ani nie kształtują komórek T w jednakowy sposób. Raki jelita grubego były wzbogacone w określone kombinacje segmentów genów receptorowych w klasycznym łańcuchu β, co wskazuje na silną rolę konwencjonalnych komórek T. Raki żołądka z kolei wykazywały większe wykorzystanie receptorów γδ, sugerując, że te mniej zbadane strażnice mogą odgrywać szczególną rolę w guzach żołądka. Gdy badacze przyjrzeli się najważniejszej części receptora — krótkiej pętli, która faktycznie styka się z celami — znaleźli wspólne wzorce sekwencyjne między typami nowotworów, oznaki, że komórki T są kierowane przez podobne selekcyjne naciski. Jednocześnie występowały też wyraźne różnice w długości, składzie aminokwasowym i drobnych powtarzających się „motywach”, co sugeruje, że każdy typ guza zmusza komórki T do rozwiązania nieco innej zagadki rozpoznawczej.
Wspólne i unikatowe cele dla ataku immunologicznego
Wykorzystując globalną bazę znanych par receptor T — antygen, autorzy powiązali konkretne wzory receptorów z ich prawdopodobnymi celami. Niektóre antygeny pojawiały się zarówno w raku jelita grubego, jak i żołądka, w tym znane onkogeny i białka związane z odpornością, takie jak KRAS, SF3B1, BST2 oraz kilka klasycznych antygenów nowotwór‑jądrowo‑jajnikowych (cancer‑testis). Te wspólne cele mogłyby wspierać strategie „pan‑nowotworowe”, wykorzystujące te same narzędzia immunologiczne w różnych typach guzów. Jednocześnie każdy typ nowotworu miał też własne, prywatne cele. Guzy jelita grubego wiązały się z antygenami takimi jak MAGEA10, WT1 oraz z fuzją genową występującą tylko w komórkach nowotworowych, podczas gdy raki żołądka wyróżniały się PABPC1 — białkiem zaangażowanym w kontrolę mRNA. Takie antygeny specyficzne dla guza są atrakcyjnymi kandydatami do wysoce selektywnych szczepionek lub inżynierowanych terapii komórkowych, które oszczędzają tkanki zdrowe.
Jak sygnatury odpornościowe zmieniają się, gdy rak się rozprzestrzenia
Badanie poświęciło szczególną uwagę rakowi jelita grubego, który już dał przerzuty, porównując guzy pacjentów z i bez odległych rozrostów. Guzy przerzutowe były większe, częściej naciekały naczynia krwionośne i wykazywały wyższe poziomy standardowych markerów nowotworowych we krwi. Ich repertuary receptorów T również były bogatsze i bardziej złożone, szczególnie w łańcuchu β, co jest zgodne z trudniejszą i bardziej zróżnicowaną konfrontacją immunologiczną. Śledząc klony wspólne dla ustawień bezprzerzutowych i przerzutowych, badacze pogrupowali je na stabilne, kurczące się lub ekspandujące populacje. Uderzającym odkryciem było to, że niektóre klony γδ T, początkowo rzadkie w guzach pierwotnych, silnie się rozwinęły w chorobie przerzutowej i stały się liczniejsze wraz ze wzrostem guzów. W obrębie konwencjonalnych limfocytów T szczególnie rozszerzona grupa klonów niosła specyficzny motyw sekwencyjny w łańcuchu β i często celowała w MLANA, antygen związany z guzem. Wysoka ekspresja MLANA w guzach jelita grubego wiązała się z lepszym przeżyciem pacjentów, sugerując, że ten antygen może oznaczać nowotwory nadal widoczne dla układu odpornościowego i podatne na terapie oparte na odporności.
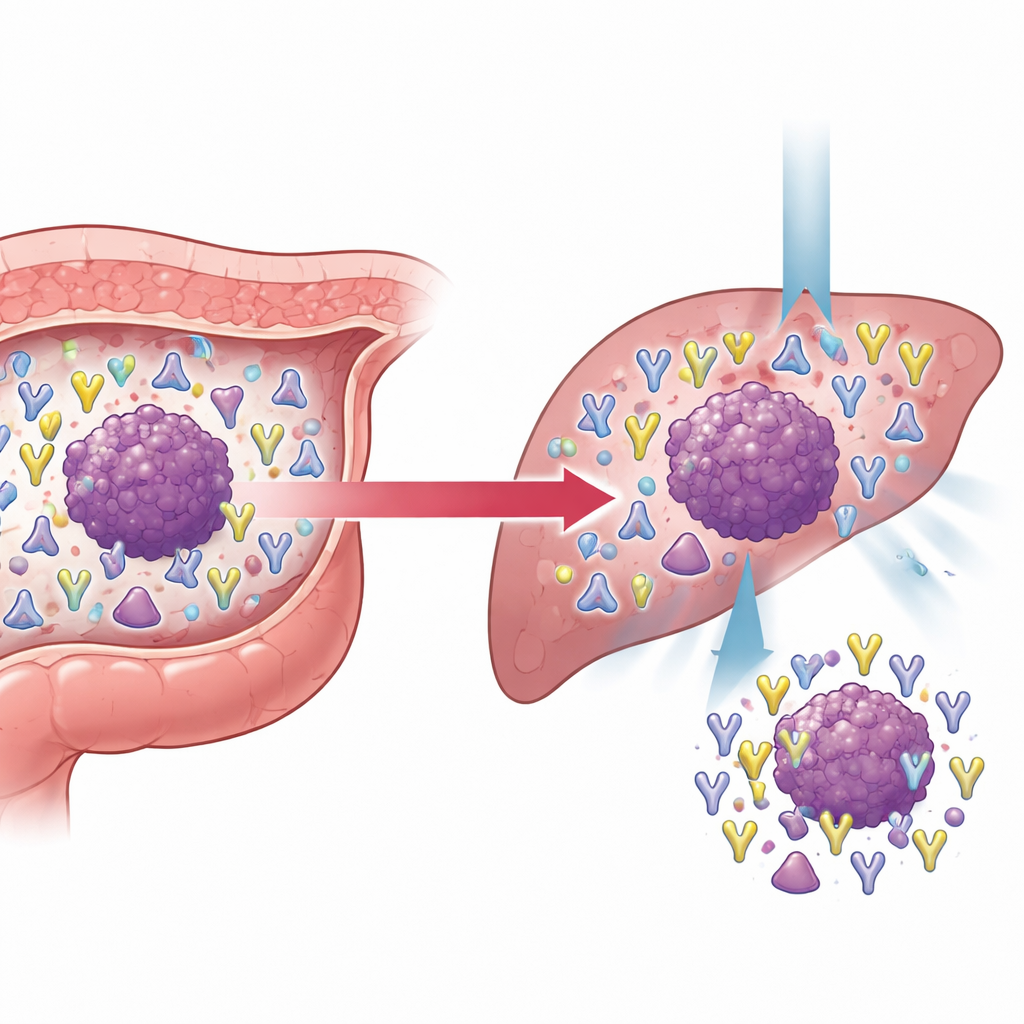
Co to oznacza dla przyszłej opieki onkologicznej
Podsumowując, praca pokazuje, że krajobraz odpornościowy wewnątrz nowotworów układu pokarmowego nie jest przypadkowy, lecz kształtowany przez typ nowotworu, jego stadium i rozprzestrzenianie się. Konkretne wzory receptorów T działają jak czytelne odciski palców tego, jak układ odpornościowy angażuje guz, uwydatniając zarówno wspólne, jak i specyficzne dla nowotworu antygeny. Dla pacjentów oznacza to perspektywę, w której lekarze mogliby profilować repertuar receptorów T z próbki guza, by dopracować prognozę, wybierać immunoterapie z większą precyzją, a nawet projektować spersonalizowane terapie sięgające po najskuteczniejsze klony T. W raku jelita grubego i żołądka sygnatury receptorowe i zidentyfikowane antygeny przedstawione w tym badaniu tworzą mapę drogową dla takich działań w kierunku precyzyjnej immunoterapii.
Cytowanie: Li, L., Li, J., Wang, F. et al. T-cell receptor clonotypic diversity and specialization in digestive system cancers. npj Precis. Onc. 10, 91 (2026). https://doi.org/10.1038/s41698-026-01294-4
Słowa kluczowe: receptory komórek T, rak jelita grubego, rak żołądka, odporność przeciwnowotworowa, biomarkery immunoterapii