Clear Sky Science · pl
Utrata mikroRNA-29b sprzyja DNMT3b-mediowanej obniżce STING prowadzącej do osłabienia immunologii przeciwnowotworowej wywołanej radioterapią w raku jelita grubego z mutacją KRAS
Dlaczego to badanie ma znaczenie
Dla wielu osób z rakiem odbytnicy i okrężnicy radioterapia jest kluczowym elementem leczenia przed operacją. Mimo to niektóre guzy prawie się nie zmniejszają, a choroba często nawraca lub daje przerzuty. To badanie zajmuje się jednym powszechnym zaburzeniem genetycznym w raku jelita grubego — mutacją KRAS — aby wyjaśnić, dlaczego te nowotwory często są oporne na radioterapię i nowe immunoterapie, oraz proponuje strategię ponownego uruchomienia własnego układu odpornościowego przeciwko nim.
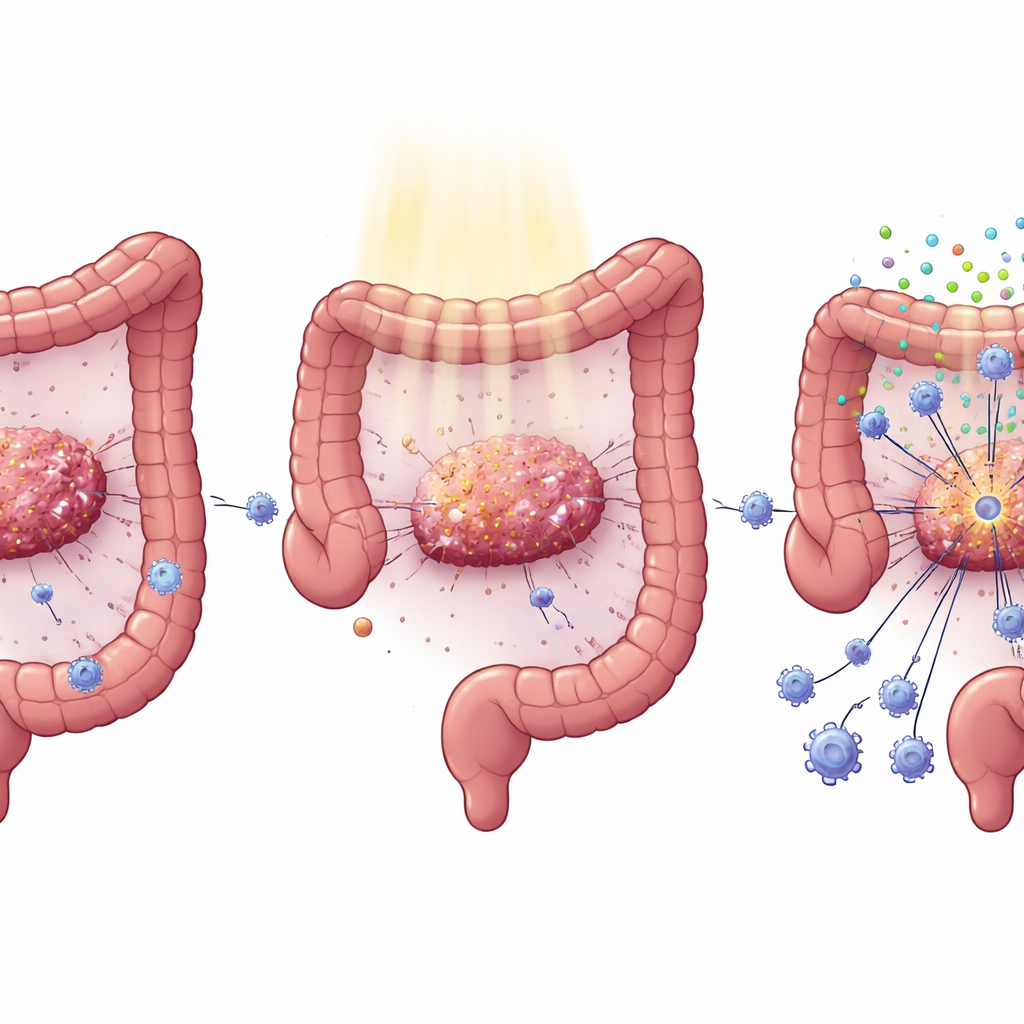
Powszechna mutacja, która ukrywa guzy przed atakiem odporności
Rak jelita grubego często niesie mutacje w genie KRAS, będące głównym czynnikiem napędzającym wzrost i rozprzestrzenianie się nowotworu. Klinicyści zauważyli już wcześniej, że guzy z mutacją KRAS zwykle słabiej reagują zarówno na leki ukierunkowane, jak i na radioterapię. Analizując duże bazy danych nowotworowych oraz próbki pacjentów, autorzy stwierdzili, że guzy z mutantem KRAS mają mniej cytotoksycznych limfocytów CD8 oraz słabszą aktywność stymulujących odporność sygnałów interferonowych. U pacjentów otrzymujących standardową chemioradioterapię przed operacją raka odbytnicy ci z prawidłowym KRAS mieli znacznie większy wzrost liczby limfocytów CD8 wewnątrz guza po leczeniu niż pacjenci z mutacją KRAS, co pomaga wyjaśnić ich lepsze wyniki.
Brakujący system alarmowy w komórkach nowotworowych
Radioterapia nie tylko uszkadza DNA guza; może też działać jak flara, powodując uwalnianie fragmentów DNA przez komórki nowotworowe, które uruchamiają wewnętrzny szlak alarmowy zwany cGAS–STING. Gdy STING jest aktywny, komórki produkują interferony typu I i inne sygnały przyciągające i aktywujące komórki odpornościowe, w tym limfocyty T i komórki dendrytyczne. Badacze wykazali, że w komórkach raka jelita grubego zaprojektowanych tak, by miały mutację KRAS, ten system alarmowy jest stłumiony: po napromienieniu te komórki wytwarzały znacznie mniej interferonu i pokrewnych cząsteczek. U myszy wyciszenie KRAS w guzach przywracało poziomy STING, wzmacniało sygnały interferonowe i prowadziło do większej liczby limfocytów CD4 i CD8, mniejszej liczby regulatorowych komórek T oraz silniejszej kontroli guza — nie tylko w napromienianych guzach, ale także w odległych, nienapromienianych guzach „abscopal”.
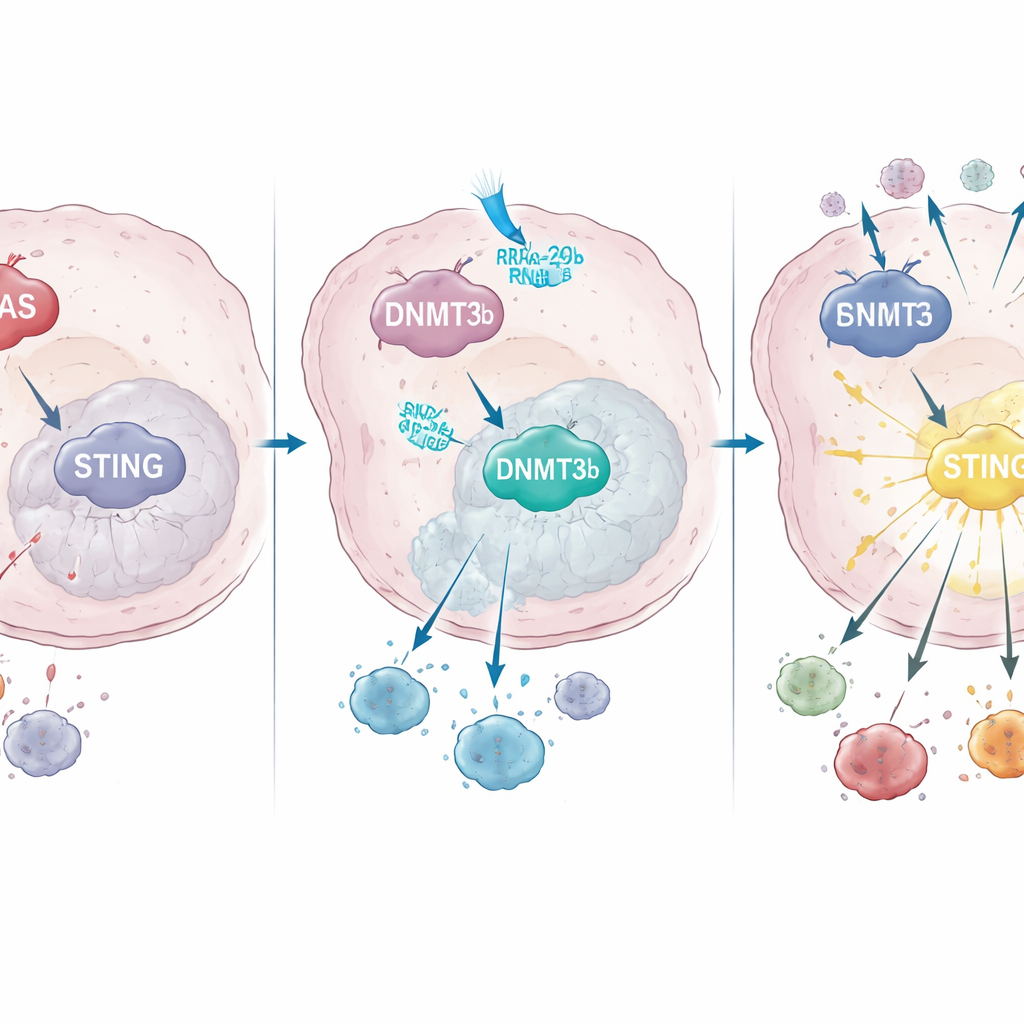
Jak KRAS przebudowuje regulację genów, aby wyłączyć STING
Wnikając głębiej, zespół odkrył, że mutant KRAS zwiększa aktywność enzymu modyfikującego DNA o nazwie DNMT3b, który dodaje grupy metylowe do określonych regionów DNA i wycisza pobliskie geny. Zarówno w liniach komórkowych, jak i w próbkach pacjentów wysoki poziom DNMT3b współwystępował z niskim poziomem STING. Kluczowy fragment promotora STING — region „włącznika” DNA — był silnie metylowany w guzach z mutacją KRAS, ale nie w guzach z prawidłowym KRAS. Pacjenci, których guzy potrafiły zwiększyć ekspresję STING po chemioradioterapii, mieli więcej infiltracji limfocytami CD8 i lepsze przeżycie, co podkreśla znaczenie tego szlaku dla skutecznego leczenia.
Mały RNA, który może ponownie obudzić alarm
Następnie autorzy zapytali, co powoduje tak wysokie stężenie DNMT3b w nowotworach z mutacją KRAS. Dzięki sekwencjonowaniu microRNA zidentyfikowali drobną regulacyjną cząsteczkę RNA, microRNA‑29b‑3p, która normalnie tłumi DNMT3b, lecz jest silnie supresjonowana przez mutant KRAS. Przywrócenie tego microRNA w hodowlach komórkowych z mutacją KRAS obniżało DNMT3b, przywracało STING i wzmacniało produkcję interferonu po radioterapii; blokada microRNA powodowała efekt odwrotny. W próbkach guzów pacjentów osoby z mutacją KRAS miały skłonność do niskiego poziomu microRNA‑29b‑3p, wysokiego DNMT3b i niskiego STING, a pacjenci z wyższym poziomem microRNA‑29b‑3p żyli dłużej, co łączy ten łańcuch molekularny bezpośrednio z wynikami klinicznymi.
Skierowane dostarczanie genu, które wzmacnia radioterapię i immunoterapię
Aby przełożyć te wyniki na potencjalne leczenie, zespół skonstruował nieszkodliwego wirusa (AAV) dostarczającego microRNA‑29b‑3p pod kontrolą promotora aktywnego głównie w komórkach raka jelita grubego. W modelach mysich z guzami raka jelita grubego z mutacją KRAS podanie tego AAV w połączeniu z miejscową radioterapią dramatycznie zmniejszyło zarówno napromieniane guzy, jak i odległe guzy niepoddane radioterapii. Guzy wykazywały mniej DNMT3b, więcej STING, silniejsze sygnały interferonowe oraz intensywną infiltrację przez limfocyty T i inne komórki odpornościowe. Gdy to samo leczenie microRNA‑29b‑3p połączono z inhibitorem punktu kontrolnego immunologicznego skierowanym przeciwko PD‑1, przeżycie poprawiło się jeszcze bardziej, a korzyść ta zależała od limfocytów CD8, co potwierdza, że to układ odpornościowy wykonywał zasadniczą pracę.
Co to może oznaczać dla pacjentów
Mówiąc prosto, badanie to ujawnia, jak rak jelita grubego z mutacją KRAS „przecina przewód” do wewnętrznego systemu alarmowego, który normalnie uruchamia radioterapia, pozwalając tym guzom unikać ataku immunologicznego. Przywracając pojedyncze małe RNA, microRNA‑29b‑3p, badacze mogli obniżyć DNMT3b, obudzić STING i przekształcić immunologicznie „zimne” guzy w „gorące”, które lepiej reagują zarówno na radioterapię, jak i blokadę punktów kontrolnych. Choć prace te pozostają na etapie przedklinicznym, wskazują drogę do przyszłych terapii łączących radioterapię z celowaną terapią genową skierowaną do guza, aby przezwyciężyć oporność w raku jelita grubego z mutacją KRAS i potencjalnie uczynić istniejące terapie skutecznymi dla znacznie większej liczby pacjentów.
Cytowanie: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Słowa kluczowe: rak jelita grubego z mutacją KRAS, oporność na radioterapię, szlak STING, microRNA-29b, immunologia nowotworów