Clear Sky Science · pl
Uczenie głębokie multi-omics poprawia długoterminowe prognozowanie raka piersi oparte na PET-CT z użyciem FDG
Dlaczego ma to znaczenie dla pacjentów i rodzin
Kiedy ktoś otrzymuje diagnozę raka piersi, jednym z pierwszych pytań jest: „Co to oznacza dla mojej przyszłości?” Dzisiejsze systemy stadializacji i badania laboratoryjne dają jedynie przybliżone oszacowania. To badanie sprawdza, czy połączenie skanów medycznych, raportów lekarskich i podstawowych danych klinicznych z zaawansowaną sztuczną inteligencją może dostarczyć jaśniejszego, bardziej spersonalizowanego obrazu długoterminowego przeżycia i ryzyka nawrotu choroby.
Wgląd w wykorzystanie paliwa przez organizm
Kluczowym narzędziem w tych badaniach jest skan zwany FDG PET-CT. Pokazuje on nie tylko kształt tkanek, jak zwykłe CT, lecz także, ile cukru zużywają, co ujawnia aktywność guza. Lekarze już wiedzą, że pewne wartości z tych skanów — na przykład jak „jasno” wygląda guz lub jak duży jest — wiążą się z wynikami klinicznymi. Jednak tradycyjne miary uchwytują tylko niewielką część bogactwa informacji ukrytych w obrazach i często zależą od pracochłonnej pracy specjalistów, którzy ręcznie obrysowują guzy.
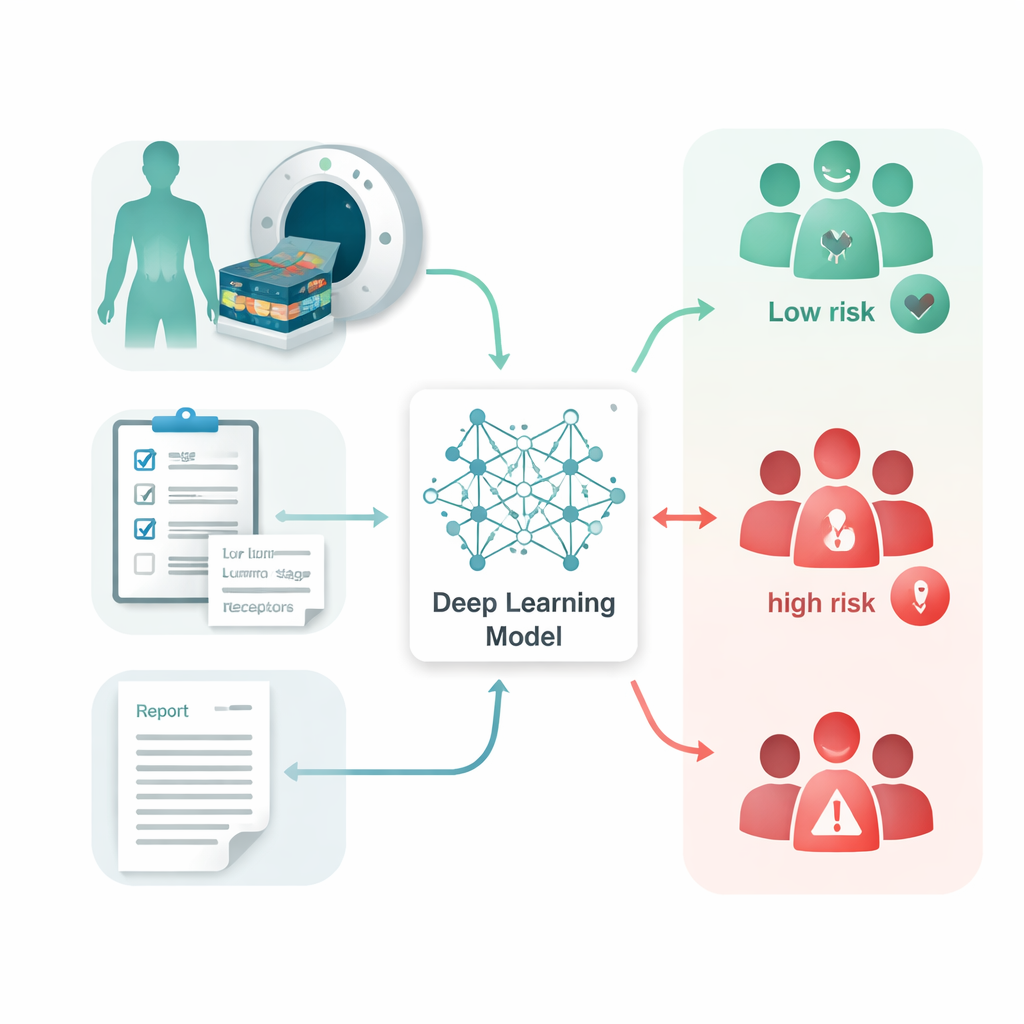
Nauka komputerów czytania skanów i raportów
Naukowcy zgromadzili skany FDG PET-CT, odpowiadające im raporty radiologiczne oraz rutynowe dane kliniczne od 1210 kobiet z rakiem piersi leczonych w jednym holenderskim ośrodku onkologicznym przez 15 lat. U żadnej z nich przy rozpoznaniu nie stwierdzono widocznych odległych przerzutów. Zbudowali system nazwany Multi-Omics Prognostic Stratification (MOPS), który wykorzystuje uczenie głębokie — rodzaj sztucznej inteligencji uczącej się wzorców z dużych zbiorów danych — do łączenia trzech rodzajów informacji: samych obrazów, pisemnych raportów opisujących obserwacje radiologów oraz czynników klinicznych takich jak wiek, rozmiar guza, status węzłów chłonnych i typy receptorów hormonalnych. Zautomatyzowany program najpierw obrysował guzy piersi i zajęte węzły chłonne, aby model mógł skupić się na najbardziej istotnych obszarach bez ręcznego śledzenia.
Więcej dzięki łączeniu wielu wskazówek
Zespół najpierw sprawdził, jak dobrze standardowe miary z obrazów przewidują, kto przeżyje dłużej, a u kogo nastąpi nawrot choroby. Miary odzwierciedlające całkowite obciążenie guzem, takie jak metaboliczna objętość guza i całkowita glikoliza zmian, wypadały lepiej niż prosta miara maksymalnej jasności, ale ich dokładność wciąż była umiarkowana. Model uczenia głębokiego analizujący całe pole klatki piersiowej na PET-CT poprawił te tradycyjne parametry. Następnie badacze przetestowali trzy „strumienie” danych oddzielnie: obrazy, raporty tekstowe i informacje kliniczne. Spośród nich same dane kliniczne zapewniały najsilniejsze pojedyncze źródło prognostyczne. Jednak gdy wszystkie trzy połączono w systemie MOPS, wydajność poprawiła się dalej, oferując bardziej wiarygodne prognozy zarówno dla przeżycia ogólnego, jak i przeżycia bez choroby w perspektywie 3, 5 i 10 lat.
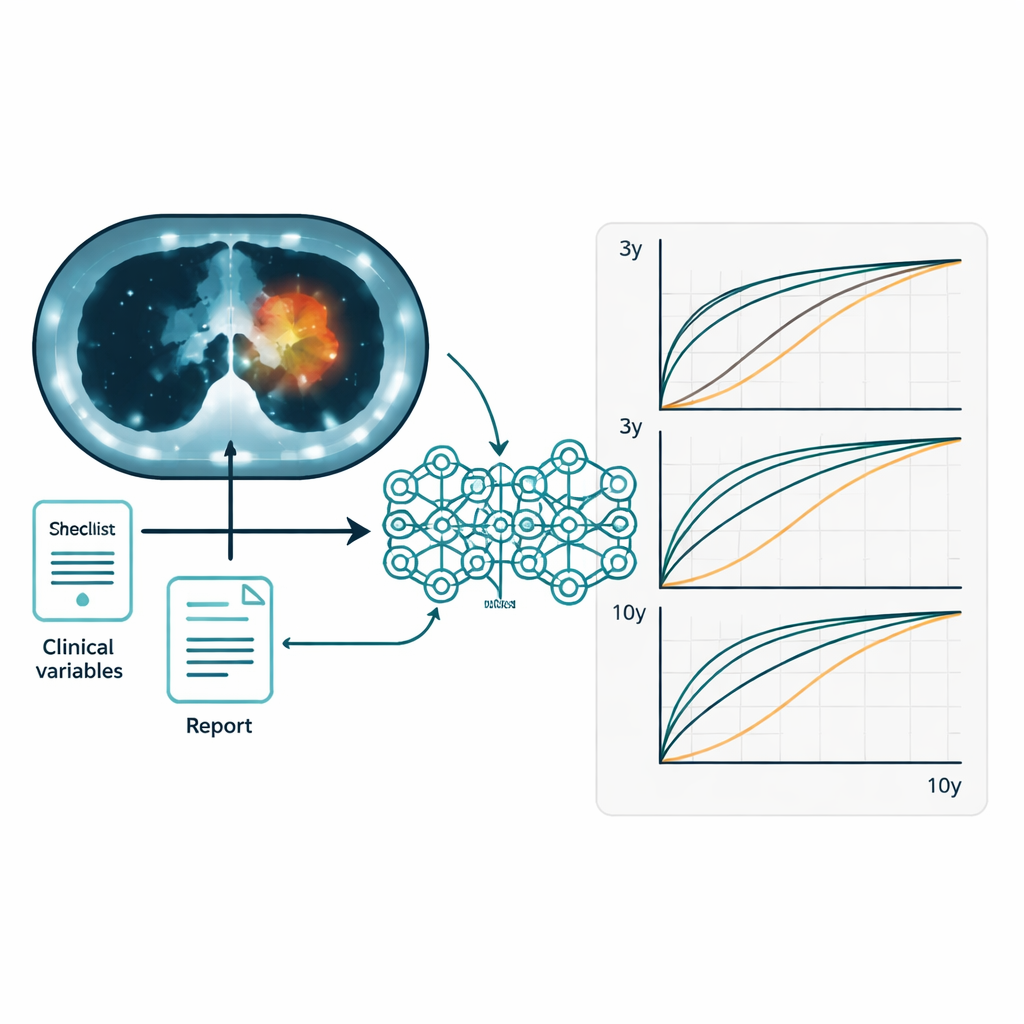
Otwieranie czarnej skrzynki
Ponieważ lekarze muszą móc zaufać i wyjaśnić każde narzędzie wpływające na decyzje terapeutyczne, zespół zaprojektował MOPS z myślą o interpretowalności. Mapy cieplne nakładane na przekroje CT pokazały, że model koncentrował się na pierwotnych guzach piersi i zajętych węzłach chłonnych, a nie na nieistotnych częściach obrazu. W danych klinicznych model wyróżniał znane czynniki o dużym znaczeniu, takie jak rozmiar guza (stopień T), status węzłów chłonnych i historia rodzinna. W raportach tekstowych skłaniał się ku podkreślaniu słów opisujących węzły chłonne, lokalizację guza i aktywność metaboliczną, odzwierciedlając tok rozumowania radiologów. W różnych stadiach zaawansowania i biologicznych podtypach nowotworu model potrafił podzielić pacjentki na grupy wyższego i niższego ryzyka, choć rozróżnienie było oczywiście mniej wyraźne dla bardzo małych, wczesnych zmian, które już mają doskonałe wskaźniki przeżycia.
Co to może znaczyć dla opieki
W praktyce praca ta sugeruje, że przemyślane połączenie obrazowania, notatek lekarskich i standardowych informacji klinicznych może usprawnić oszacowania długoterminowych perspektyw pacjentki z rakiem piersi ponad to, co daje każde pojedyncze źródło. Jeśli zostanie to zweryfikowane w innych szpitalach i na różnych typach skanerów, narzędzie takie jak MOPS mogłoby pomóc lekarzom zidentyfikować pacjentki, które naprawdę potrzebują bliższego nadzoru lub intensywniejszego leczenia, jednocześnie oszczędzając pacjentkom o niższym ryzyku niepotrzebnych terapii i lęku. Zamiast zastępować klinicystów, system działa jako druga para oczu, destylując złożone dane do spersonalizowanego wyniku ryzyka, który wspiera jaśniejsze rozmowy o rokowaniu i kolejnych krokach.
Cytowanie: Liang, X., Zhang, T., Braga, M. et al. Multi-omics deep learning improves FDG PET-CT-based long-term prognostication of breast cancer. npj Precis. Onc. 10, 74 (2026). https://doi.org/10.1038/s41698-026-01283-7
Słowa kluczowe: prognoza raka piersi, obrazowanie PET-CT, uczenie głębokie, multi-omics, predykcja przeżycia