Clear Sky Science · pl
Nadekspresja podjednostki kompleksu I mitochondriów NDUFS4 napędza postęp glejaka przez regulację funkcji mitochondrialnych i COX5B
Dlaczego energetycznie żłodne guzy mózgu są ważne
Glejaki należą do najbardziej agresywnych nowotworów mózgu, często nawracając pomimo operacji, radioterapii i chemioterapii. To badanie zagląda pod maskę komórek glejaka i stawia proste pytanie o dalekosiężnych konsekwencjach: czy te guzy zależą od konkretnej części swoich wewnętrznych „elektrowni”, aby rosnąć i się rozprzestrzeniać? Śledząc małe białko mitochondrialne o nazwie NDUFS4, badacze odkrywają metaboliczny słaby punkt, który wydaje się napędzać postęp nowotworu, podczas gdy zdrowe komórki mózgu pozostają znacznie mniej dotknięte.
Ukryty przełącznik w elektrowniach guza mózgu
Wewnątrz każdej komórki mitochondria działają jak maleńkie generatory, przekształcając składniki odżywcze w użyteczną energię. W komórkach glejaka te generatory pracują na przyspieszonych obrotach. Zespół przeanalizował duże publiczne zbiory danych onkologicznych i dane sekwencjonowania pojedynczych komórek i stwierdził, że białko NDUFS4 — składnik jednego z głównych kompleksów wytwarzających energię w mitochondriach — jest konsekwentnie podwyższone w tkance glejakowej w porównaniu z normalnym mózgiem. Wyższy poziom NDUFS4 korelował z wyższym stopniem zaawansowania guza i z krótszym przeżyciem pacjentów. Analiza na poziomie pojedynczych komórek wykazała, że to dodatkowe NDUFS4 skupia się konkretnie w komórkach nowotworowych, a nie w otaczających je komórkach nieonkologicznych mózgu.
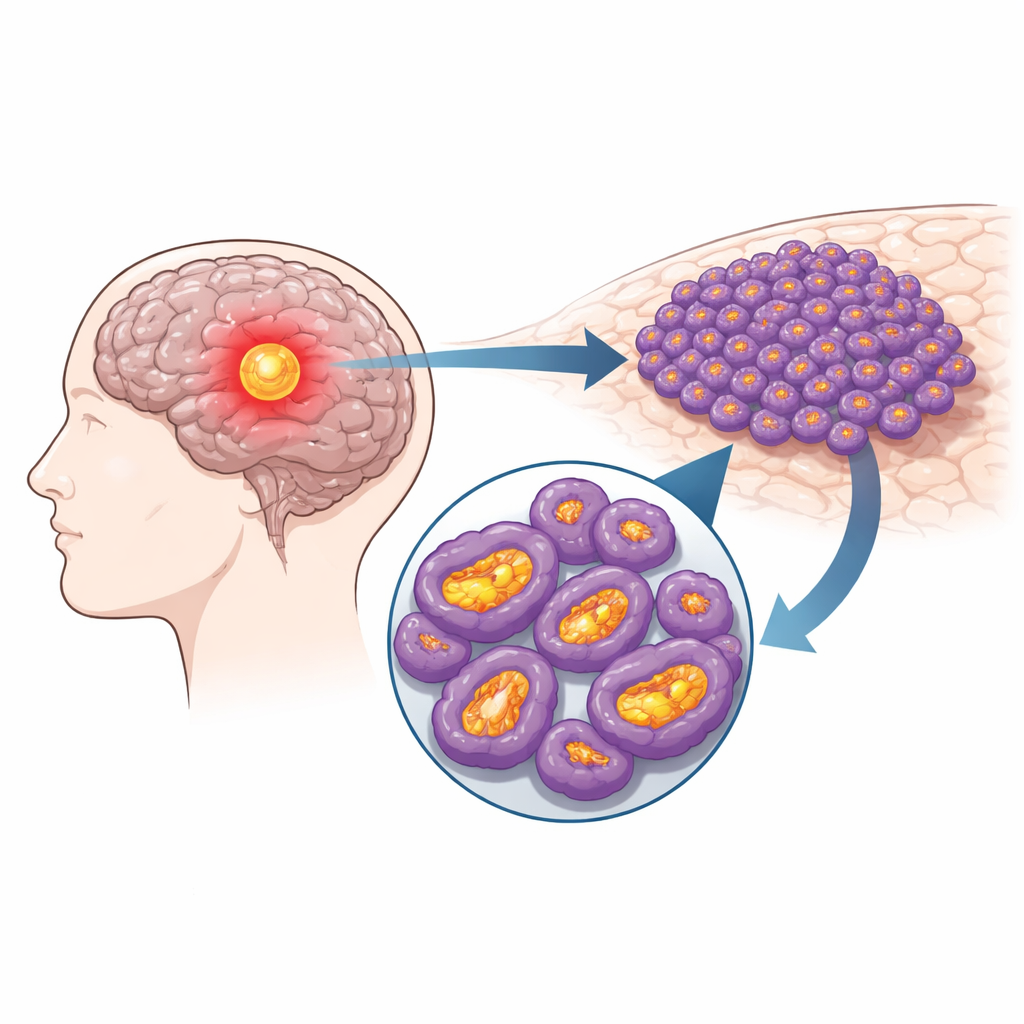
Przykręcenie pokrętła energii, aby spowolnić raka
Aby sprawdzić, czy NDUFS4 jest tylko markerem, czy rzeczywistym sprawcą, badacze celowo zmniejszyli albo całkowicie usunęli jego ekspresję w komórkach glejakowych pochodzących od pacjentów hodowanych w laboratorium. Gdy NDUFS4 został wyciszony lub wyeliminowany, mitochondria komórek zawodziły: spadło zużycie tlenu, osłabł kluczowy etap wytwarzania energii, a poziom paliwa komórkowego (ATP) się obniżył. Równocześnie wzrosła ilość szkodliwych produktów ubocznych, tzw. reaktywnych form tlenu, a wewnętrzne błony komórkowe wykazywały oznaki stresu i utlenienia. Funkcjonalnie te pozbawione energii komórki nowotworowe dzieliły się mniej, tworzyły mniej kolonii, poruszały się i inwadowały słabiej oraz wykazywały więcej cech zaprogramowanej śmierci. Co znamienne, ta sama interwencja genetyczna w niezmienionych astrocytach — komórkach wspierających z normalnej tkanki mózgowej — wywołała niewielkie lub żadne szkody, co sugeruje, że komórki nowotworowe są wyjątkowo zależne od tego mitochondrialnego przełącznika.
Zwiększenie mocy czyni guzy bardziej agresywnymi
Druga strona eksperymentu dała równie przejrzysty obraz. Gdy naukowcy zmusili komórki glejakowe do produkcji dodatkowego NDUFS4, ich mitochondria stały się bardziej aktywne: wzrosła produkcja energii, a kluczowy kompleks oddechowy pracował mocniej. Tak wzmocnione komórki rosły szybciej, migrowały chętniej i agresywniej penetrowały bariery, zarówno w komórkach pierwotnych od pacjentów, jak i w standardowych liniach komórkowych. U myszy komórki glejakowe zaprojektowane tak, by utrzymywać wysoki poziom NDUFS4, tworzyły większe guzy śródczaszkowe, podczas gdy komórki z obniżonym NDUFS4 rosły w mózgu znacznie wolniej, wykazywały słabszą sprawność mitochondrialną, więcej uszkodzeń oksydacyjnych, mniej dzielących się komórek i więcej komórek ginących. W sumie te eksperymenty ustanawiają NDUFS4 nie tylko jako pasażera, lecz jako czynnik napędzający progresję glejaka.
Partner białkowy łączy kontrolę energii z zachowaniem guza
Pogłębiając analizę, zespół zapytał, jak NDUFS4 wywiera tak szerokie efekty. Poprzez porównanie danych ekspresji genów z masowych próbek guzów, pojedynczych komórek i map białkowych komórek nowotworowych, wytypowali kolejne białko mitochondrialne — COX5B — jako kluczowego partnera. COX5B uczestniczy w końcowym etapie głównego łańcucha energetycznego komórki. Było ono silnie skorelowane z poziomami NDUFS4 w glejakach i już wcześniej wiadomo, że jest podwyższone w innych nowotworach. Gdy badacze zmniejszyli COX5B w komórkach glejakowych, zaobserwowali ten sam wzorzec co przy utracie NDUFS4: osłabienie wydajności mitochondriów, większy stres oksydacyjny, wolniejszy wzrost i migrację oraz więcej śmierci komórek. Co kluczowe, przywrócenie COX5B w komórkach pozbawionych NDUFS4 odwracało w dużej mierze uszkodzenia mitochondrialne i efekt przeciwguźny. Odkryli też, że NDUFS4 wpływa na to, jak mocno czynnik transkrypcyjny (Sp1) wiąże się z regionem kontrolnym genu COX5B, pomagając regulować ilość produkowanego COX5B.
Co to oznacza dla przyszłych terapii nowotworów mózgu
Dla osób spoza specjalności główne przesłanie jest takie: wiele glejaków wydaje się polegać na wyśrubowanym systemie energetycznym skupionym wokół NDUFS4 i jego wtórnego partnera COX5B. Przykręcenie tego systemu pozbawia komórki nowotworowe paliwa i równowagi potrzebnej do wzrostu i inwazji, jednocześnie oszczędzając w stosunkowo dużym stopniu normalne komórki wspierające mózgu. Ponieważ ta podatność pojawia się konsekwentnie w próbkach pacjentów, izolowanych komórkach i guzach u myszy, NDUFS4 — oraz jego kontrola nad COX5B — wyłania się jako obiecujący cel dla nowych leków. Terapie selektywnie zakłócające ten mitochondrialny „obwód zasilania” mogłyby uzupełniać istniejące leczenie, potencjalnie spowalniając wzrost guza i wydłużając przeżycie bez druzgocącego uszkadzania zdrowej tkanki mózgowej.
Cytowanie: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
Słowa kluczowe: glejak, mitochondria, NDUFS4, COX5B, metabolizm nowotworów mózgu