Clear Sky Science · pl
Zintegrowany atlas raka płuca na poziomie pojedynczych komórek ujawnia odrębne fenotypy fibroblastów między gruczolakorakami a rakami płaskonabłonkowymi
Dlaczego otoczenie guza ma znaczenie
Rak płuca to nie tylko komórki nowotworowe. To raczej zatłoczone miasto, w którym komórki rakowe współistnieją z naczyniami krwionośnymi, komórkami układu odpornościowego i komórkami wspierającymi. W tym badaniu zadano pozornie proste pytanie o dużych implikacjach: czy dwie główne postacie niedrobnokomórkowego raka płuca — gruczolakorak i rak płaskonabłonkowy — tworzą różne „sąsiedztwa” w płucu i czy te różnice mogą pomóc wyjaśnić, dlaczego pacjenci mają różne wyniki? Wykorzystując potężne narzędzia do czytania DNA pojedynczych komórek, badacze odwzorowali setki tysięcy pojedynczych komórek, pokazując, że jedna kluczowa grupa komórek wspierających, zwana fibroblastami, zachowuje się bardzo różnie w tych dwóch typach raka.
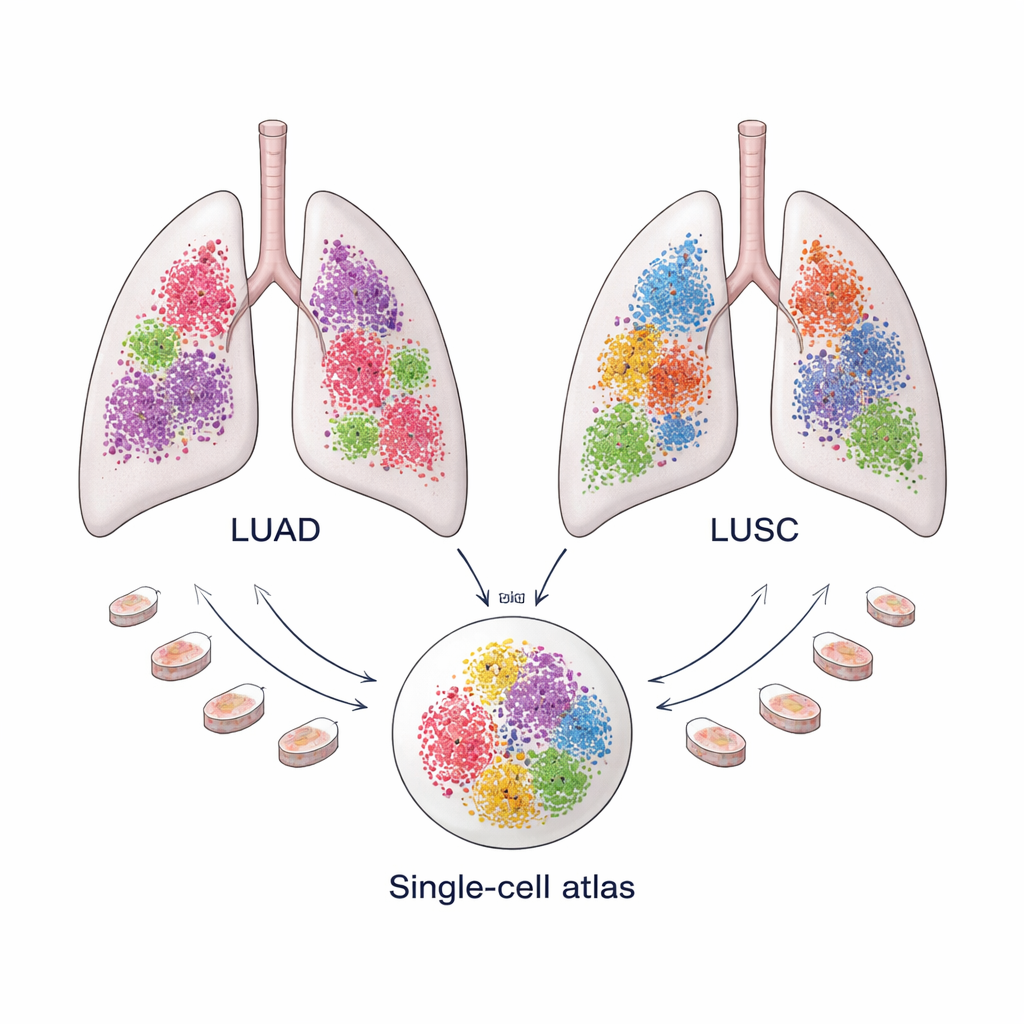
Dwa powszechne raki płuca, dwa odrębne ekosystemy
Niedrobnokomórkowy rak płuca stanowi około 85 procent przypadków raka płuca i dominuje w nim dwóch typów: gruczolakorak płuca (LUAD), który często powstaje w zewnętrznych partiach płuca, oraz rak płaskonabłonkowy płuca (LUSC), częściej występujący centralnie. Chociaż oba są dziś traktowane pod tym samym szerokim mianem, różnie reagują na leczenie i mają odmienne długoterminowe wyniki. Coraz więcej dowodów sugeruje, że te różnice wynikają nie tylko z cech komórek rakowych, lecz także z „mikrośrodowiska guza” — mieszanki komórek odpornościowych, naczyń i komórek strukturalnych, które otaczają i oddziałują z guzem.
Budowanie atlasu raka płuca na poziomie pojedynczych komórek
Aby szczegółowo poznać te mikrośrodowiska, zespół stworzył duży „atlas” danych z sekwencjonowania RNA pojedynczych komórek: 366 652 komórek z 175 próbek LUAD i 125 238 komórek z 74 próbek LUSC, pochodzących z dziesięciu publicznych zbiorów danych. Wzorzec aktywności genów każdej komórki posłużył jako odcisk palca, który pozwolił badaczom sklasyfikować komórki do głównych grup, takich jak komórki odpornościowe, komórki naczyń, komórki nowotworowe oraz komórki strukturalne lub „stromalne”. Zaawansowane metody obliczeniowe usunęły następnie zakłócenia techniczne i wyrównały próbki, tak by komórki z różnych pacjentów mogły być porównywane bezpośrednio. Taki zakres jest kluczowy, ponieważ niektóre typy komórek — zwłaszcza fibroblasty — są rzadkie i trudne do zebrania w dostatecznej liczbie w pojedynczym badaniu.
Fibroblasty: kształtujące krajobraz guza
Fibroblasty to komórki wspierające, które budują i przebudowują tkankę łączną. W guzach przekształcają się w fibroblasty związane z nowotworem (CAFs), które w zależności od stanu mogą hamować lub wspierać wzrost guza. Analizując ponad 8700 fibroblastów, autorzy wyróżnili pięć głównych podtypów CAF: miofibroblastyczne CAF (mCAFs), zapalne CAF (iCAFs), naczyniowo związane CAF (vCAFs), dzielące się CAF (cCAFs) oraz prezentujące antygen CAF (apCAFs). Równowaga między tymi podtypami różniła się wyraźnie między LUAD a LUSC. Guzy LUAD miały skłonność do większej liczby iCAFs, które wydzielają duże ilości molekuł zapalnych, podczas gdy guzy LUSC były bogatsze w mCAFs, produkujące sztywną, włóknistą tkankę i kształtujące fizyczny szkielet guza.
Komórki nowotworowe uczą fibroblasty ich ról
Aby sprawdzić, czy to komórki nowotworowe instruują fibroblasty, by przyjmowały te tożsamości, badacze hodowali normalne fibroblasty płucne w obecności linii komórkowych LUAD lub LUSC. Pod wpływem komórek LUAD fibroblasty włączały geny typowe dla iCAFs, w tym znane sygnały zapalne, takie jak IL-6 i niektóre chemokiny. W kontakcie z komórkami LUSC te same fibroblasty aktywowały geny mCAF związane ze skurczem mięśniopodobnym i produkcją kolagenu. Analizy komunikacji międzykomórkowej sugerowały, że komórki LUAD używają cytokin takich jak IL-1, LIF i OSM, by napędzać zapalny stan iCAF, podczas gdy komórki LUSC polegają bardziej na sygnałach mechanicznych i niekanonicznym szlaku WNT, by przesunąć fibroblasty ku matryco-tworzącemu stanowi mCAF.
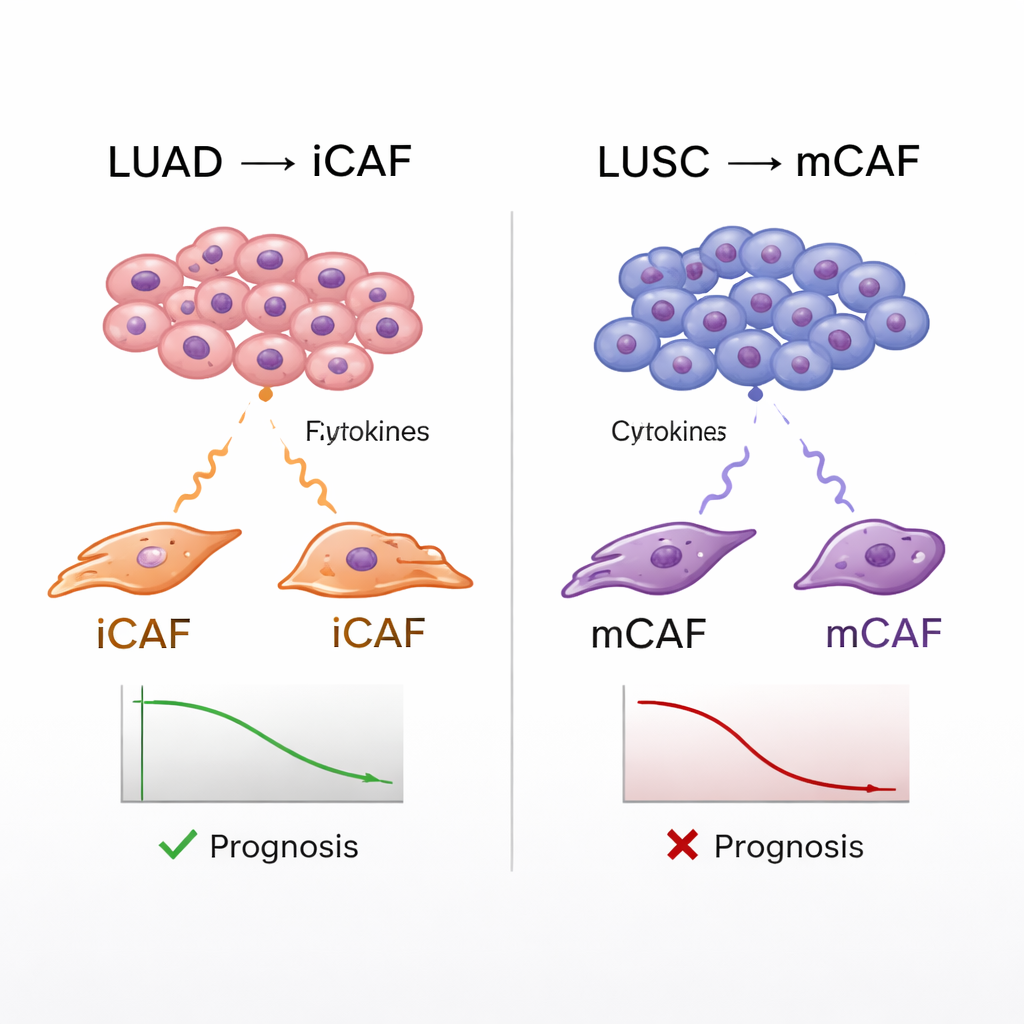
Powiązanie typów fibroblastów z wynikami pacjentów
Atlas pozwolił także zespołowi powiązać podtypy CAF z danymi klinicznymi pacjentów. Korzystając z dużych baz danych onkologicznych, oszacowali, jak silnie każdy guz pacjenta wyrażał sygnatury genowe różnych typów fibroblastów, a następnie porównali te wskaźniki z przeżywalnością. W obu typach — LUAD i LUSC — guzy wzbogacone w mCAFs wiązały się z gorszymi wynikami, co jest zgodne z ideą, że gęsta, włóknista otoczka wokół guzów może sprzyjać progresji nowotworu i blokować atak odpornościowy. iCAFs wykazywały jednak dwoistą rolę: w LUSC wysokie sygnatury iCAF również przewidywały gorsze przeżycie, podczas gdy w LUAD wiązały się z lepszymi wynikami. Dalsze analizy sugerowały, że w LUSC iCAFs przyciągają neutrofile — komórki odpornościowe, które w tym kontekście zdają się hamować pomocne komórki T — tworząc szczególnie niesprzyjające środowisko dla skutecznej odpowiedzi immunologicznej.
Co to oznacza dla przyszłej opieki nad rakiem płuca
Dla osoby niezwiązanej z dziedziną kluczowy przekaz jest taki, że nie wszystkie komórki wspierające w guzach płuca są takie same, a ten sam podtyp fibroblastów może mieć przeciwne znaczenie w zależności od kontekstu nowotworowego. LUAD i LUSC różnią się nie tylko pod względem DNA komórek rakowych; budują różne mikroskopijne ekosystemy, które kształtują wzrost guza i losy pacjentów. Mapując te ekosystemy komórka po komórce, badanie identyfikuje konkretne populacje fibroblastów, które mogłyby służyć jako markery rokownicze lub cele przyszłych terapii — co w optymalnym scenariuszu pozwoli dopasować leczenie nie tylko do typu nowotworu, ale też do składu komórkowego, który go otacza i podtrzymuje.
Cytowanie: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Słowa kluczowe: rak płuca, mikrośrodowisko guza, fibroblasty, sekwencjonowanie RNA pojedynczych komórek, rokowanie w nowotworach