Clear Sky Science · pl
TheraMind: zespół wielu LLM przyspieszający ponowne wykorzystanie leków w raku płuca poprzez wydobywanie danych z opisów przypadków
Dlaczego to ma znaczenie dla pacjentów i lekarzy
Dla osób z zaawansowanym rakiem płuca czas jest na wagę złota, a możliwości leczenia często szybko się wyczerpują. Opracowanie zupełnie nowych leków może zająć ponad dekadę, tymczasem rozproszone wskazówki dotyczące pomocnych terapii mogą już być ukryte w opublikowanych opisach pacjentów, zwanych opisami przypadków. W tym artykule przedstawiono TheraMind — system sztucznej inteligencji, który przeszukuje tysiące takich opisów, aby odnaleźć istniejące leki, które mogłyby zostać bezpiecznie ponownie zastosowane u osób z trudnymi do leczenia nowotworami płuca.
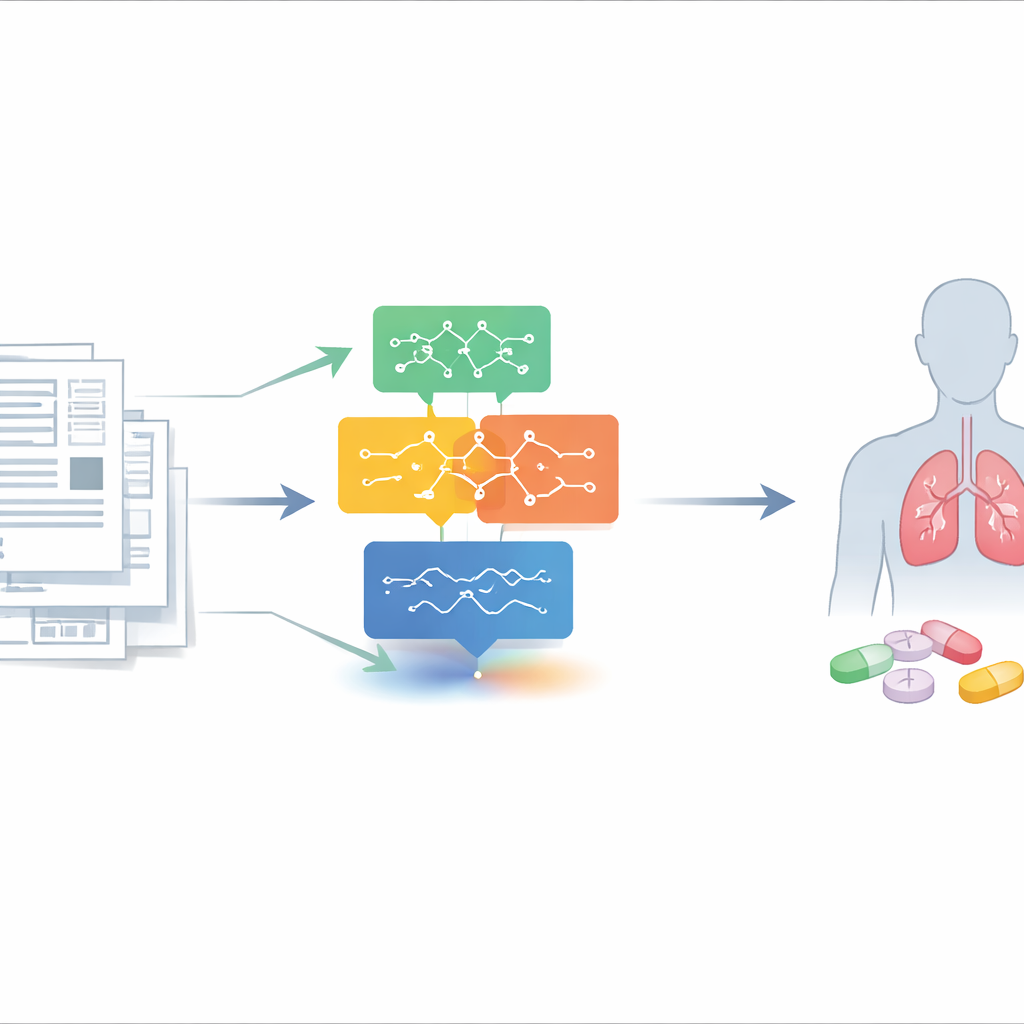
Wyzwanie polegające na znalezieniu nowych zastosowań dawnych leków
Niedrobnokomórkowy rak płuca jest najgroźniejszym nowotworem na świecie, a wskaźniki przeżycia pozostają bardzo niskie po rozprzestrzenieniu się choroby. Odkrywanie i testowanie nowych leków od podstaw jest powolne, kosztowne i obarczone ryzykiem. Natomiast „ponownie wykorzystane” leki są już zatwierdzone dla innych schorzeń, więc ich bezpieczeństwo jest znacznie lepiej poznane. Onkolodzy interesują się takimi lekami, zwłaszcza dla pacjentów, którzy wyczerpali standardowe opcje leczenia, ale potrzebują dowodów z rzeczywistej praktyki, że lek faktycznie pomógł komuś z rakiem płuca — nie tylko obiecających danych z badań laboratoryjnych. Te kliniczne wskazówki często pojawiają się w pojedynczych opisach przypadków ukrytych w literaturze medycznej, które trudno i czasochłonnie znaleźć ręcznie.
Cyfrowy czytelnik tysięcy historii pacjentów
Naukowcy stworzyli TheraMind, aby działał jak niestrudzony, uważny czytelnik opisów przypadków. Rozpoczynając od 18 kandydatów na leki zasugerowanych przez wcześniejsze badania genomowe i laboratoryjne, system automatycznie pobrał 10 023 opisów przypadków z PubMed, największej bazy artykułów medycznych. Następnie podał tekst każdego raportu trzem oddzielnym modelom językowym — różnym „czytelnikom” AI wyszkolonym do rozumienia tekstów medycznych. Dla każdego raportu modele odpowiadały na te same cztery proste pytania: Czy opisany pacjent miał niedrobnokomórkowego raka płuca? Czy badany lek podano konkretnie w celu leczenia tego schorzenia? Czy leczenie przerwano wcześniej? I czy pacjent osiągnął dobry wynik kliniczny?
Jak zespół AI podejmuje wspólną decyzję
Gdy TheraMind zamienia każdy raport na zestaw odpowiedzi tak/nie, wchodzą w grę kolejne warstwy podejmowania decyzji. Jedna metoda wykorzystuje ręcznie skonstruowane drzewo decyzyjne, które wymaga spełnienia wszystkich czterech warunków, zanim przypadek zostanie uznany za istotny dla ponownego wykorzystania leku. Inna pozwala pojedynczemu modelowi elastyczniej ocenić dowody, uwzględniając zarówno odpowiedzi tak/nie, jak i krótkie wyjaśnienia, które wygenerował. Najsilniejsza metoda łączy trzy odrębne klasyfikatory, z których każdy oparty jest na innym modelu, i akceptuje raport tylko wtedy, gdy przynajmniej dwa z trzech zgadzają się, że jest istotny. Podejście „głosu większości” pomaga zniwelować indywidualne błędy, podobnie jak poproszenie kilku niezależnych lekarzy o ocenę tej samej dokumentacji.
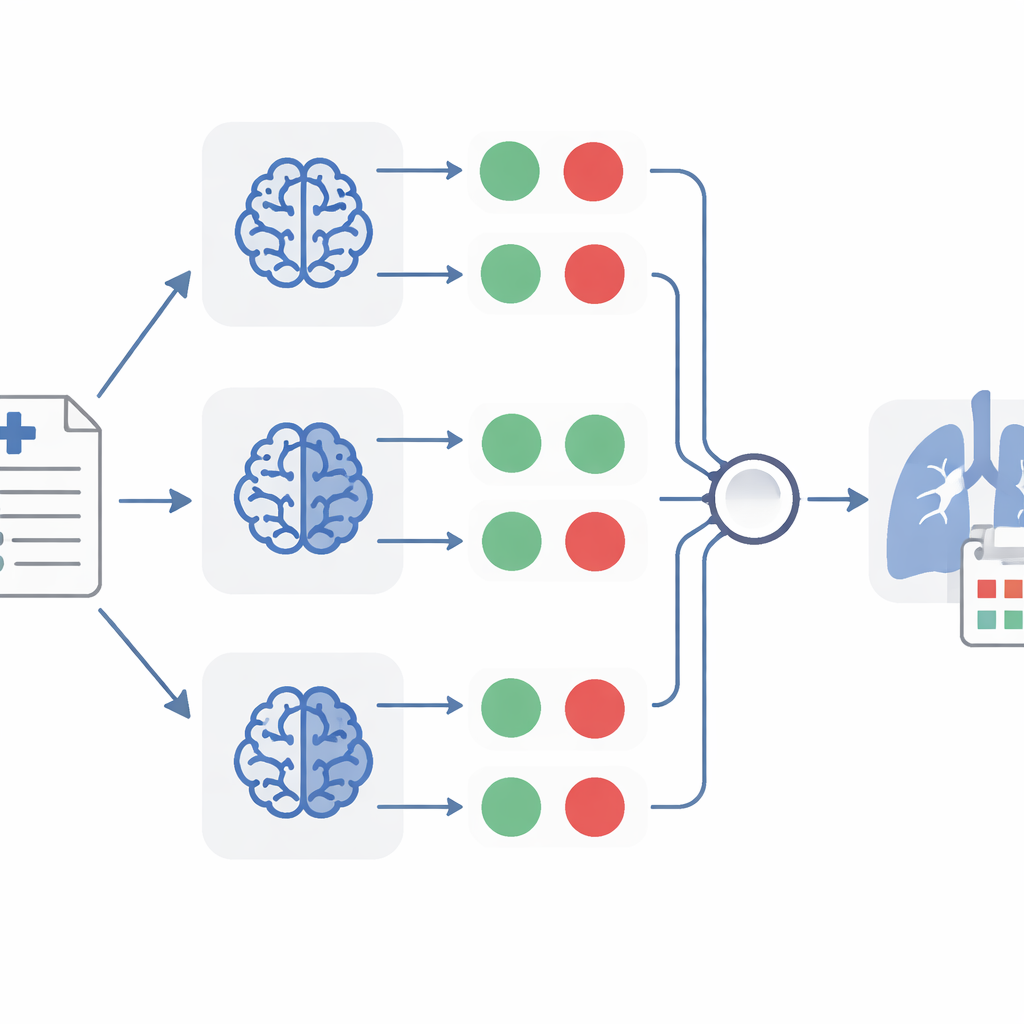
Co TheraMind odkrył w raportach o raku płuca
Zastosowany do dużego zbioru opisów przypadków TheraMind wskazał 26 raportów jako silnie wspierające zastosowanie dziesięciu różnych leków w niedrobnokomórkowym raku płuca. Metoda zespołowa osiągnęła tzw. recall na poziomie około 92 procent, co oznacza, że wychwyciła prawie wszystkie rzeczywiście istotne raporty, jednocześnie utrzymując bardzo wysoką specyficzność wynoszącą 99,7 procent, dzięki czemu bardzo niewiele nieistotnych raportów przedostało się dalej. Dla każdego wybranego raportu system wyodrębnił także kluczowe dane o pacjencie — takie jak wiek, płeć, wywiad chorobowy, stan oraz podejrzewany lek — do spójnego formatu danych i wygenerował krótki, przystępny streszczenie przypadku. Recenzenci ludzie z wykształceniem biologicznym i informatycznym sprawdzili te wyniki i potwierdzili, że jeden z modeli w szczególności wygenerował bardzo dokładne i kompletne ekstrakcje.
Poza rakiem płuca i w kierunku praktyki klinicznej
Aby sprawdzić elastyczność systemu, zespół skierował TheraMind także na raka piersi i kilka kandydatów na leki wcześniej zidentyfikowanych w ich własnych badaniach. W tym przypadku system nie zgłosił żadnych pasujących opisów przypadków, co wiernie odzwierciedla aktualny stan wiedzy naukowej, zamiast tworzyć dowody. Autorzy argumentują, że tego rodzaju ustrukturyzowany, przejrzysty pipeline — łączący logikę opartą na regułach z wieloma czytelnikami AI — może pomóc zmniejszyć przepaść między odkryciami laboratoryjnymi a terapiami gotowymi do badań klinicznych. Zwracają uwagę zarówno na obiecujące zastosowanie podobnych metod w innych nowotworach, jak i na konieczność uważnej ochrony prywatności pacjentów, jeśli przyszłe wersje będą łączyć się bezpośrednio z elektronicznymi rekordami zdrowotnymi.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, TheraMind przekształca rozproszone, niestrukturalne historie pacjentów w uporządkowane dowody, na których lekarze i badacze mogą się oprzeć. Poprzez szybkie uwydatnianie raportów, w których istniejące leki wydają się pomagać osobom z rakiem płuca, może wskazać, które ponownie wykorzystane leki zasługują na bliższe badania w ramach prób klinicznych. Choć nie zastępuje osądu medycznego, ten wielomodelowy czytelnik AI oferuje sposób przesiania gór tekstów medycznych i dostarczenia krótkiej, wiarygodnej listy obiecujących opcji dla pacjentów, którzy pilnie potrzebują nowych możliwości.
Cytowanie: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Słowa kluczowe: ponowne wykorzystanie leków, rak płuca, opisy przypadków, duże modele językowe, wydobywanie dowodów klinicznych