Clear Sky Science · pl
Neoadjuvantowy sintilimab, paklitaksel związany z albuminą i karboplatyna w miejscowo zaawansowanym, resekcyjnym rakowiaku płaskonabłonkowym przełyku: badanie kliniczne i eksploracja mechanizmów
Odwracając losy zabójczego raka gardła
Rak przełyku należy do najbardziej śmiertelnych nowotworów na świecie i często jest wykrywany dopiero po znacznym zaawansowaniu w klatce piersiowej. Wiele osób wciąż kwalifikuje się do operacji, lecz nawet przy najlepszej obecnie chemioterapii i radioterapii ryzyko nawrotu choroby pozostaje wysokie. To badanie sprawdza nowe podejście polegające na wzmocnieniu własnej odporności organizmu przed zabiegiem i analizuje, jak guzy oraz otaczające je komórki zmieniają się pod mikroskopem. Wyniki wskazują na bardziej skuteczne leczenie i drogę ku naprawdę spersonalizowanej opiece.
Nowy trzylekowy plan przed operacją
Badacze zarejestrowali 24 osoby w Chinach z powszechną i agresywną postacią raka przełyku — rakiem płaskonabłonkowym. Wszyscy mieli guzy zaawansowane, ale nadal możliwe do usunięcia chirurgicznie. Przed operacją każdy pacjent otrzymał trzy cykle leczenia skojarzonego: sintilimab, przeciwciało aktywujące układ odpornościowy, które pomaga limfocytom T rozpoznać nowotwór; oraz dwie standardowe chemioterapie, paklitaksel związany z albuminą i karboplatynę. Po tej fazie neoadiuwantowej pacjenci przeszli operację usunięcia guza przełyku, a większość kontynuowała następnie leczenie sintilimabem.
Mocniejsze zmniejszenie guza i obiecujące przeżycia
Gdy chirurdzy i patolodzy oceniali wycięte guzy, stwierdzili, że to przedoperacyjne schematy spowodowały głęboką redukcję u wielu pacjentów. Około 42% wykazało to, co lekarze określają jako duże patologiczne odpowiedzi, czyli że pozostała tylko niewielka część żywych komórek nowotworowych. Jeden na trzech pacjentów nie miał wykrywalnych komórek nowotworowych w głównej masie guza. Na obrazach i w badaniach kontrolnych wyniki również były obiecujące: trzy lata po leczeniu około trzy na cztery osoby żyły bez oznak nawrotu choroby, a niemal cztery na pięć było nadal przy życiu. Co ważne, objawy niepożądane tego nasilonego schematu były możliwe do opanowania — nie odnotowano zgonów związanych z leczeniem, a zabieg chirurgiczny pozostał bezpieczny i wykonalny.
Jak sąsiedztwo guza wpływa na odpowiedź
Nie wszyscy pacjenci skorzystali jednak w równym stopniu, więc zespół zadał pytanie dlaczego. Skoncentrowano się na mikrośrodowisku guza — złożonym otoczeniu komórek nowotworowych, komórek odpornościowych i molekuł sygnalizacyjnych. Wykorzystując ukierunkowane pomiary białek w starannie wyodrębnionych próbkach guza, porównano osoby dobrze reagujące z tymi, które nie reagowały. Przed leczeniem zidentyfikowano 14 białek różnicujących obie grupy. Jedno białko powierzchniowe, CD44, wyróżniało się: guzy o wyższych poziomach CD44 miały skłonność do lepszej odpowiedzi na terapię z sintilimabem. Po leczeniu u osób reagujących obniżyła się ekspresja wielu białek związanych z aktywnością odpornościową i naprawą DNA, co sugeruje, że terapia skojarzona skutecznie zakłóciła mechanizmy wsparcia guza i przekształciła lokalne środowisko immunologiczne.
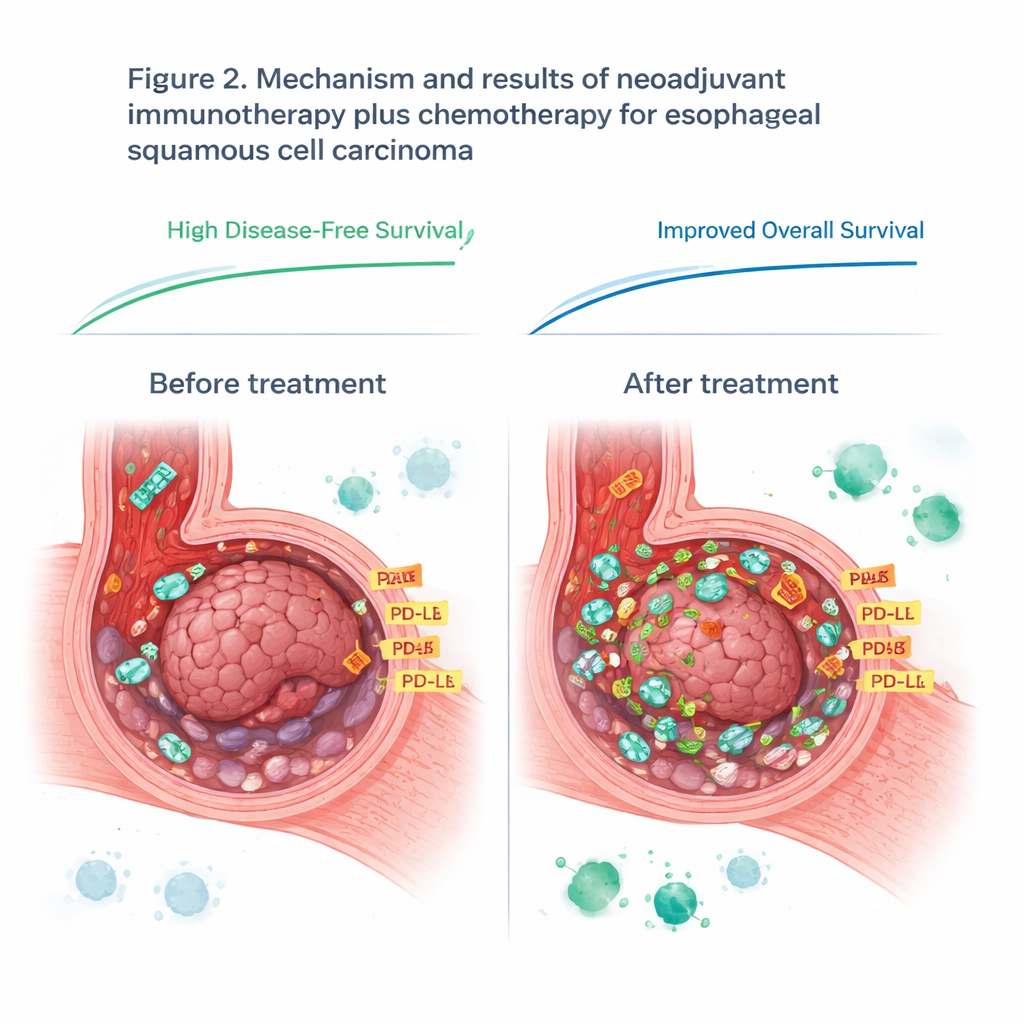
Przemyślenie popularnego markera immunologicznego
Badanie przyjrzało się także PD-L1, białku często wykorzystywanemu jako wskazówka, kto może odnieść korzyść z leków hamujących punkt kontrolny immunologiczny. Przed leczeniem poziomy PD-L1 w próbkach guzów nie przewidywały, kto będzie dobrze reagował, co podważa obecne praktyki w tym typie nowotworu. Jednak w trakcie terapii poziomy PD-L1 wzrosły u każdego pacjenta, prawdopodobnie dlatego, że aktywowany układ odpornościowy napłynął do guza sygnałami zapalnymi. Po terapii wyższe poziomy PD-L1 w pozostałej tkance guza były bliżej związane z tym, jak skuteczna była immunoterapia. To sugeruje, że ma znaczenie moment pomiaru: pojedyncze badanie PD-L1 przed leczeniem może pominąć kluczowe zmiany, które zachodzą po zaangażowaniu układu odpornościowego.
Co to oznacza dla pacjentów i przyszłości
Dla osób przygotowujących się do operacji z powodu zaawansowanego raka przełyku to badanie niesie dwie optymistyczne wiadomości. Po pierwsze, łączenie sintilimabu z chemioterapią przed operacją wydaje się prowadzić do głębszego zmniejszenia guzów i może poprawiać szanse długoterminowego przeżycia, bez dodawania niebezpiecznych działań niepożądanych. Po drugie, praca pokazuje, że guz i jego mikrośrodowisko nie są stałe — są przekształcane przez leczenie w sposób, który można śledzić za pomocą białek takich jak PD-L1 i CD44. W przyszłości takie molekularne „odciski palców” mogą pomóc lekarzom wybierać i dostosowywać terapie w czasie rzeczywistym, przekształcając więcej „zimnych” guzów ignorujących układ odpornościowy w „gorące” guzy zapraszające silną, trwałą odpowiedź immunologiczną.
Cytowanie: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Słowa kluczowe: rak przełyku, immunoterapia, terapia neoadiuwantowa, inhibitory PD-1, mikrośrodowisko guza