Clear Sky Science · pl
Projektowanie terapii z pomocą algorytmów poprawia przeżycia w modelu myszy z potrójnie ujemnym rakiem piersi
Dlaczego inteligentniejsza chemioterapia ma znaczenie
Chemioterapia ratuje życie, ale wciąż jest w dużej mierze stosowana według zasady „jeden rozmiar dla wszystkich”: pacjenci z podobnym nowotworem często otrzymują tę samą dawkę leku w tym samym schemacie. Dla niektórych może to oznaczać silne skutki uboczne, a dla innych — zbyt mały efekt terapeutyczny. Opisane badanie stawia proste, lecz istotne pytanie: co by było, gdybyśmy mogli użyć algorytmów komputerowych do dostosowywania chemioterapii do każdego chorego w czasie rzeczywistym, tak jak termostat reguluje ogrzewanie w domu? Na zaawansowanym modelu myszy z agresywnym rakiem piersi badacze pokazują, że takie dopasowane dawkowanie może wydłużyć przeżycie i ograniczyć rozwój oporności na lek.
Problem rutynowych schematów leczenia onkologicznego
Obecnie wielu pacjentów otrzymuje najwyższą dawkę chemioterapii, jaką mogą tolerować, podawaną w stałych odstępach. Tzw. protokół maksymalnie tolerowanej dawki nie uwzględnia tempa wzrostu konkretnego guza, sposobu, w jaki organizm pacjenta przetwarza lek, ani zmieniającej się odpowiedzi guza w czasie. W efekcie guzy mogą początkowo się kurczyć, a potem nawracać jako odmiany bardziej oporne na lek, podczas gdy pacjenci doświadczają dotkliwych skutków ubocznych. Wcześniejsze próby poprawy tego podejścia, takie jak chemioterapia „metronomiczna” przy użyciu mniejszych, częstszych dawek, dały mieszane wyniki w badaniach klinicznych i nie ustaliły jednoznacznie, jak optymalnie dobierać dawki i harmonogram. Istnieje wyraźna potrzeba bardziej racjonalnego, indywidualnego planowania schematów chemioterapii.
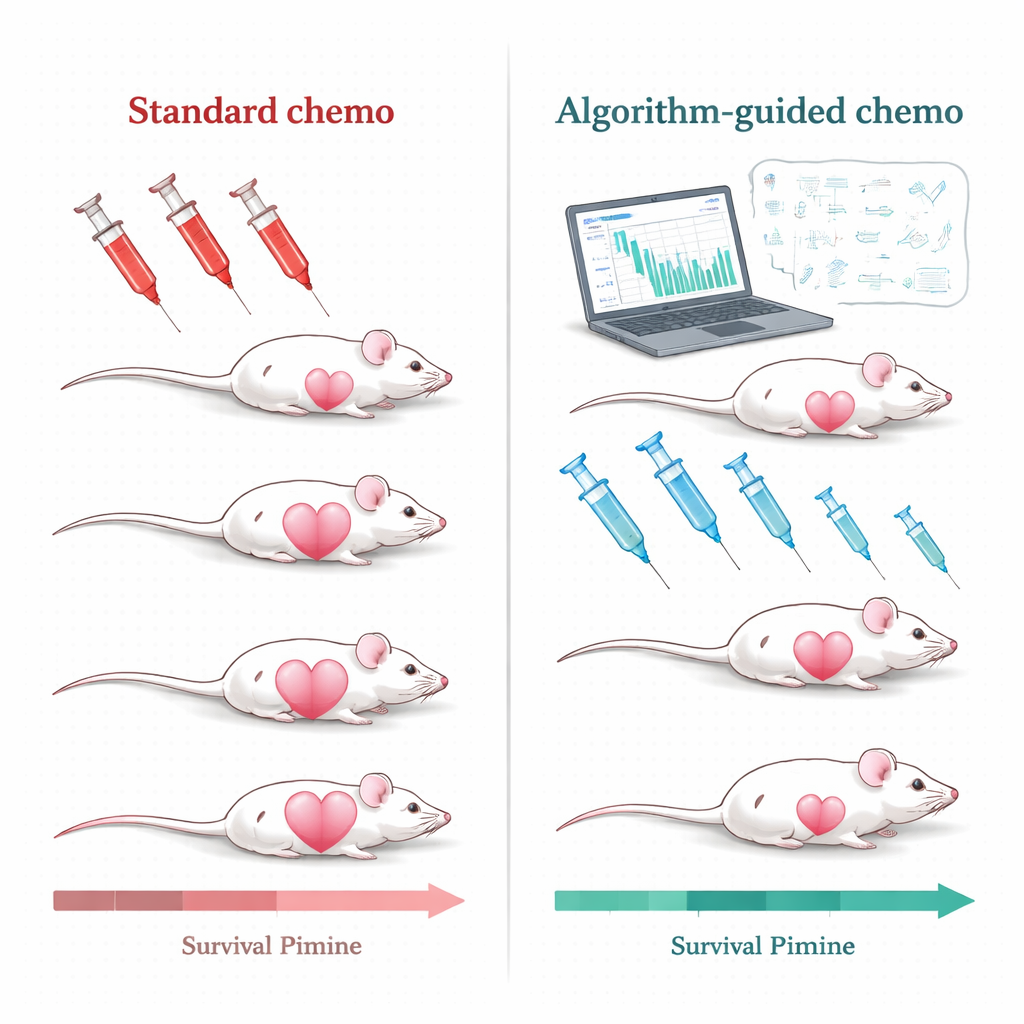
Wykorzystanie algorytmów do dopasowania leczenia
Zespół badawczy podjął to wyzwanie u myszy z potrójnie ujemnymi guzami piersi — postacią raka, która u ludzi jest szczególnie trudna w leczeniu i nadal opiera się w dużej mierze na chemioterapii. Myszy leczono powszechnie stosowaną formułą leku, pegylowaną liposomalną doksorubicyną. Zamiast powtarzać leczenie wysokimi dawkami tylko wtedy, gdy guzy odrastały do określonego rozmiaru, naukowcy zbudowali modele matematyczne opisujące, jak guz rośnie, jak zmniejsza się pod wpływem terapii oraz jak lek krąży we krwi. Modele te zasilono prostymi, klinicznie realistycznymi pomiarami: powtarzanymi odczytami rozmiaru guza i stężeniami leku we krwi. Na podstawie tych danych algorytm komputerowy generował spersonalizowane plany leczenia dla każdej myszy.
Dwa sposoby, by komputer pomagał
Badanie przetestowało dwa warianty projektowania terapii wspomaganej algorytmem. W jednym podejściu, nazwanym PDPK, komputer używał wczesnych danych do zaprojektowania 30-dniowego harmonogramu stosunkowo małych, powtarzanych dawek mających utrzymać stężenie leku we krwi stabilnie, ale nisko — wystarczająco wysoko, by kontrolować guz, lecz na tyle nisko, by ograniczyć toksyczność. W drugim podejściu, zwanym sterowaniem predykcyjnym modelu (model predictive control), algorytm codziennie aktualizował plan na podstawie najnowszego pomiaru guza, dostosowując wielkość dawek, by systematycznie zmniejszać rozmiar guza. Obie metody opierały się na tej samej zasadzie: użyciu realistycznego „cyfrowego bliźniaka” myszy z guzem do symulowania wielu możliwych wzorców dawkowania z wyprzedzeniem i wyboru tych najbardziej obiecujących w ramach ograniczeń bezpieczeństwa.
Dłuższe przeżycie i mniejsza oporność na lek
Gdy zespół porównał te algorytmicznie kierowane schematy z konwencjonalnym protokołem wysokich dawek wywoływanym wzrostem guza, różnice były uderzające. W terapii konwencjonalnej guzy często początkowo silnie się kurczyły, ale ostatecznie powracały, a powtarzane duże dawki sprzyjały pojawieniu się choroby opornej na lek. W przeciwieństwie do tego większość terapii zaprojektowanych przez algorytm utrzymywała guzy pod znacznie lepszą kontrolą, wydłużała czas do nawrotu i w wielu przypadkach zapobiegała wyraźnym oznakom oporności w okresie badania. Wśród dziesiątek myszy grupy PDPK i sterowania predykcyjnego przeżywały znacząco dłużej niż zwierzęta leczone według standardowego schematu, a kilka strategii opartych na algorytmach wykazało silne, istotne statystycznie korzyści w zakresie przeżywalności.
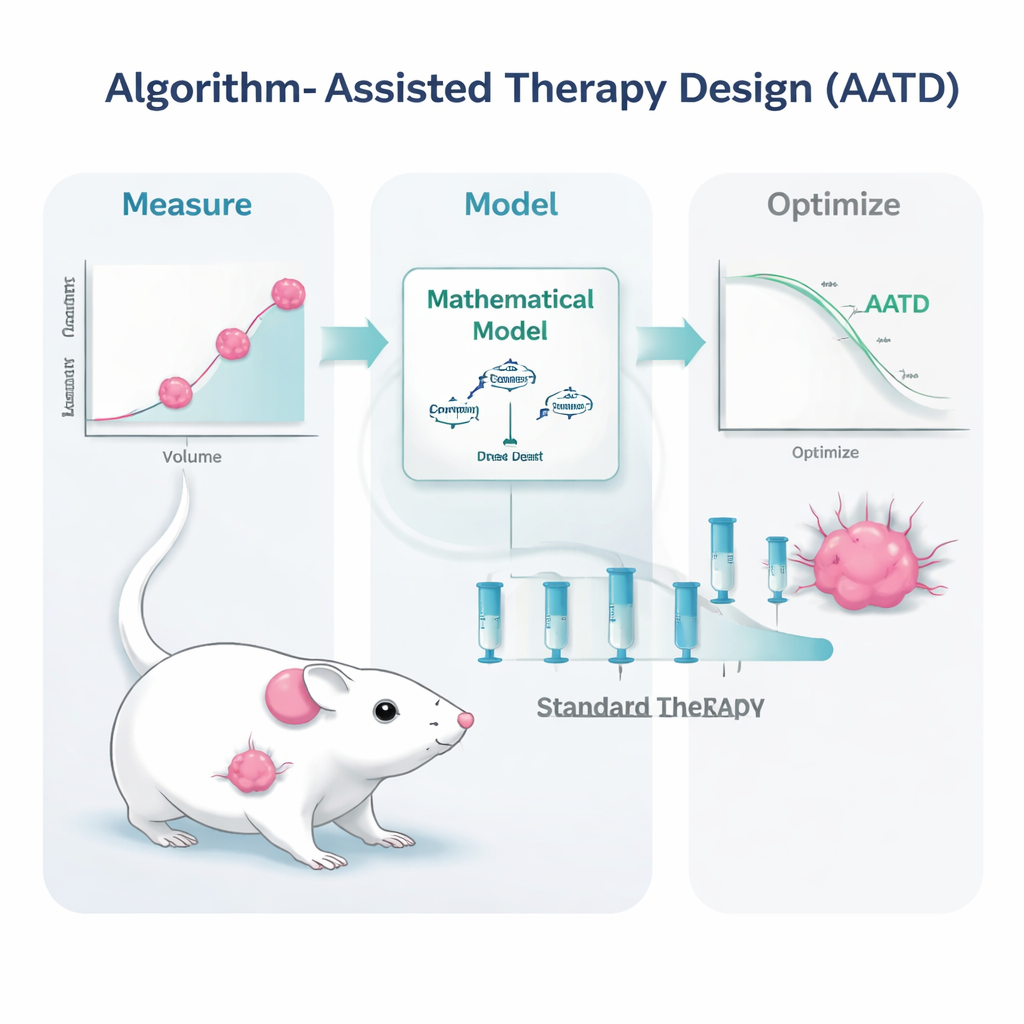
Co to może znaczyć dla przyszłych pacjentów
Chociaż prace przeprowadzono na myszach, ich kluczowe elementy — mierzenie rozmiaru guza, monitorowanie stężeń leku we krwi oraz uruchamianie modeli komputerowych — są już możliwe u pacjentów z użyciem współczesnych narzędzi obrazowania i badań laboratoryjnych. Badanie sugeruje, że zamiast pytać „Jaka jest standardowa dawka?”, lekarze mogliby w przyszłości pytać: „Biorąc pod uwagę zachowanie tego konkretnego guza i sposób gospodarowania lekiem przez tego pacjenta, jaka dawka i rozkład czasowy będą teraz najskuteczniejsze?” Pozostają praktyczne przeszkody, takie jak konieczność częstszych pomiarów i logistyka elastycznego dawkowania, ale przesłanie jest jasne: chemioterapia nie musi być tępa i jednolita. Z pomocą algorytmów może stać się narzędziem bardziej precyzyjnym i adaptacyjnym, dającym pacjentom lepszą szansę na długoterminową kontrolę agresywnych nowotworów.
Cytowanie: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
Słowa kluczowe: spersonalizowana chemioterapia, potrójnie ujemny rak piersi, terapia wspomagana algorytmem, matematyczne modelowanie guza, dawkowanie doksorubicyny