Clear Sky Science · pl
Transkryptomika przestrzenna ujawnia molekularną heterogeniczność i cele terapeutyczne specyficzne dla podtypów w drobnokomórkowym raku płuca
Dlaczego to badanie raka płuca ma znaczenie
Drobnokomórkowy rak płuca jest jednym z najbardziej śmiertelnych nowotworów, występując głównie u osób z historią palenia i często nawracając po chemioterapii. Lekarze wiedzą, że nie wszystkie drobnokomórkowe raki płuca zachowują się jednakowo, lecz brakowało narzędzi pozwalających zobaczyć, jak różne typy komórek nowotworowych i komórki układu odpornościowego są rozmieszczone w obrębie każdego guza. W tym badaniu zastosowano nową technologię odczytującą aktywność genów w tysiącach drobnych punktów na przecięciu guza, tworząc „molekularną mapę” każdej próbki. W połączeniu z niestandardową analizą komputerową badacze odkryli ukryte wzorce, które mogą wskazywać na bardziej precyzyjne, specyficzne dla podtypów terapie.
Mapowanie guzów w kontekście przestrzennym
Zespół przeanalizował próbki guzów od 21 pacjentów z ograniczonym stadium drobnokomórkowego raka płuca, którzy przeszli operację zanim otrzymali jakiekolwiek leki. Zamiast rozdrabniać tkankę i utracić informacje przestrzenne, zastosowali transkryptomikę przestrzenną — technikę mierzącą, które geny są aktywne w wielu określonych punktach na przekroju tkanki. Każdy punkt zachowuje swoje pierwotne położenie, co pozwala naukowcom powiązać aktywność genów z tym, gdzie fizycznie znajdują się komórki nowotworowe, komórki prawidłowe i komórki odpornościowe. Do tego dodali dwa kluczowe narzędzia: nowy wskaźnik „Edgeindex” służący do kwantyfikacji głębokości naciekania komórek nowotworowych w sąsiednią tkankę oraz sztuczną sieć neuronową — formę uczenia maszynowego — do automatycznego oznaczania, które punkty należą do guza, a które nie.
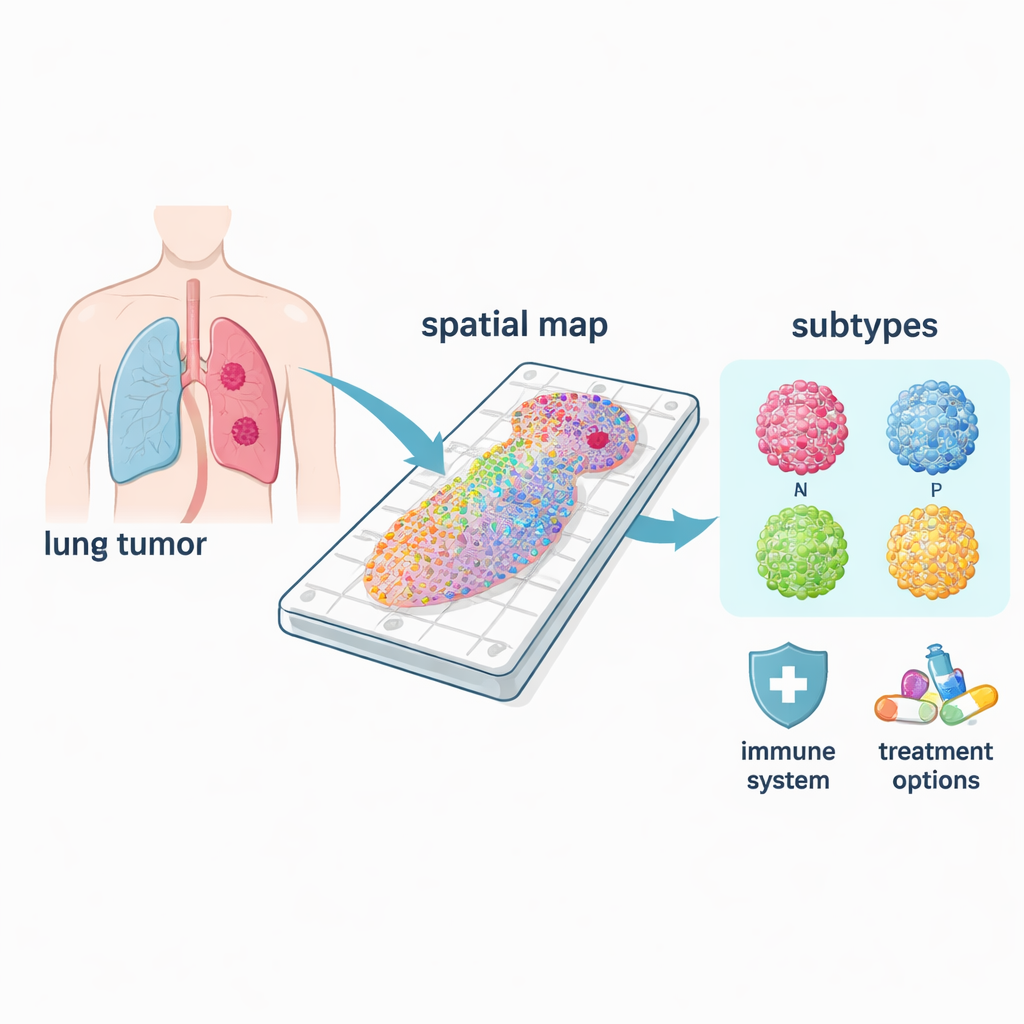
Różne typy nowotworu w jednej chorobie
Drobnokomórkowy rak płuca nie jest jednym schorzeniem, lecz obejmuje co najmniej cztery główne podtypy molekularne, często oznaczane jako ASCL1, NEUROD1, POU2F3 i YAP1, nazwane od kluczowych genów regulatorowych je definiujących. Dzięki mapom przestrzennym badacze mogli zobaczyć, gdzie każdy podtyp dominował w guzach i jak różniła się ich biologia. Powszechne formy ASCL1 i NEUROD1 były silnie powiązane z programami podziału komórek, co odpowiada ich opinii jako wysoce proliferacyjnych. Natomiast obszary POU2F3 łączyły się ze szlakami związanymi z odpowiedzią immunologiczną, a strefy YAP1 wykazywały sygnały związane z metabolizmem i przebudową tkanki — cechy mogące wiązać się z rozsiewem i opornością na leczenie. Ponieważ wzorce te są rozdzielone przestrzennie, metoda potrafi zidentyfikować rzeczywisty „napędzający” podtyp w zmieszanym guzie — tego często nie wykrywają testy masowe.
Brzeg naciekania i przesunięcia immunologiczne
Jedną z kluczowych innowacji badania jest Edgeindex, który mierzy, jak bardzo komórki nowotworowe przenikają do otaczającej tkanki nie‑nowotworowej. Niskie wartości odzwierciedlają zwarte, dobrze odgraniczone guzy, podczas gdy wysokie wartości wskazują na rozproszone wyspy i postrzępione, inwazyjne brzegi. Guzy o wysokim Edgeindex były wzbogacone o programy genowe związane z macierzą zewnątrzkomórkową, przerzutami i śmiercią komórek. Pokazywały też wyraźnie zmienione mikrośrodowisko immunologiczne: mniej limfocytów pomocniczych i innych elementów odporności adaptacyjnej, lecz więcej komórek układu wrodzonego, takich jak niektóre komórki NK i monocyty. Autorzy interpretują to jako „przebudowę niszy immunologicznej”, w której guz odsuwa precyzyjne, ukierunkowane odpowiedzi immunologiczne i pozostawia mniej skuteczną, głównie wrodzoną obronę, która nie jest w stanie w pełni opanować nowotworu.
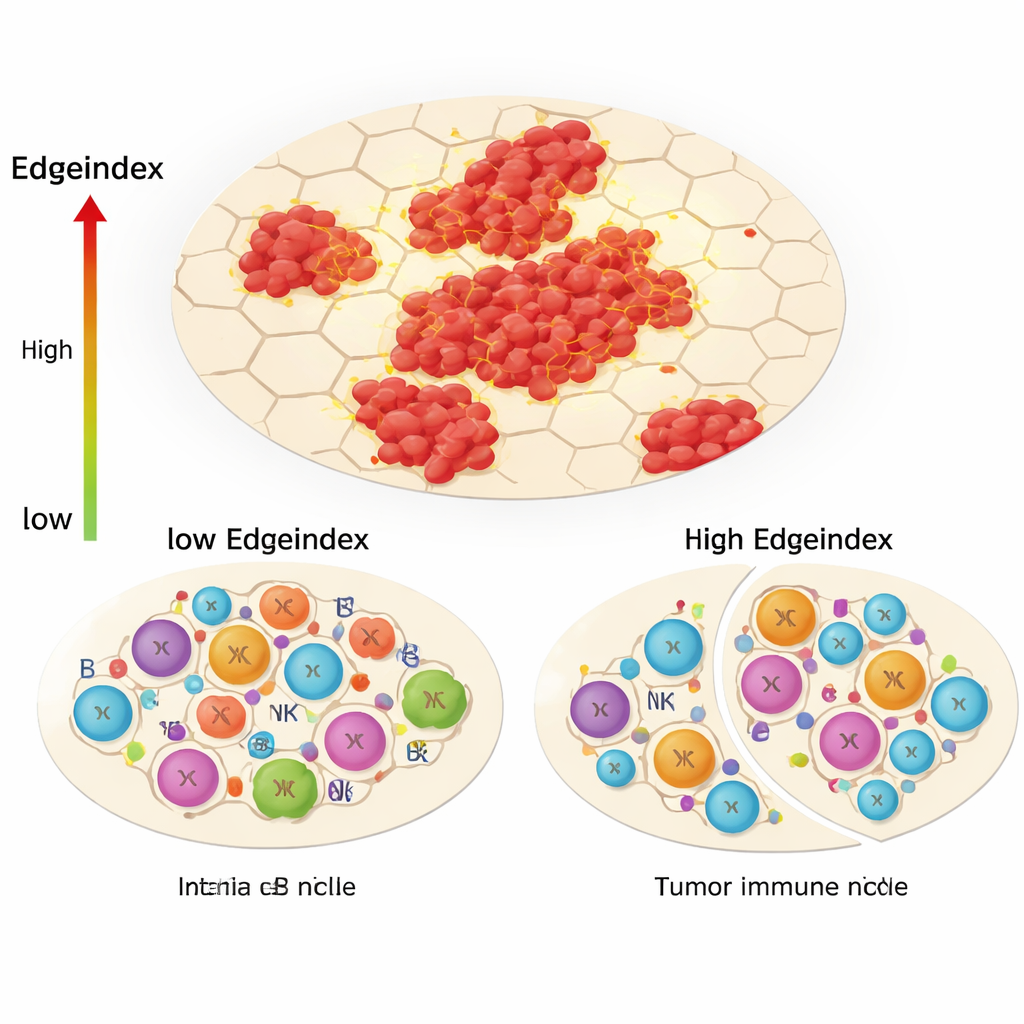
Ukryta różnorodność w obrębie i wokół guzów
Poza podtypami i wzorcami naciekania, dane przestrzenne ujawniły, że zarówno populacje komórek nowotworowych, jak i ich otaczające mikrośrodowiska są wewnętrznie zróżnicowane. Poprzez grupowanie punktów wewnątrz każdego guza zespół policzył, ile odrębnych „sąsiedztw” ekspresji genów istniało w obszarach nowotworowych i w pobliskiej tkance nie‑nowotworowej. Wyższa różnorodność wewnątrz guza wiązała się ze szlakami związanymi z odpowiedzią immunologiczną, podczas gdy określone wzorce w tkance otaczającej łączyły się z aktywnością cyklu komórkowego i regulacją genetyczną. Badacze zbadali także, jak silnie różne regiony „komunikują się” za pomocą znanych cząsteczek sygnałowych. Guzy z intensywniejszą komunikacją między regionami wykazywały silniejsze sygnały immunologiczne, co wzmacnia pogląd, że aktywność immunologiczna i wzrost guza są ściśle splecione w przestrzeni.
Śledzenie rozwoju guza w czasie
Aby przybliżyć, jak komórki nowotworowe zmieniają się w miarę postępu choroby, zespół przeprowadził analizę „pseudoczasu”, która porządkuje komórki wzdłuż ścieżki rozwojowej na podstawie ich aktywności genowej. W próbkach wielokrotnie identyfikowano jeden gen, UCHL1, jako centralny dla tych trajektorii. Wysokie poziomy UCHL1 zbiegały się z silną aktywnością cyklu komórkowego w punktach nowotworowych, podczas gdy niższe poziomy korelowały ze szlakami związanymi z odpowiedzią immunologiczną i śmiercią komórek. Ponieważ UCHL1 to białko typu neuronalnego wcześniej powiązane z agresywnymi nowotworami płuc, wyniki te wzmacniają hipotezę, że może to być użyteczny cel terapeutyczny, szczególnie dla komórek o cechach neuroendokrynnych napędzających drobnokomórkowy rak płuca.
Co to oznacza dla pacjentów
Mówiąc prosto, to badanie przekształca płaskie preparaty mikroskopowe drobnokomórkowego raka płuca w bogate, warstwowe mapy pokazujące, gdzie leżą różne podtypy nowotworu, jak agresywnie naciekają, jak komunikują się z otoczeniem i jak układ odpornościowy reaguje lub zawodzi. Nowy wskaźnik Edgeindex i podejście mapowania wskazują, które guzy są szczególnie naciekające i które komórki odpornościowe są obecne lub brakują na granicy. Powiązanie tych wzorców przestrzennych ze słabościami specyficznymi dla podtypów — takimi jak leki celujące w DLL3, BCL‑2, AURKA, IGF‑1R/PARP czy punkty kontrolne układu odpornościowego — przybliża pole do dopasowania każdego pacjenta do spersonalizowanej strategii leczenia. Chociaż narzędzia te wymagają jeszcze walidacji w większych badaniach, oferują plan działania dla bardziej precyzyjnych i potencjalnie skuteczniejszych terapii w typie nowotworu, który pilnie potrzebuje lepszych opcji.
Cytowanie: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Słowa kluczowe: drobnokomórkowy rak płuca, transkryptomika przestrzenna, heterogeniczność guza, mikrośrodowisko immunologiczne guza, onkologia precyzyjna