Clear Sky Science · pl
Rozszyfrowanie przerzutów do mózgu w raku jajnika o cechach nabłonkowych: analiza multimodalna i potencjalne markery
Dlaczego te badania są ważne
Rak jajnika jest już chorobą groźną, ale u niewielkiej liczby kobiet pojawia się później w znacznie bardziej wrażliwym miejscu: w mózgu. Te przerzuty do mózgu są rzadkie, lecz często śmiertelne, a lekarze wciąż mają niewiele sposobów, by przewidzieć, kto jest narażony, albo jak najlepiej je leczyć. Badanie to śledzi tę drogę od miednicy do mózgu na poziomie molekularnym, wykorzystując nowoczesne narzędzia DNA i RNA, aby zrozumieć, jak nowotwory jajnika adaptują się do mózgu i wskazać wczesne sygnały ostrzegawcze, które pewnego dnia mogłyby poprowadzić do bardziej spersonalizowanej opieki.
Od powszechnego nowotworu do rzadkiego zagrożenia mózgowego
Rak jajnika o budowie nabłonkowej jest najgroźniejszym nowotworem ginekologicznym w krajach rozwiniętych. Większość pacjentek początkowo reaguje na operację i chemioterapię, ale około 80 procent ostatecznie doświadcza nawrotu i lekooporności. Wznowy zwykle ograniczają się do jamy brzusznej; tylko niewielka część kobiet rozwija odległe przerzuty, np. do mózgu. W miarę poprawy leczenia i dłuższego przeżycia pacjentek pojawia się jednak więcej czasu na to, by wędrujące komórki nowotworowe zagnieździły się w mózgu, i lekarze obserwują takie przerzuty częściej. Gdy przerzuty do mózgu się pojawiają, typowy czas przeżycia spada poniżej roku, co podkreśla potrzebę zrozumienia, jak i dlaczego dochodzi do tego zjawiska.
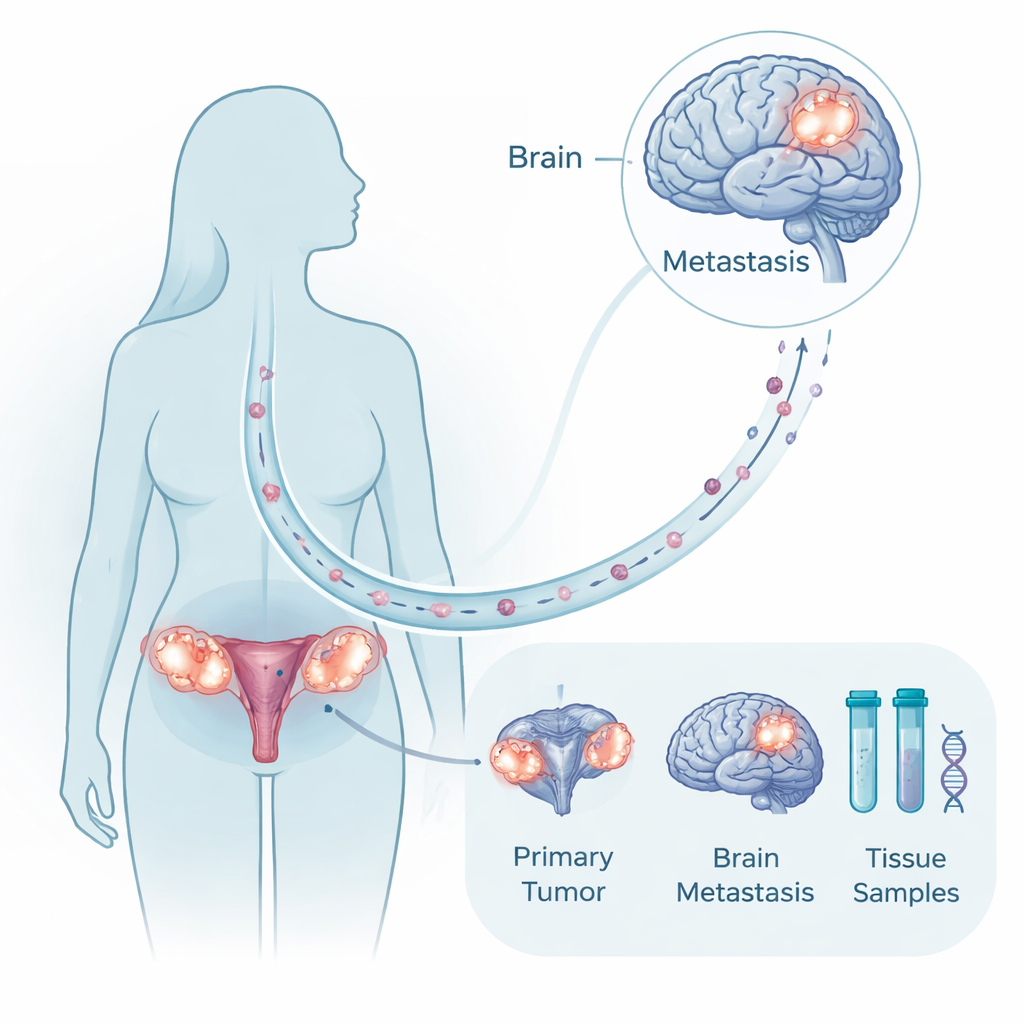
Rzadkie, lecz wartościowe zgromadzenie tkanek
Ponieważ operacja mózgu nie jest możliwa ani wskazana u wielu pacjentek, rzadko dysponuje się próbkami guza zarówno z pierwotnej masy jajnikowej, jak i z odpowiadającego jej przerzutu mózgowego u tej samej kobiety. Badacze zgromadzili dokładnie taki sparowany materiał od dziesięciu pacjentek leczonych przez dwie dekady oraz próbki porównawcze z zdrowego mózgu i jajnika oraz z innych, nie-mózgowych przerzutów. Analizowali DNA guzów pod kątem mutacji i dużych zmian chromosomalnych oraz profili RNA, aby zobaczyć, które geny są włączone, a które wyciszone. To multimodalne podejście pozwoliło im zapytać, czy guzy mózgowe są całkowicie nowymi odgałęzieniami, czy blisko spokrewnionymi kuzynami guza pierwotnego, oraz które programy molekularne ulegają zmianie, gdy komórki osiedlają się w mózgu.
Stabilność genetyczna, ale nowe zachowania
Analiza DNA wykazała, że pierwotne guzy jajnika i odpowiadające im przerzuty do mózgu były zadziwiająco podobne. Oba miały wiele tych samych mutacji napędzających nowotwór, zwłaszcza w genie TP53, i wykazywały ogólnie „monoklonalne” pochodzenie, co oznacza, że zmiany w mózgu wydają się pochodzić od tej samej komórki przodkowej. Duże zyski i utraty fragmentów DNA były nieco częstsze w zmianach mózgowych, ale nie dominowały obrazu. Sugeruje to, że to nie nabycie zupełnie nowego zestawu mutacji umożliwia rozsiew do mózgu. Krytyczna zmiana zachodzi raczej na poziomie aktywności genów — które instrukcje są odczytywane z DNA i wykorzystywane przez komórki nowotworowe, gdy adaptują się do unikalnego środowiska mózgu.
Jak guzy jajnika uczą się żyć w mózgu
Gdy zespół porównał aktywność genów we wszystkich tkankach, wyłonił się odrębny sygnaturowy wzorzec związany z przerzutami do mózgu. Zmiany mózgowe wykazywały cechy agresywnego wzrostu, z aktywacją programów cyklu komórkowego napędzanych przez znanych regulatorów nowotworowych, takich jak MYC i E2F. Zmieniały też białka tworzące i przebudowujące zrąb tkankowy, co pomaga komórkom w inwazji i zakotwiczeniu się w istocie mózgu. Uderzające było włączenie się niektórych genów powiązanych z komórkami nerwowymi i glejowymi, co sugeruje, że komórki raka jajnika częściowo naśladują komórki mózgu, by się w nim osadzić. Wśród najbardziej godnych uwagi znalazły się AFP, zwykle aktywne w płodzie i w niektórych nowotworach, oraz GFAP, charakterystyczne białko komórek wspierających w mózgu. Autorzy zidentyfikowali także niewielki zestaw genów już podwyższonych w pierwotnych guzach jajnika u kobiet, które później rozwinęły przerzuty do mózgu, ale nie u długoterminowych ozdrowieńców bez zajęcia mózgu. Ten „przodujący” wzorzec obejmował modulację układu odpornościowego, komunikację z sygnałami przypominającymi nerwowe oraz zmiany w metabolizmie.
Wczesne sygnały i molekularna rozmowa
Zagłębiając się dalej, badacze skupili się na cząsteczkach znajdujących się na powierzchni komórek lub wydzielanych, ponieważ są one naturalnymi kandydatami do badań krwi lub terapii. Wskazali trzy czynniki — MET, GDF15 i S100A9 — które były konsekwentnie podwyższone zarówno w pierwotnych guzach skierowanych do mózgu, jak i w samych przerzutach mózgowych. Molekuły te biorą udział w ruchu komórek, reagowaniu na stres i sensingu składników odżywczych oraz kształtowaniu środowiska immunologicznego, co sugeruje, że pomagają komórkom raka jajnika komunikować się z tkanką mózgową i przekształcać ją na swoją korzyść. Wraz z AFP i GFAP tworzą one krótką listę potencjalnych markerów, które w przyszłości mogłyby wskazywać pacjentki wysokiego ryzyka lub naprowadzać na leki przerywające komunikację między guzem a mózgiem.
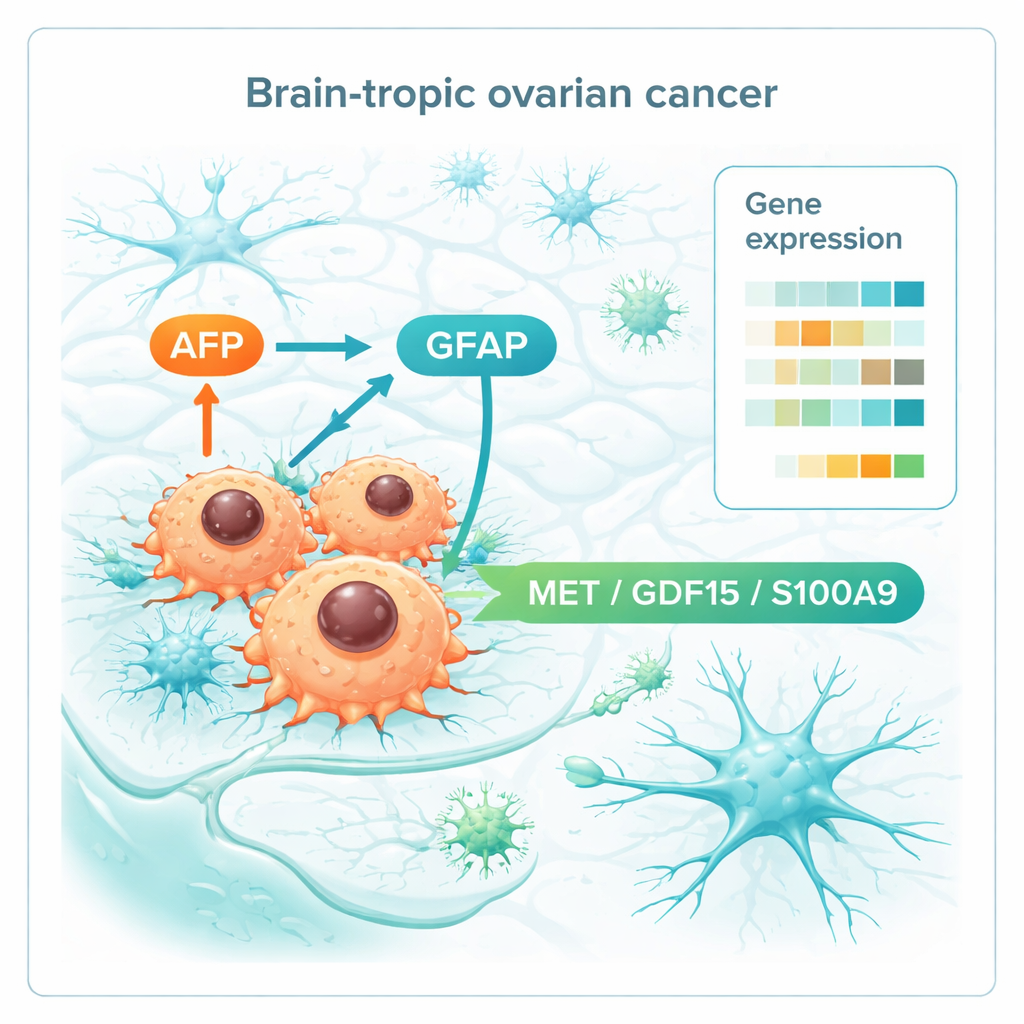
Co to oznacza dla pacjentek
Na razie ta praca nie zmieni od razu leczenia, a autorzy przyznają, że ich grupa pacjentek jest niewielka. Mimo to wykazując, że raki jajnika dające przerzuty do mózgu zachowują dużą część swojego pierwotnego składu genetycznego, jednocześnie przestawiając sposób wykorzystania genów, badanie wskazuje nowe drogi wczesnego wykrywania zagrożeń. Jeśli przyszłe badania potwierdzą, że markery takie jak AFP, GFAP, MET, GDF15 i S100A9 wiarygodnie sygnalizują skłonność do rozprzestrzeniania się do mózgu, lekarze mogliby baczniej monitorować wybrane pacjentki, modyfikować wybory terapeutyczne lub testować leki blokujące te szlaki. W istocie badanie zaczyna przekształcać przerażające późne powikłanie w proces, który można zmierzyć, zrozumieć i w końcu powstrzymać.
Cytowanie: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Słowa kluczowe: rak jajnika, przerzuty do mózgu, markery, ekspresja genów, onkologia precyzyjna