Clear Sky Science · pl
Oś STAT3-ANGPT2-PTGIS napędzana przez adipocyty promuje przerzuty do skóry w raku piersi i stanowi podatną na terapię ścieżkę
Dlaczego rozsiew do skóry w raku piersi ma znaczenie
Gdy rak piersi się rozprzestrzenia, większość osób myśli o kościach, wątrobie czy płucach. Tymczasem u wielu pacjentów nowy guz pojawia się w nieoczekiwanym miejscu: na skórze klatki piersiowej, czasem lata po usunięciu pierwotnego guza. Te uporczywe, bolesne guzki skórne to nie tylko problem estetyczny — są oznaką agresywnej choroby trudnej w leczeniu. Badanie wyjaśnia, dlaczego niektóre raki piersi mają skłonność do osiedlania się w skórze, ujawniając zaskakujące współdziałanie między komórkami nowotworowymi, pobliską tkanką tłuszczową oraz naczyniami krwionośnymi i limfatycznymi odżywiającymi guzy.
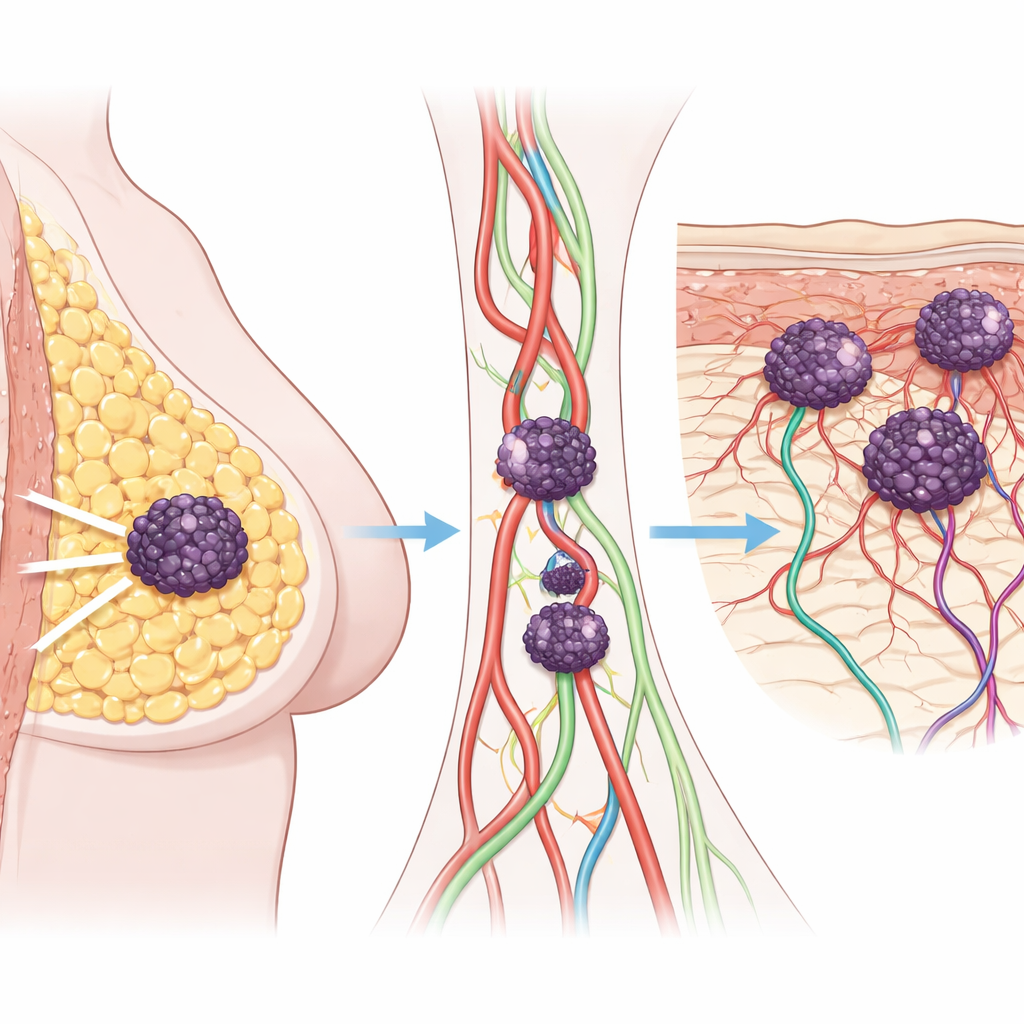
Guzy skórne jako sygnał ostrzegawczy
Naukowcy najpierw przeanalizowali dokumentację medyczną 126 osób z rakiem piersi, porównując pacjentów, którzy nigdy nie mieli nawrotu, tych, u których choroba rozprzestrzeniła się do narządów takich jak płuca czy kości, oraz tych, którzy rozwinęli przerzuty skórne. Pacjenci, u których choroba powróciła wyłącznie w skórze, już przy rozpoznaniu mieli bardziej zaawansowane i szybko rosnące guzy. Ich nowotwory wykazywały wysokie tempo podziałów komórkowych i wczesne naciekanie naczyń krwionośnych oraz limfatycznych. Nawet jeśli u części tych pacjentów nie stwierdzono widocznych przerzutów odległych, ich przeżycie ogólne i bezobjawowe choroby było gorsze niż u pacjentów bez zajęcia skóry, co podkreśla, że przerzuty skórne oznaczają szczególnie agresywną postać raka piersi.
Naczynia krwionośne i tłuszcz kształtują niszę skórną
Aby zrozumieć, co czyni skórę tak żyznym środowiskiem, badacze śledzili jednego pacjenta przez kilka lat, pobierając próbki z pierwotnego guza piersiowego i późniejszych guzków skórnych. Pod mikroskopem zarówno zmiany w piersi, jak i w skórze były wypełnione nowo powstałymi naczyniami krwionośnymi i limfatycznymi — maleńkimi autostradami, które ułatwiają komórkom nowotworowym przemieszczanie się i osiedlanie. Profilowanie aktywności genów wykazało, że w miarę postępu choroby guzy włączały całe sieci związane z tworzeniem naczyń, stanem zapalnym oraz metabolizmem tłuszczów i kwasów tłuszczowych. W szczególności intensyfikowały się szlaki rozkładu powszechnych tłuszczów pokarmowych, takich jak kwasy arachidonowy i linolowy, co sugeruje, że paliwo z tłuszczu oraz własne warstwy tłuszczowe skóry pomagają napędzać ewolucję guza.
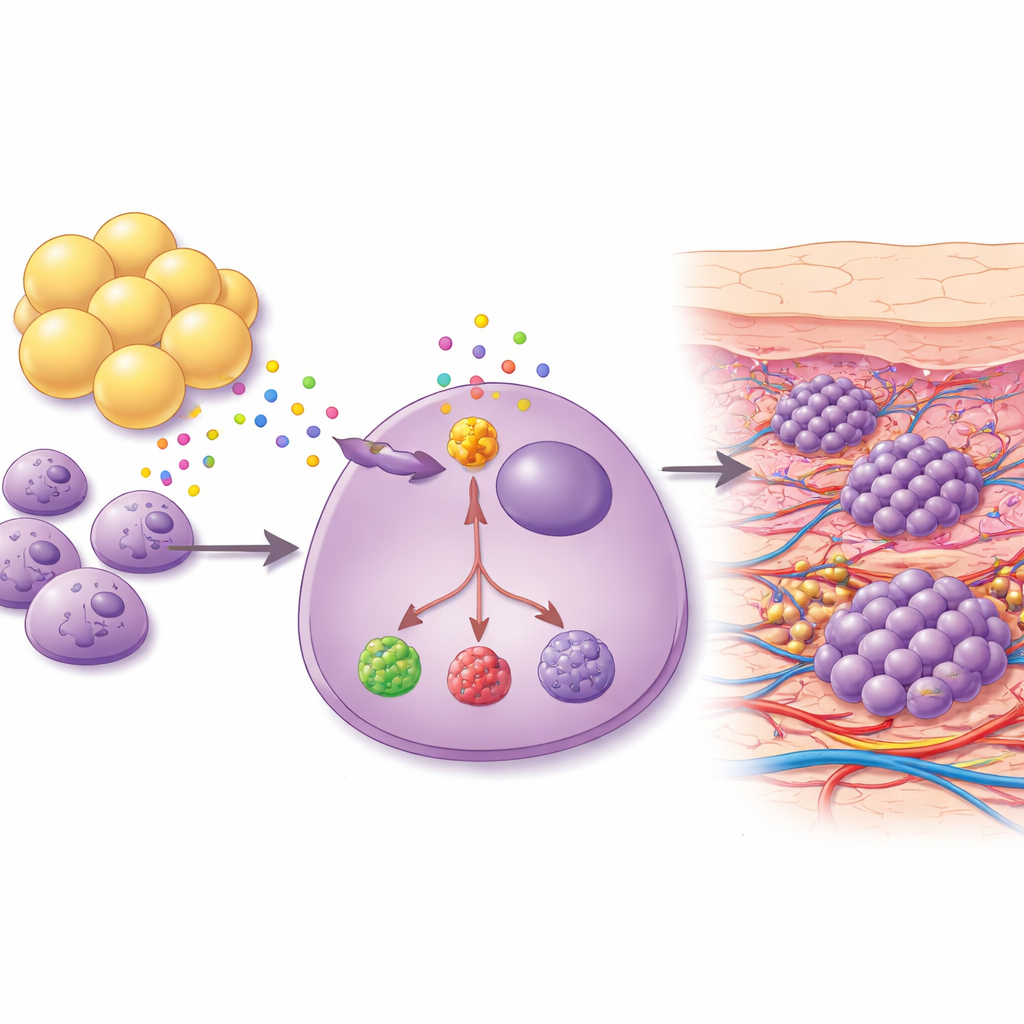
Komórki tłuszczowe wysyłają silne sygnały wzrostowe
Ponieważ pierś i leżąca poniżej ściana klatki piersiowej są bogate w tłuszcz, naukowcy zastanawiali się, czy same adipocyty mogą skłaniać komórki nowotworowe do osiedlania się w skórze. Hodowali komórki raka piersi razem z adipocytami — dojrzałymi komórkami tłuszczowymi pochodzącymi od tego samego pacjenta — i zbierali mieszaninę cząsteczek uwalnianych przez te komórki tłuszczowe. Ten koktajl silnie zwiększał zdolność komórek śródbłonka do tworzenia struktur przypominających rurki w warunkach laboratoryjnych, co jest cechą angiogenezy. W modelach mysich ekspozycja guzów na płyn pochodzący od adipocytów prowadziła do powstawania nowych ognisk nowotworu w obszarach bogatych w skórę i tłuszcz, takich jak kark czy grzbiet. Komórki nowotworowe pobrane z tych zmian skórnych miały cechy bardziej przypominające komórki macierzyste, były bardziej odporne na śmierć komórkową i wytwarzały wyższe poziomy czynników pro-wzrostowych i prozapalnych, w tym białka o nazwie ANGPT2 oraz enzymu metabolicznego PTGIS.
Przełącznik sygnalizacyjny, który można wyłączyć
Badając mechanizmy głębiej, zespół porównał zwykłe komórki guza z ich odpowiednikami preferującymi skórę i odkrył, że powszechny szlak komunikacji wewnątrzkomórkowej — droga JAK–STAT — był silnie aktywowany, a szczególnie białko STAT3. Po włączeniu STAT3 działał jak główny regulator, zwiększając ANGPT2, VEGFC (czynnik napędzający wzrost naczyń limfatycznych) i PTGIS, wszystkie sprzyjające tworzeniu naczyń i przebudowie mikrośrodowiska guza. Blokada STAT3 lekiem o nazwie Stattic zmniejszała wzrost guzów skórnych u myszy i obniżała poziomy tych czynników. W próbkach pacjentów wysoka aktywność STAT3, ANGPT2 i PTGIS wiązała się z gorszym czasem wolnym od progresji i krótszym okresem bez choroby, a markery te były szczególnie podwyższone u pacjentów, u których przerzuty ograniczały się do skóry.
Co to oznacza dla pacjentów
Podsumowując, praca ukazuje przerzutowy rak piersi do skóry jako odrębną i niebezpieczną podgrupę napędzaną trójstronną interakcją między komórkami nowotworowymi, otaczającym tłuszczem i naczyniami odżywiającymi guzy. Sygnały z adipocytów aktywują STAT3 w komórkach nowotworowych, co z kolei zwiększa ANGPT2 i PTGIS oraz przekształca metabolizm kwasów tłuszczowych, czyniąc skórę przyjazną niszą dla osiedlania się i rozrastania guzów. Dla pacjentów oznacza to, że przerzuty skórne nie są po prostu „lokalnymi” nawrotami, lecz wskaźnikiem agresywnej biologii. Co budzi nadzieję, ta sama ścieżka, która napędza proces, może być także jego słabością: leki celujące w STAT3 lub kluczowe enzymy metaboliczne, takie jak PTGIS, mogą w przyszłości pomóc odciąć linie wsparcia umożliwiające rakowi piersi kolonizację skóry.
Cytowanie: Luo, CW., Ou-Yang, F., Chang, SJ. et al. Adipocyte-driven STAT3-ANGPT2-PTGIS axis promotes cutaneous metastasis in breast cancer and represents a targetable pathway. npj Precis. Onc. 10, 111 (2026). https://doi.org/10.1038/s41698-025-01184-1
Słowa kluczowe: przerzuty raka piersi do skóry, mikrośrodowisko guza, sygnalizacja adipocytów, szlak STAT3, angiogeneza