Clear Sky Science · pl
Metody randomizowanej, zaślepionej, kontrolowanej oceny potencjalnych interwencji w chorobach w wielolaboratoryjnych sieciach przedklinicznych
Dlaczego to ma znaczenie dla codziennego zdrowia
Wiele obiecujących terapii medycznych wygląda na skuteczne w badaniach na zwierzętach, a następnie zawodzi w dużych, kosztownych badaniach klinicznych. Artykuł pokazuje, w konkretnych szczegółach, jak naukowcy mogą przeprojektować wczesne testy na zwierzętach, aby ich wyniki były bardziej wiarygodne i lepiej przewidywały, co stanie się u prawdziwych pacjentów — jako przykład posłużył udar. 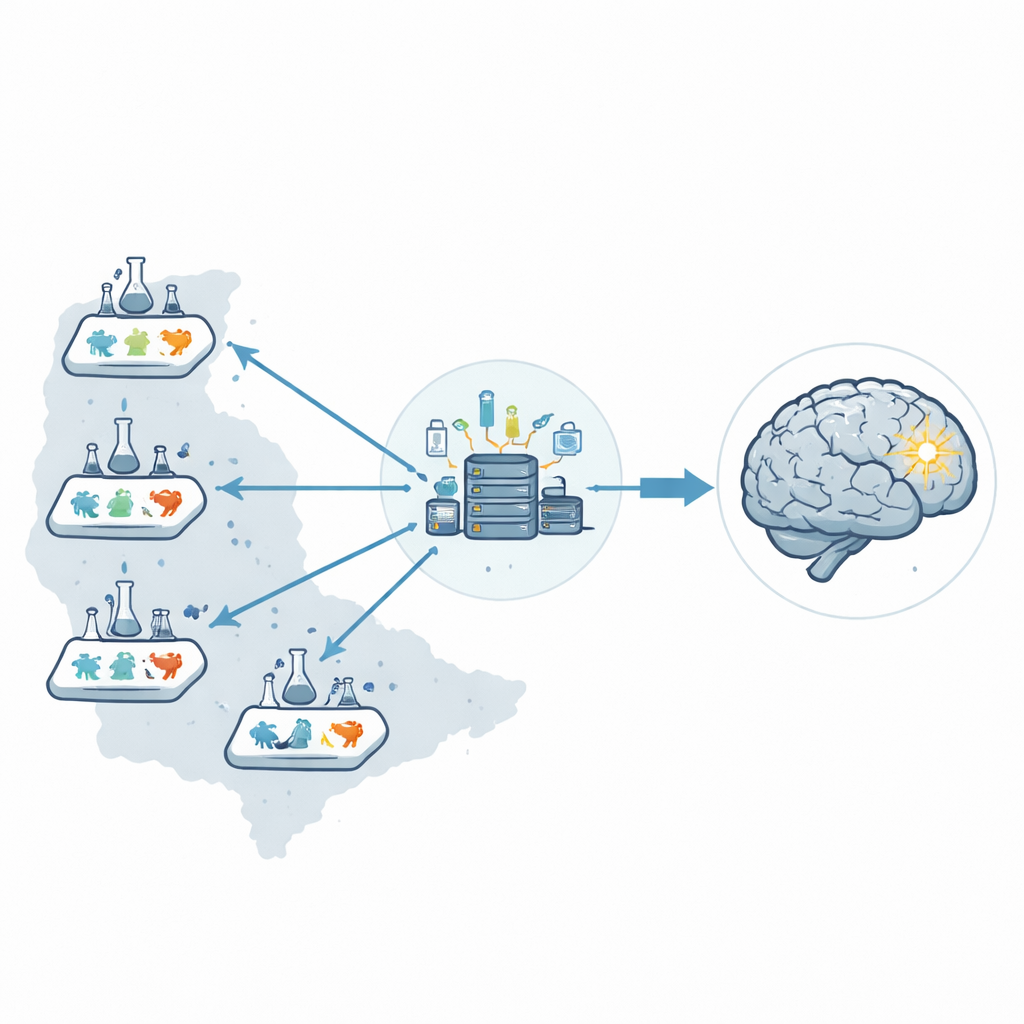
Budowanie sieci zamiast pojedynczego laboratorium
Zamiast polegać na jednym laboratorium, badacze stworzyli sześciolaboratoryjną sieć przedkliniczną w Stanach Zjednoczonych, nazwaną Stroke Preclinical Assessment Network. Centralne centrum koordynacyjne zarządzało całym przedsięwzięciem: wysyłaniem zakodowanych fiolek z lekami, losowym przydziałem terapii, odbiorem wszystkich danych i prowadzeniem analiz statystycznych. Oddzielając te role od osób przeprowadzających operacje czy oceniających wyniki, zmniejszyli ryzyko, że ludzkie oczekiwania subtelnie wpłyną na wyniki.
Wprowadzanie uczciwości i ukrycia w praktyce
Aby naśladować zasady dobrego badania klinicznego, każde zwierzę było rejestrowane, identyfikowane i śledzone od momentu przybycia do laboratorium. Terapie były ukryte w identycznych fiolkach, aby chirurdzy nie mogli odróżnić prawdziwych leków od placebo podczas indukowania udaru i podawania terapii. Ustrukturyzowany plan randomizacji zapewniał, że samce i samice, różne modele udaru oraz wszystkie sześć ośrodków wnosiły równy wkład do każdej grupy terapeutycznej. Nawet jeśli zwierzę umarło lub procedura się nie powiodła, pozostało w dokumentacji, tak by straty nie mogły zostać cicho pominięte, co pomagało unikać ukrytych uprzedzeń.
Testowanie terapii w realistycznych modelach udaru
Sieć stosowała pięć różnych modeli gryzoni, które łącznie odzwierciedlały istotne aspekty ludzkiego udaru, w tym wiek, nadciśnienie i otyłość indukowaną dietą. Udar wywoływano w ten sam sposób we wszystkich ośrodkach — krótkotrwale blokując główną tętnicę mózgu, a następnie przywracając przepływ krwi — podobnie do nowoczesnych procedur usuwania skrzeplin u ludzi. Zwierzęta otrzymywały jedną z sześciu badanych terapii ochronnych lub odpowiadający jej kontrolny preparat. Następnie śledzono je za pomocą prostych testów ruchowych, takich jak skręcanie w rogu czy chodzenie po kratownicy, oraz badań obrazowych mózgu mierzących wielkość uszkodzenia przez 30 dni.
Zaślepiona ocena, wspólne dane i inteligentna statystyka
Aby zachować bezstronność ocen, testy zachowania nagrywano na wideo i przesyłano do centralnego archiwum. Te filmy, pozbawione jakichkolwiek danych identyfikujących, przesyłano do wyszkolonych oceniajacych w innych laboratoriach, którzy punktowali je nie wiedząc, którą terapię otrzymało zwierzę ani gdzie było testowane. Obrazy rezonansu magnetycznego przetwarzano w zautomatyzowanym procesie analizy, który segmentował mózg i obszar uszkodzenia przy minimalnym udziale człowieka. Wszystkie wyniki zasilały wieloramienny, wieloetapowy projekt statystyczny, który pozwalał testować kilka terapii równolegle: słabe lub wyraźnie nieskuteczne kandydatury można było odrzucić wcześnie, podczas gdy obiecujące kontynuowały dalsze etapy. 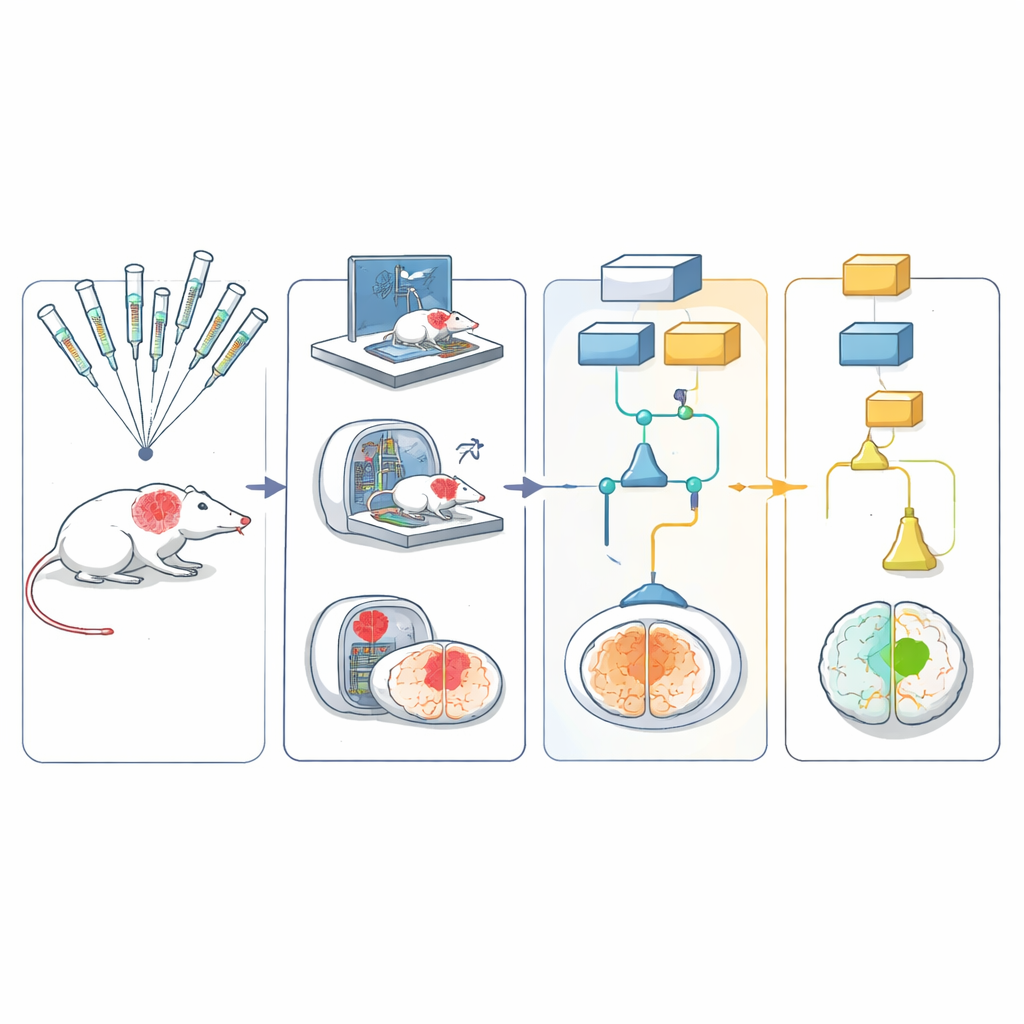
Co wyniki pokazały o terapiach udarowych
W czterech etapach i na 2 615 zwierzętach system okazał się wykonalny nawet podczas zakłóceń związanych z pandemią COVID-19. Metody konsekwentnie utrzymywały równowagę między grupami leczonymi, minimalizowały błędy w dawkowaniu i wykazywały poprawę jakości danych w miarę zdobywania doświadczenia przez ośrodki. Ostatecznie pięć z sześciu terapii zostało odrzuconych, podczas gdy jedna — kwas moczowy, wychwytujący wolne rodniki — spełniła wcześniej zaplanowane kryteria korzyści. Jednocześnie praca ujawniła ograniczenia niektórych popularnych modeli, na przykład bardzo wysokie wskaźniki śmiertelności u starych myszy, co sugeruje, że mogą one być niepraktyczne lub nierealistyczne dla przyszłych badań.
Szeroki obraz: wzorzec dla bardziej wiarygodnej nauki przedklinicznej
Dla czytelnika niebędącego specjalistą kluczowe przesłanie jest takie, że to, jak testujemy terapie na zwierzętach, ma tak samo duże znaczenie jak to, co testujemy. Wprowadzając zabezpieczenia nowoczesnych badań klinicznych — randomizację, zaślepienie, pełne rozliczenie każdego osobnika i staranną statystykę — do badań na zwierzętach, ta sieć pokazuje, że wczesne badania mogą być jednocześnie bardziej rygorystyczne i bardziej efektywne. Szczegółowy podręcznik, który przedstawili, można zaadaptować do innych chorób, oferując drogę do wyników laboratoryjnych, które wytrzymują replikację i dają lekarzom, pacjentom oraz fundatorom większą pewność, że terapia rzeczywiście ma szansę zadziałać w praktyce klinicznej.
Cytowanie: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Słowa kluczowe: udar, badania przedkliniczne, modele zwierzęce, rzetelność badań, badania wieloośrodkowe