Clear Sky Science · pl
PiggyBac‑zależna transgeneza i knockouty CRISPR–Cas9 u ćmy woskowej, Galleria mellonella
Mały gąsienica o dużym potencjale medycznym
Wyobraź sobie testowanie nowych antybiotyków lub badanie groźnych zakażeń bez użycia myszy czy innych ssaków. Larwy ćmy woskowej, Galleria mellonella, wyłaniają się jako tani i etycznie korzystny substytut do takich eksperymentów. W tym badaniu autorzy pokazują, jak naukowcy zrobili znaczący krok naprzód, wyposażając te gąsienice w tego rodzaju narzędzia genetyczne, które uczyniły muszki owocowe i danio pręgowanymi tak potężnymi w badaniach biomedycznych.
Dlaczego ten owad ma znaczenie dla zdrowia ludzi
Larwy Galleria mellonella zaskakująco dobrze naśladują odpowiedzi organizmu ludzkiego na patogeny. Mogą być utrzymywane w temperaturze 37 °C — czyli w temperaturze ciała człowieka — i dają się zakażać szerokim spektrum istotnych medycznie bakterii i grzybów. Gdy chorują, ich ciała ciemnieją w procesie zwanym melanizacją, co daje badaczom widoczny wskaźnik stanu zdrowia. Jako bezkręgowce unikają wielu prawnych i etycznych przeszkód związanych z pracą na kręgowcach, a także są tanie w hodowli na dużą skalę. Stwierdzono nawet, że larwy te rozkładają niektóre powszechne tworzywa sztuczne, co sugeruje zastosowania także w badaniach środowiskowych.
Brakujący zestaw narzędzi genetycznych
Pomimo tych zalet, larwy ćmy woskowej nie miały dotąd zaawansowanych sztuczek genetycznych dostępnych w klasycznych modelach laboratoryjnych. W ciągu ostatniej dekady kilka zespołów zsekwencjonowało genom ćmy i skatalogowało aktywne geny oraz białka, lecz badaczom wciąż trudno było łatwo wyłączać lub włączać geny albo dodawać użyteczne markery. Ta luka ograniczała możliwości modelu — na przykład tworzenie zwierząt, które świecą po zakażeniu, albo usuwanie konkretnych genów, by sprawdzić ich rolę w odporności. Obecna praca podejmuje to wyzwanie, adaptując do Galleria mellonella dwa potężne systemy inżynierii genowej: PiggyBac i CRISPR–Cas9.
Tworzenie larw‑reporterów świecących w ciemności
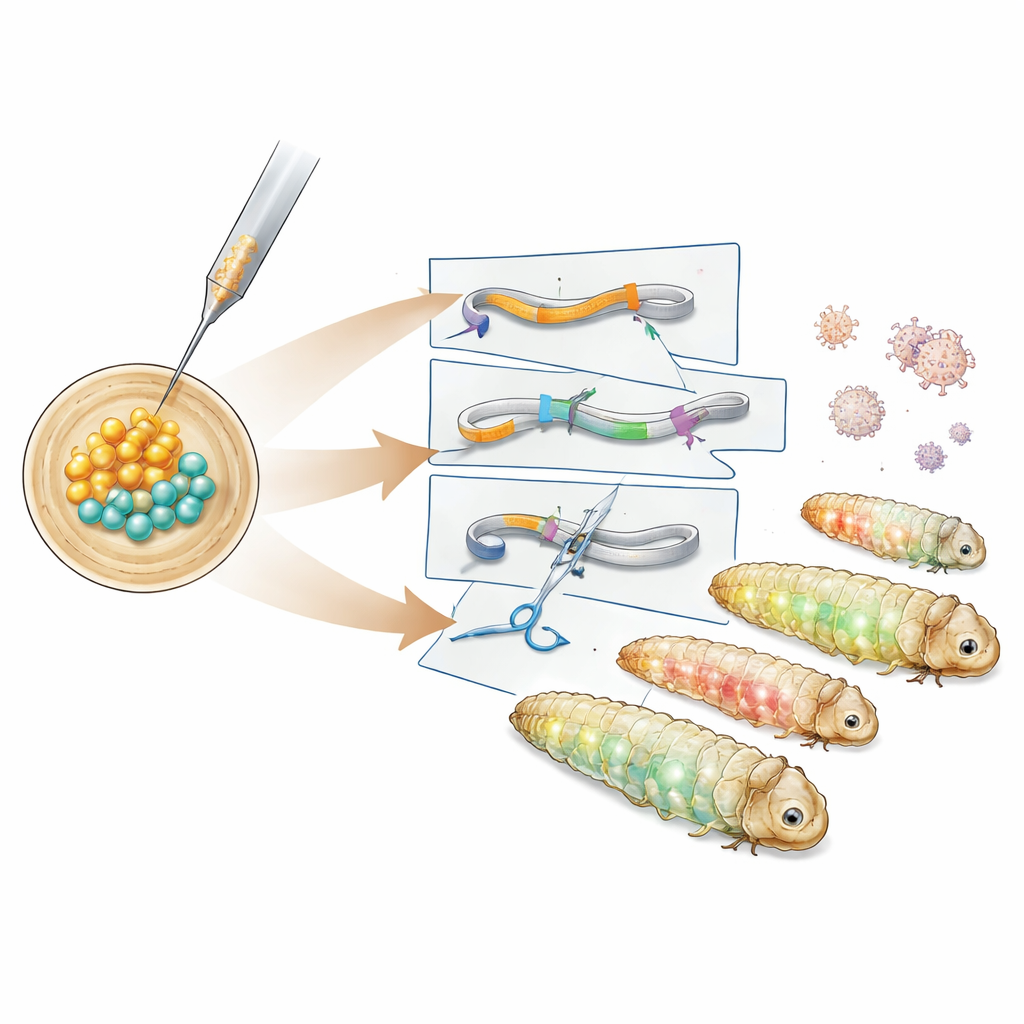
Zespół najpierw przeanalizował czasowy przebieg wczesnego rozwoju embrionalnego ćmy i wykrył mniej więcej sześciogodzinne okno po złożeniu jaj, kiedy wszystkie dzielące się jądra dzielą wspólną przestrzeń. Wstrzykiwanie DNA w tym okresie pozwala, by nowy materiał genetyczny trafił do wszystkich późniejszych tkanek, w tym przyszłych plemników i jaj. Wykorzystując to okno, badacze wprowadzili konstrukty DNA oparte na transpozonie PiggyBac — elemencie „wytnij‑i‑wklej”, który wstawia duże fragmenty DNA do genomu. Po przetestowaniu różnych plazmidów pomocniczych zidentyfikowali wersję zawierającą hiperaktywne białko PiggyBac, która skutecznie wygenerowała linie transgeniczne. Larwy te ekspresjonowały zielone i czerwone białka fluorescencyjne w różnych tkankach, a analiza DNA wykazała, że kaseta genetyczna wylądowała w niekolidującym fragmencie między rodzimymi genami.
Obserwacja komórek i wyłączanie genów
Następnie autorzy stworzyli bardziej wyspecjalizowane linie reporterowe. Jeden konstruktor znakował białko strukturalne tubulinę zieloną fluorescencją, by uwidocznić wewnętrzny szkielet komórki, podczas gdy inny łączył czerwony znacznik z histonem otaczającym DNA w jądrze. Linie te świeciły w charakterystycznych wzorcach w jelicie, tkance tłuszczowej, gruczołach jedwabnych i innych tkankach, pozwalając na wizualizację struktur komórkowych w żywych lub utrwalonych larwach. Aby pójść dalej niż tylko dodawanie genów i rzeczywiście je wyłączyć, zespół użył CRISPR–Cas9. Wstrzyknęli wstępnie zmontowane kompleksy białko–RNA CRISPR ukierunkowane na zielony marker fluorescencyjny do embrionów, które już nosiły kasetę reportera. Wielu potomków wykazało częściową lub całkowitą utratę zielonego sygnału przy zachowaniu czerwonej fluorescencji oczu, a sekwencjonowanie DNA potwierdziło drobne insercje i delecje w zamierzonym miejscu cięcia CRISPR.
Od postępu technicznego do praktycznego wpływu
Choć wydajność zarówno PiggyBac, jak i CRISPR w tych ćmach jest wciąż umiarkowana w porównaniu z niektórymi innymi owadami, autorzy proponują jasne drogi poprawy poprzez dostrajanie promotorów, wariantów enzymów i strategii wstrzykiwania. Nawet w obecnej formie zestaw narzędzi jest wystarczająco potężny, by tworzyć stabilne linie wizualizujące kluczowe elementy komórkowe lub zawierające celowane knockouty genowe. Dla osób spoza specjalności najważniejszy wniosek jest taki, że Galleria mellonella można teraz modyfikować niemal tak elastycznie jak lepiej znane zwierzęta laboratoryjne. Oznacza to, że badacze mogą tworzyć gąsienice raportujące o zakażeniu, modelować aspekty chorób ludzkich lub testować nowe leki w sposób szybszy, tańszy i bardziej humanitarny, co potencjalnie zmniejszy zależność od modeli ssaków w biologii infekcji i powiązanych dziedzinach.
Cytowanie: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Słowa kluczowe: Galleria mellonella, model infekcji bezkręgowców, inżynieria genetyczna, transgeneza PiggyBac, knockouty CRISPR