Clear Sky Science · pl
Celowanie w nowotworowo eksprymowany EGFR humanizowanym przeciwciałem monoklonalnym
Odnajdywanie ukrytych flag nowotworu
Terapie przeciwnowotworowe często mają trudność ze znalezieniem równowagi między atakiem na komórki guza a oszczędzaniem tkanek zdrowych. W tej pracy opisano nowe laboratoryjnie zaprojektowane przeciwciało, nazwane A10, które potrafi rozróżnić komórki nowotworowe noszące szczególną postać receptora sygnału wzrostu od komórek prawidłowych. Skupiając się na konformacji pojawiającej się głównie wtedy, gdy receptor jest zmieniony lub nadmiernie obecny na komórkach guza, A10 otwiera drogę do terapii zarówno silnych, jak i bardziej selektywnych niż wiele dotychczasowych opcji.
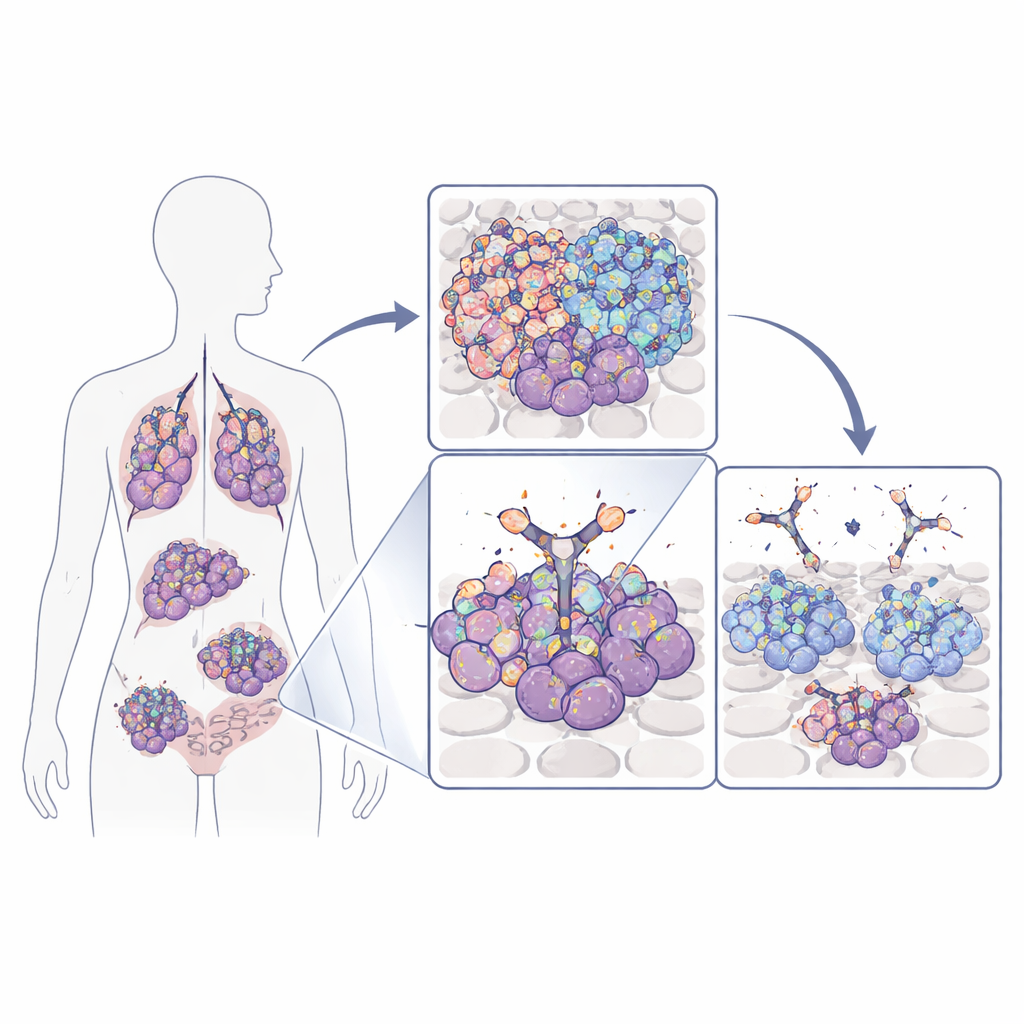
Dlaczego ten przełącznik wzrostu ma znaczenie
Wiele nowotworów, w tym agresywne nowotwory mózgu, płuc, piersi i okrężnicy, zależy od białka powierzchniowego zwanego receptorem naskórkowego czynnika wzrostu (EGFR), aby rosnąć i przetrwać. Komórki nowotworowe mogą zwiększać ilość tego receptora przez amplifikację genu, jego mutację lub wytwarzanie skróconej, ciągle aktywnej wersji zwanej EGFRvIII. Standardowe leki blokujące EGFR często trafiają zarówno w komórki nowotworowe, jak i w tkanki normalne, ponieważ rozpoznają fragmenty receptora obecne powszechnie. Zespół autorów tej pracy skoncentrował się zamiast tego na małej pętli EGFR, która staje się wyraźnie odsłonięta głównie na komórkach nowotworowych — albo dlatego, że EGFR występuje w nieprawidłowo dużej liczbie, albo dlatego, że receptor jest skrócony w EGFRvIII. Ta pętla działa jak nowotworowo‑specyficzna „flaga”, którą można w zasadzie celować znacznie bezpieczniej.
Przekształcanie mysiego przeciwciała w lek dla ludzi
Naukowcy wcześniej odkryli mysie przeciwciało, 40H3, które rozpoznawało tę odsłoniętą pętlę na EGFR eksprymowanym przez nowotwory. Mysie przeciwciała jednak mogą wywoływać reakcje immunologiczne przy powtarzalnym podawaniu pacjentom. Aby temu zapobiec, zespół zastosował metody inżynierii białek, przeszczepiając kluczowe segmenty wiążące 40H3 na ludzkie ramy przeciwciał, generując czternaście kandydatów „humanizowanych” oraz cząsteczkę referencyjną chimeryczną. Testując te warianty na komórkach nowotworowych nadprodukujących EGFR, trzy wersje wiązały się wyjątkowo dobrze, a jedna — A10 — wyróżniła się jako najsilniejszy binder, jednocześnie ignorując komórki normalne z umiarkowanymi poziomami EGFR. W szerokim panelu linii komórkowych nowotworowych o różnych mutacjach i liczbie kopii EGFR, A10 konsekwentnie wykazywała silniejsze wiązanie niż oryginalne mysie przeciwciało i utrzymywała wyraźne preferencje wobec komórek złośliwych.
Jak przeciwciało chwyta swój cel
Aby zrozumieć, dlaczego A10 jest tak selektywna, zespół wyznaczył strukturę 3D o wysokiej rozdzielczości aktywnej części przeciwciała związanej z pętlą EGFR. Pętla składa się w ciasny spinkowy kształt stabilizowany przez mostek disiarczkowy, a A10 obejmuje tę formę w rowku utworzonym między swoimi dwiema „ramionami”, z wieloma ładunkowymi kontaktami blokującymi ją na miejscu. Porównanie tej struktury ze znanymi kształtami pełnego białka EGFR ujawniło kluczową obserwację: zarówno w nieaktywnej, „związan ej” formie, jak i w aktywnej dimerowej formie normalnego EGFR pętla jest w dużej mierze ukryta lub częściowo osłonięta przez sąsiednie domeny. Oznacza to, że A10 nie ma łatwego dostępu do swojego miejsca wiązania na typowych receptorach wyrażanych w umiarkowanych ilościach. Natomiast w nowotworowo‑specyficznym wariancie EGFRvIII przednia część receptora jest usunięta, co pozostawia pętlę wysoko odsłoniętą i dostępną. Dane sugerują, że A10 rozpoznaje EGFR głównie w określonych przejściowych kształtach oraz w formach przeludnionych lub skróconych, które występują preferencyjnie na komórkach nowotworowych.
Uzbrajanie przeciwciała do zabijania komórek guza
Rozpoznanie nowotworowo‑specyficznej flagi jest samo w sobie użyteczne, lecz badacze poszli dalej, przekształcając A10 w koniugat przeciwciało‑lek (ADC). Chemicznie przyłączyli silnie cytotoksyczny związek, monometyl aurystatynę E (MMAE), do A10 przy użyciu łącznika, który może zostać przecięty wewnątrz komórek. Ten koniugat A10‑MMAE wiązał komórki nowotworowe równie dobrze jak niekonjugowane przeciwciało. W testach laboratoryjnych na wielu liniach komórkowych ADC był najbardziej skuteczny przeciwko nowotworom z bardzo wysokimi poziomami EGFR lub EGFRvIII, gdzie A10 miała obfite miejsca wiązania. W tych komórkach niewielkie ilości koniugatu wystarczały, by wywołać śmierć komórek. Linie nowotworowe z mniejszą liczbą celów dla A10 lub z wrodzoną odpornością na MMAE były mniej dotknięte, a normalne fibroblasty z dzikiego EGFR pozostały nienaruszone mimo wrażliwości na wolne MMAE. Wyniki pokazują, że połączenie selektywnego wiązania i wewnątrzkomórkowego uwolnienia leku może wyraźnie skupić toksyczność na komórkach nowotworowych.
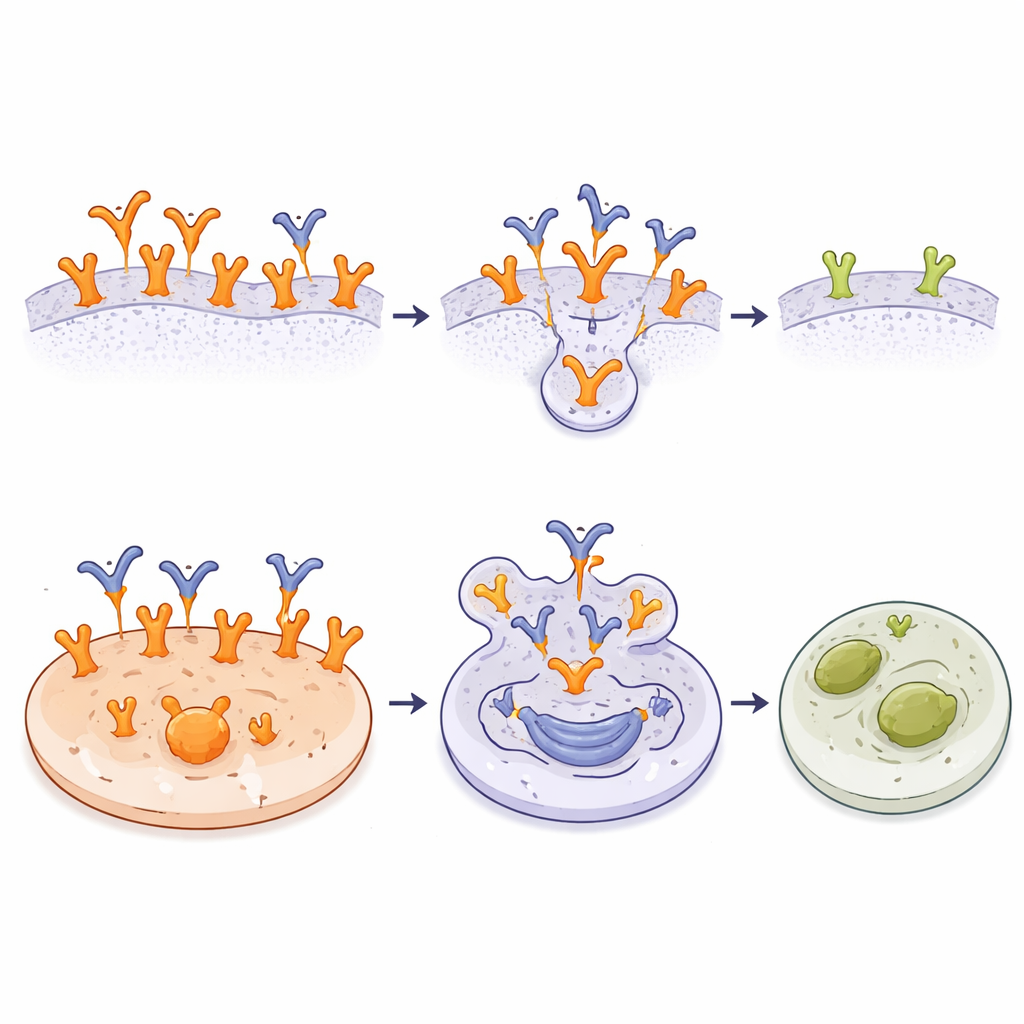
Co to może znaczyć dla przyszłej opieki onkologicznej
Mówiąc prosto, praca ta pokazuje, że możliwe jest zbudowanie przeciwciała, które „widzi” EGFR tylko wtedy, gdy wygląda i zachowuje się jak receptor napędzający nowotwór, jednocześnie w dużej mierze ignorując jego codzienną postać w tkankach zdrowych. Mapując dokładnie, jak A10 chwyta ukrytą pętlę na EGFR i demonstrując, że koniugat oparty na A10 może skutecznie zabijać komórki guza bogate w receptor, przy jednoczesnym oszczędzaniu komórek normalnych, badanie dostarcza solidnych podstaw do rozwoju bezpieczniejszych, wysoce ukierunkowanych terapii. Jeśli te wyniki przełożą się na pacjentów, przyszłe terapie oparte na A10 mogłyby dostarczać silne leki bezpośrednio do nowotworów zależnych od EGFR, pozostawiając resztę organizmu w dużej mierze nietkniętą.
Cytowanie: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Słowa kluczowe: EGFR, konjugat przeciwciało‑lek, ukierunkowana terapia przeciwnowotworowa, glejaki, EGFRvIII