Clear Sky Science · pl
Strukturalne i mechanistyczne spojrzenie na celowanie w integryny α2β1 i α5β1 za pomocą bioinżynieryjnych pęcherzyków zewnątrzkomórkowych pochodzących z komórek raka płuca
Ukryci posłańcy raka
Raka płuca często wykrywa się późno, gdy możliwości leczenia są ograniczone. Jednym z obiecujących sposobów walki z chorobą jest dostarczanie leków wyłącznie do komórek nowotworowych, oszczędzając tkanki zdrowe. W tym badaniu analizowano niewielki, naturalny system dostarczania—pęcherzyki zewnątrzkomórkowe (EV), których komórki nowotworowe już używają do przesyłania sygnałów. Poprzez przeprojektowanie tych pęcherzyków za pomocą krótkiego znacznika kierunkowego, badacze pokazują, jak mogą one przyłączać się do określonych miejsc dokujących na komórkach guza, tworząc podstawy do bardziej precyzyjnych i mniej toksycznych terapii przeciwnowotworowych.
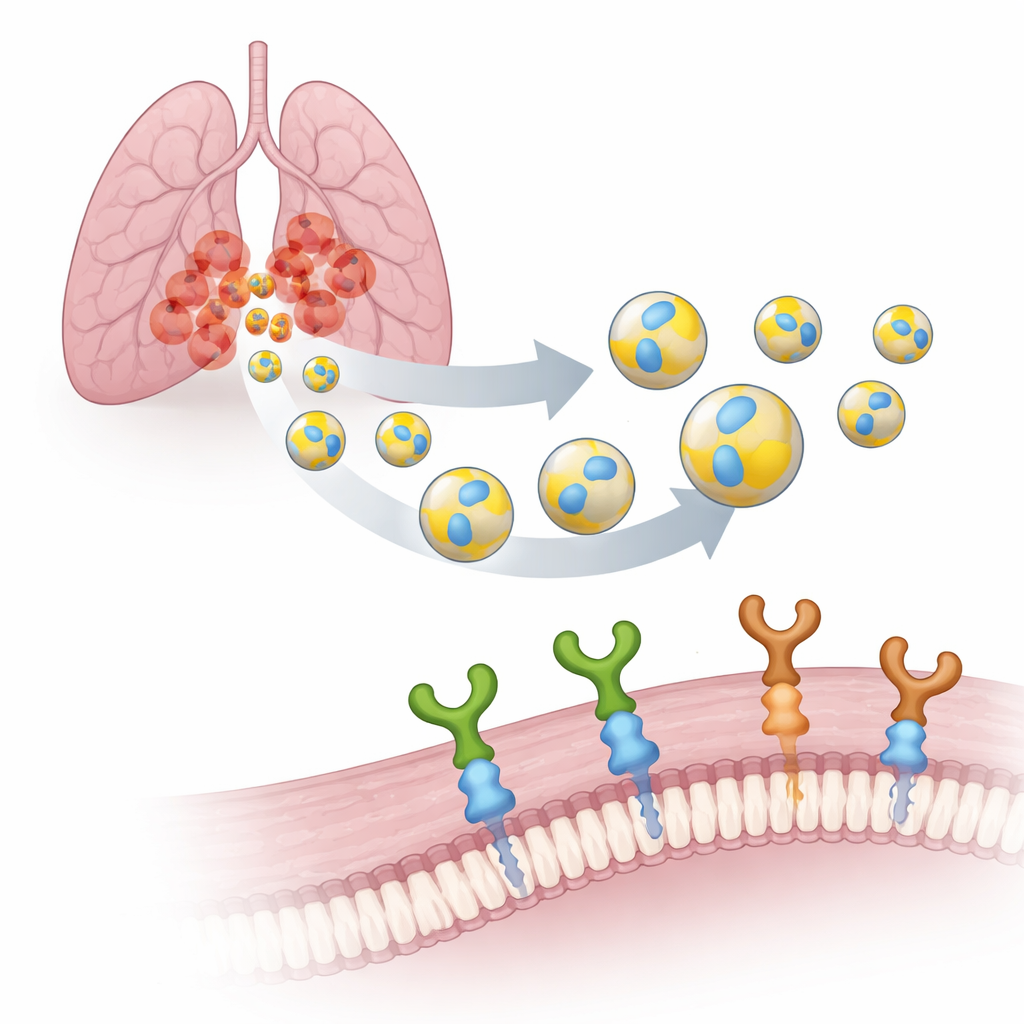
Przekształcanie naturalnych opakowań w inteligentnych kurierów
Każda komórka w naszym ciele uwalnia EV: nanoskala pęcherzyki otoczone błoną, nieco jak mikroskopijne bańki mydlane. Ponieważ powstają w naszych własnych komórkach, EV są biodegradowalne, łatwo przenikają bariery biologiczne i rzadziej wywołują skutki uboczne niż nośniki syntetyczne. Zespół skupił się na EV produkowanych przez ludzkie komórki raka płuca (A549) i udekorował ich powierzchnię małym siedmiowęzłowym znacznikiem o sekwencji PTHTRWA. Wcześniejsze eksperymenty wykazały, że ten znacznik kieruje EV do komórek raka płuca u myszy, wiążąc się znacznie silniej z komórkami nowotworowymi niż z normalnymi komórkami płuc, przy jednoczesnej niskiej toksyczności.
Znajdowanie właściwych portów dokujących na komórkach guza
Aby przekształcić te znakowane pęcherzyki w rzeczywiście ukierunkowane narzędzia, badacze musieli zidentyfikować, które „porty” na komórkach nowotworowych rozpoznają. Zbadali dwa spokrewnione receptory powierzchniowe, integryny α2β1 i α5β1. Są to molekularne haki, które pomagają komórkom przylegać do otoczenia i przekazywać sygnały do wnętrza. W rakach płuca α5β1 jest mocno powiązana z agresywnym przebiegiem choroby, przerzutami i gorszym przeżyciem, podczas gdy α2β1 łączona była z opornością na chemioterapię. Przy użyciu wrażliwej techniki rezonansu powierzchniowego zespół porównał, jak silnie EV z PTHTRWA wiążą się z obiema integrynami. Stwierdzili, że pęcherzyki bez znacznika prawie nie wchodziły w interakcje, natomiast znakowane EV tworzyły stabilne, mocne kompleksy z obiema cząsteczkami przy warunkach zbliżonych do fizjologicznych.
Przybliżenie na molekularne objęcie
Aby zrozumieć, co dzieje się atom po atomie, gdy znacznik spotyka integryny, badacze sięgnęli po symulacje komputerowe. Zbudowali trójwymiarowe modele znacznika związane z kluczowymi obszarami integryn i pozwolili tym układom ewoluować w wirtualnej wodzie przez setki nanosekund. Obliczenia wykazały, że PTHTRWA wpasowuje się ciasno w płytkie zagłębienie na receptorze α2β1, tworząc sieć wiązań wodorowych i kontaktów hydrofobowych, które stabilizują kompleks. Co istotne, wiązanie sprzyjało bardziej „otwartej” konformacji receptora—jego formie o wysokim powinowactwie i gotowej do sygnalizacji—w porównaniu z „zamkniętym” stanem spoczynkowym. Testując nieco zmodyfikowane wersje znacznika, zauważyli, że drobne chemiczne zmiany na jednym końcu mogą subtelnie przekształcić sposób, w jaki peptyd układa się w szczelinie i jak silnie preferuje jedną integrynę nad drugą.
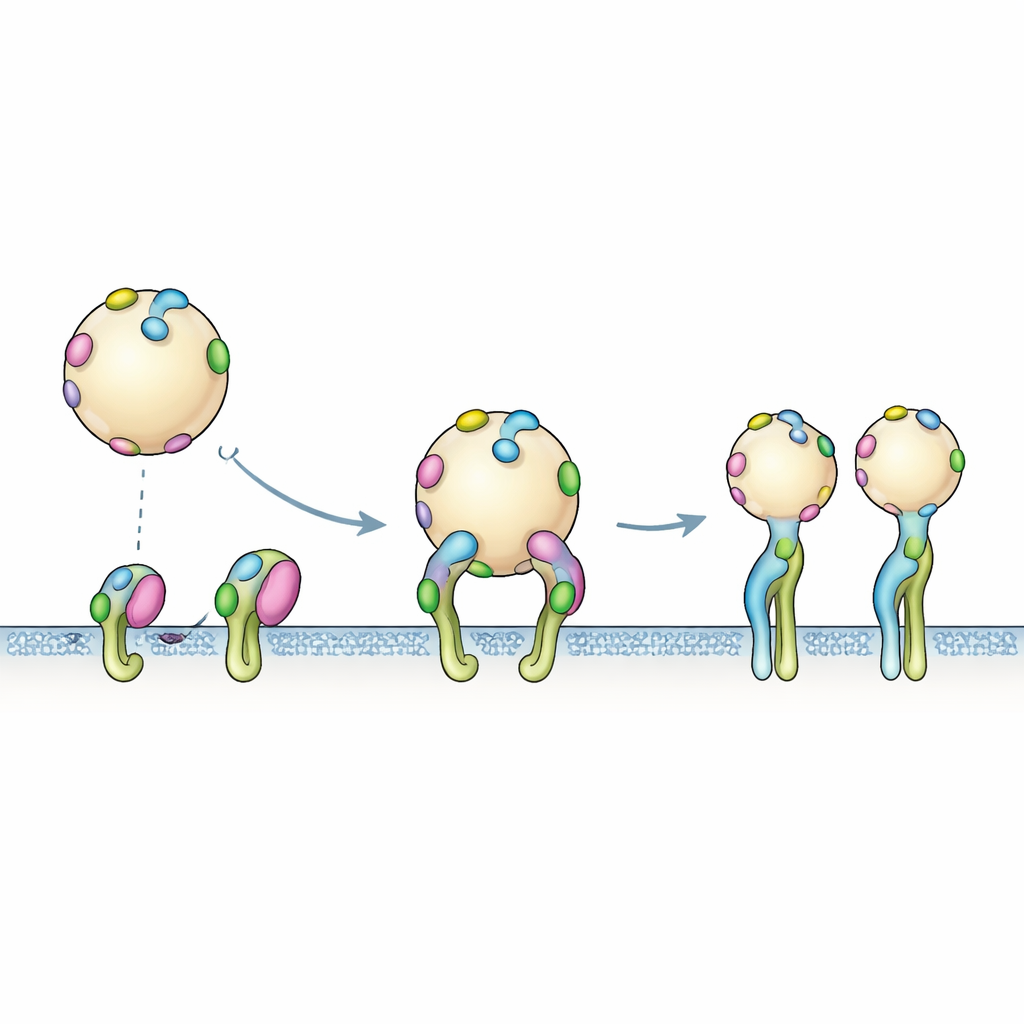
Od pojedynczych znaczników do wielowartościowego chwytu
Modele komputerowe oddają pojedynczy znacznik stykający się z jednym receptorem w danym momencie, lecz rzeczywista powierzchnia EV jest pokryta wieloma kopiami PTHTRWA. Eksperymenty wiążące odzwierciedlały tę wielowartościową rzeczywistość: gdy znakowany pęcherzyk zbliża się do pola integryn, wiele znaczników może zaangażować się jednocześnie. Dane z sensora najlepiej pasowały do procesu dwuetapowego. Najpierw pęcherzyk krótkotrwale dokuje poprzez szybkie, odwracalne kontakty. Następnie zachodzi wolniejsza reorganizacja, podczas której integryny przechodzą w otwartą konformację, a ogólny chwyt się wzmacnia. Ta kooperatywna, wieloręka spinka wyjaśnia, dlaczego pozorne powinowactwo całych pęcherzyków jest wyższe niż to, które przewidywałoby wiązanie pojedynczego znacznika.
Co to może znaczyć dla przyszłych terapii
Mówiąc wprost, badanie pokazuje, że EV uzbrojone w znacznik PTHTRWA mogą selektywnie rozpoznawać integryny nadaktywne w raku płuca i robią to, popędzając te receptory w kierunku otwartej, ściśle związanej formy. Mapując te interakcje w szczegółach, badacze dostarczają zasad projektowania dla kolejnej generacji nośników opartych na pęcherzykach, które mogłyby dostarczać leki, agenty obrazujące lub inne ładunki bezpośrednio do komórek nowotworowych, przy jednoczesnym minimalnym oddziaływaniu na tkanki zdrowe. Choć potrzebne są dalsze badania na zwierzętach i ludziach, ta strategia celowania w integryny przybliża wizję spersonalizowanej medycyny przeciwnowotworowej opartej na EV do praktycznej realizacji.
Cytowanie: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Słowa kluczowe: rak płuca, pęcherzyki zewnątrzkomórkowe, integryny, ukierunkowane dostarczanie leków, symulacje molekularne