Clear Sky Science · pl
Związek fluorochinolinowy wykazuje przeciw-erytroleukemiczne działanie poprzez podwójne celowanie w GLUT1 i szlak sygnałowy PI3K/AKT
Nowe spojrzenie na groźny nowotwór krwi
Erytroleukemia to rzadka, ale wyjątkowo agresywna postać nowotworu krwi, na którą poza przeszczepieniem komórek macierzystych dostępnych jest niewiele opcji leczenia. Dla wielu, zwłaszcza starszych pacjentów, oznacza to intensywne terapie, wysokie koszty i niekorzystne rokowania. W badaniu opisano laboratoryjnie zaprojektowany związek nazwany FKL-137, który atakuje komórki erytroleukemii w nieoczekiwany sposób: odcinając ich ulubione paliwo — cukier — i wywołując ich autodestrukcję. Praca sugeruje możliwą nową klasę leków ukierunkowanych, które wykorzystują zależność komórek nowotworowych od zmienionego wykorzystania energii, przy stosunkowo mniejszym uszkodzeniu zdrowych tkanek.
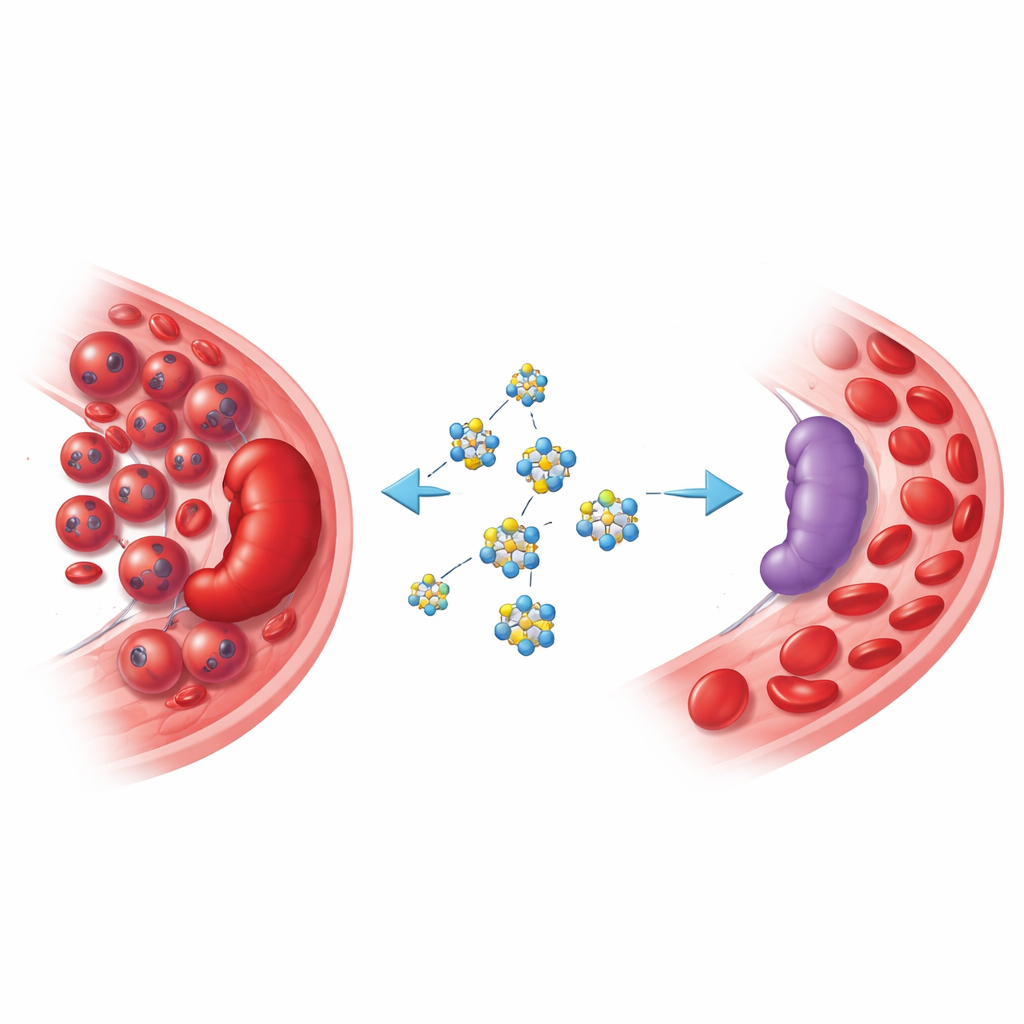
Gdy komórki krwi wymykają się spod kontroli
W erytroleukemii niedojrzałe prekursory czerwonych krwinek mnożą się w sposób niekontrolowany w szpiku kostnym i śledzionie. Pacjenci mogą rozwijać ciężką anemię, powiększenie śledziony obarczone ryzykiem pęknięcia oraz szybkie pogorszenie stanu zdrowia. Obecne terapie są ograniczone, a wielu chorych jest zbyt słabych na agresywne leczenie. Równocześnie naukowcy wykazali, że wiele nowotworów krwi polega na przeprogramowanym wykorzystaniu cukru: intensywnie pobierają glukozę i szybko przekształcają ją w energię oraz składniki budulcowe, co sprzyja ich namnażaniu i unikaniu układu odpornościowego. Atakowanie tej metabolicznej „uzależnienia” stało się atrakcyjną strategią dla nowych leków.
Głodzenie komórek nowotworowych ze względu na cukier
Naukowcy skupili się na małocząsteczkowym związku syntetycznym FKL-137, pochodzącym z rodziny chemicznej już znanej z aktywności przeciwnowotworowej. W eksperymentach laboratoryjnych wystawili dwie ludzkie linie komórek erytroleukemii na rosnące dawki FKL-137. Związek wyraźnie spowalniał wzrost komórek w czasie i prowadził do śmierci zaprogramowanej, widocznej przez klasyczne zmiany morfologii komórki i aktywację wewnętrznych mechanizmów apoptozy. Co istotne, FKL-137 był znacznie silniejszy wobec komórek białaczkowych niż wobec normalnych komórek wątroby, a oceny bezpieczeństwa wskazywały na relatywnie niską toksyczność w skutecznych dawkach.
Atak na „bramki” cukrowe nowotworu
Zagłębiając się w mechanizmy, zespół zbadał, jak FKL-137 zakłóca metabolizm nowotworu. Stwierdzono, że komórki białaczkowe poddane leczeniu pobierały mniej glukozy i wydzielały mniej mleczanu, produktu ubocznego intensywnego spalania cukru. Kluczowe białka, które normalnie pomagają przekształcać glukozę w energię i składniki budulcowe, zostały osłabione. Przy użyciu modelowania komputerowego, testów stabilności termicznej i obrazowania wykazano, że FKL-137 wiąże się z GLUT1 — główną „bramką” na powierzchni komórki, przez którą glukoza trafia do wnętrza. Gdy poziomy GLUT1 zostały zmniejszone przy pomocy metod genetycznych, komórki białaczkowe rosły wolniej, korzystały z mniejszej ilości cukru i stały się jeszcze bardziej wrażliwe na FKL-137. To potwierdziło, że GLUT1 jest zarówno motorem wzrostu komórek erytroleukemii, jak i istotnym celem leku.
Zakłócenie pętli sygnalizacyjnej wzrostu
Badanie ujawniło również efekty wykraczające poza samą „bramkę” cukrową. Komórki erytroleukemii korzystają z szlaku sygnałowego znanego jako PI3K/AKT, który wspiera przeżycie, wzrost i intensywne wykorzystanie cukru, częściowo poprzez wspieranie GLUT1. Leczenie FKL-137 obniżało aktywne formy kluczowych białek w tym szlaku, przerywając wzmacniającą pętlę między transportem cukru a sygnałami wzrostu. U myszy zakażonych wirusem, który wiarygodnie wywołuje erytroleukemię, terapia FKL-137 poprawiła poziomy czerwonych krwinek, zmniejszyła powiększoną śledzionę, ograniczyła inwazję komórek nowotworowych do narządów i skorygowała nieprawidłowy metabolizm cukru w tkance śledziony — wszystko to bez oczywistych uszkodzeń serca, wątroby, płuc czy nerek.
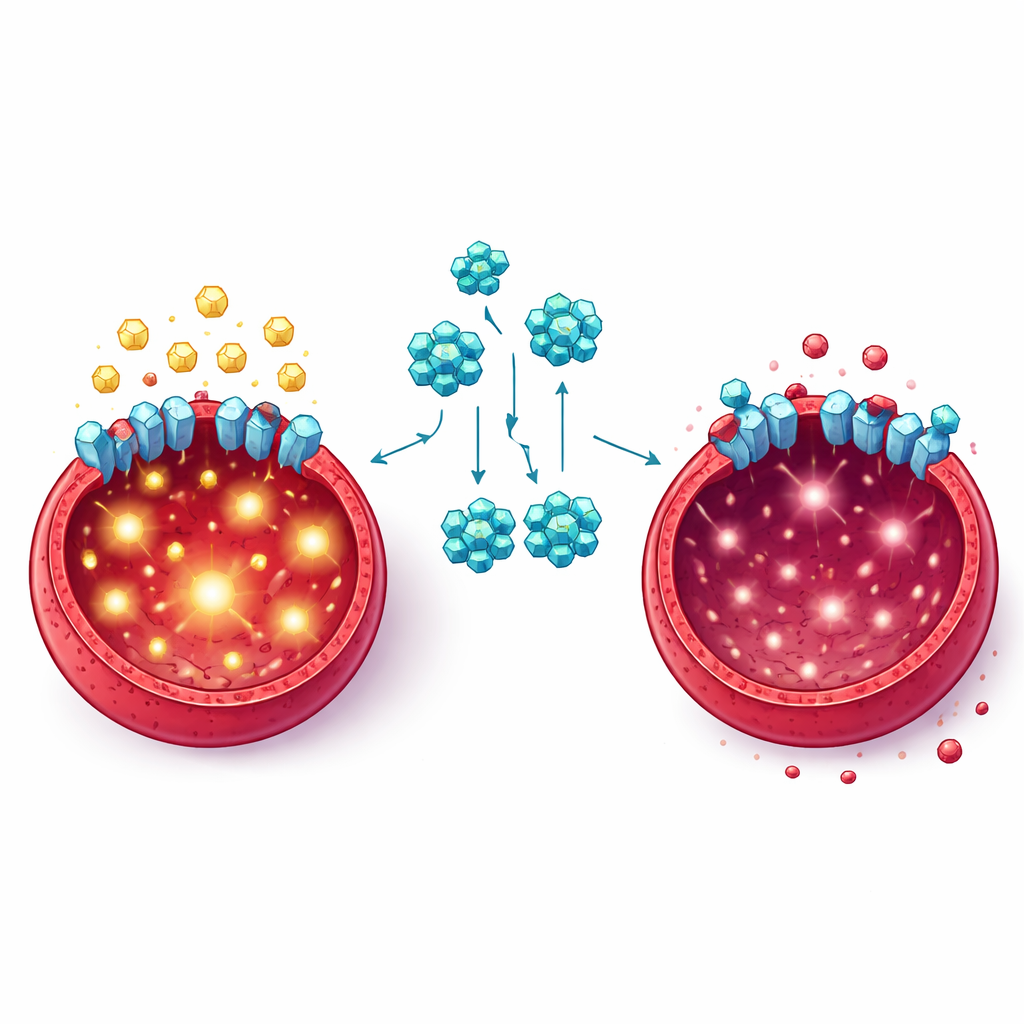
Obietnica, ograniczenia i następne kroki
Podsumowując, praca przedstawia FKL-137 jako kandydat na lek o podwójnym działaniu: blokuje główną „bramkę” cukrową komórek erytroleukemii i osłabia potężny szlak wzrostu zależny od tego paliwa. Poprzez najpierw głodzenie komórek nowotworowych, a następnie popychanie ich w kierunku śmierci, związek oferuje koncepcyjnie elegancki sposób wykorzystania słabości, której zdrowe komórki nie wykazują w takim samym stopniu. Autorzy zaznaczają jednak, że FKL-137 wymaga dalszego dopracowania: ma stosunkowo wąskie okno terapeutyczne, komórki nowotworowe mogą znaleźć sposoby rekompensacji poprzez przekierowanie metabolizmu, a wyniki uzyskane na liniach komórkowych i modelach mysich muszą zostać potwierdzone w tkankach ludzkich. Mimo to badanie wzmacnia przekonanie, że precyzyjne celowanie w to, jak komórki nowotworowe „jedzą” i rosną, może otworzyć nowe pole walki w leczeniu tej trudnej do opanowania choroby krwi.
Cytowanie: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
Słowa kluczowe: erytroleukemia, metabolizm nowotworu, inhibitor GLUT1, szlak PI3K AKT, terapia ukierunkowana