Clear Sky Science · pl
Dowód koncepcji ekstrakcji DNA wolnego od komórek z osocza oparty na dwufazowym układzie wodnym dla zastosowań biopsii płynnej
Dlaczego test krwi jest ważny w diagnostyce raka i innych chorób
Wiele współczesnych badań medycznych poszukuje drobnych fragmentów DNA krążących swobodnie we krwi. Te cząsteczki, nazywane DNA wolnym od komórek, mogą ujawnić, czy guz uwalnia materiał genetyczny, czy przeszczepiony narząd jest odrzucany, albo jak przebiega ciąża. Ponieważ fragmenty te są rzadkie, krótkie i wymieszane z białkami oraz innymi molekułami, ich czyste i szybkie wyizolowanie okazuje się zaskakująco trudne. W pracy tej zaprezentowano nowe, prostsze podejście do ekstrakcji tych fragmentów z osocza krwi z użyciem łagodnej, wodnej metody separacji, co może uczynić zaawansowane testy „biopsji płynnej” bardziej dostępnymi i niedrogimi.
Wyzwaniem jest wyłowienie maleńkich fragmentów DNA
Lekarze i badacze stosują biopsje płynne, aby odczytywać wskazówki genetyczne z prostego pobrania krwi zamiast wycinania tkanki. Problem polega na tym, że DNA wolne od komórek w osoczu występuje zwykle w ilościach rzędu kilkudziesięciu nanogramów na mililitr i jest rozdrobnione na krótkie fragmenty. Niewielka część tego materiału może pochodzić z guza albo z przeszczepionego narządu, więc każdy fragment ma znaczenie. Standardowe zestawy do izolacji DNA wychwytują materiał, sprawiając, że przylega on do powierzchni krzemionkowych w obecności silnych soli, a następnie stosują wielokrotne płukania i wirowanie. Zestawy te działają dobrze, ale wymagają czasu, specjalnego sprzętu i mogą być drogie. Mogą też mieć trudności z odzyskiwaniem najkrótszych fragmentów i przypadkowo pobierać długie odcinki DNA genomowego, które mogą maskować rzadkie sygnały chorobowe.
Dwuwarstwowy, wodny trik do wychwytywania DNA
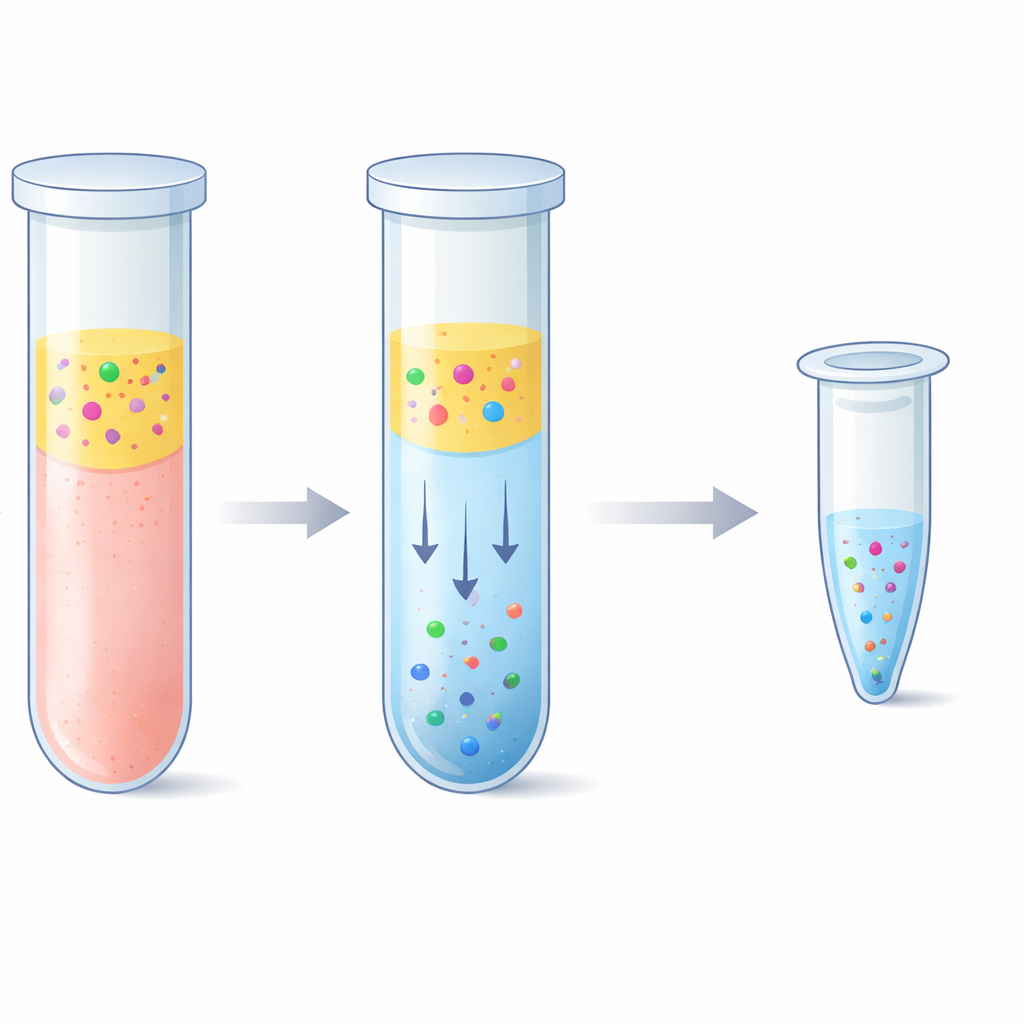
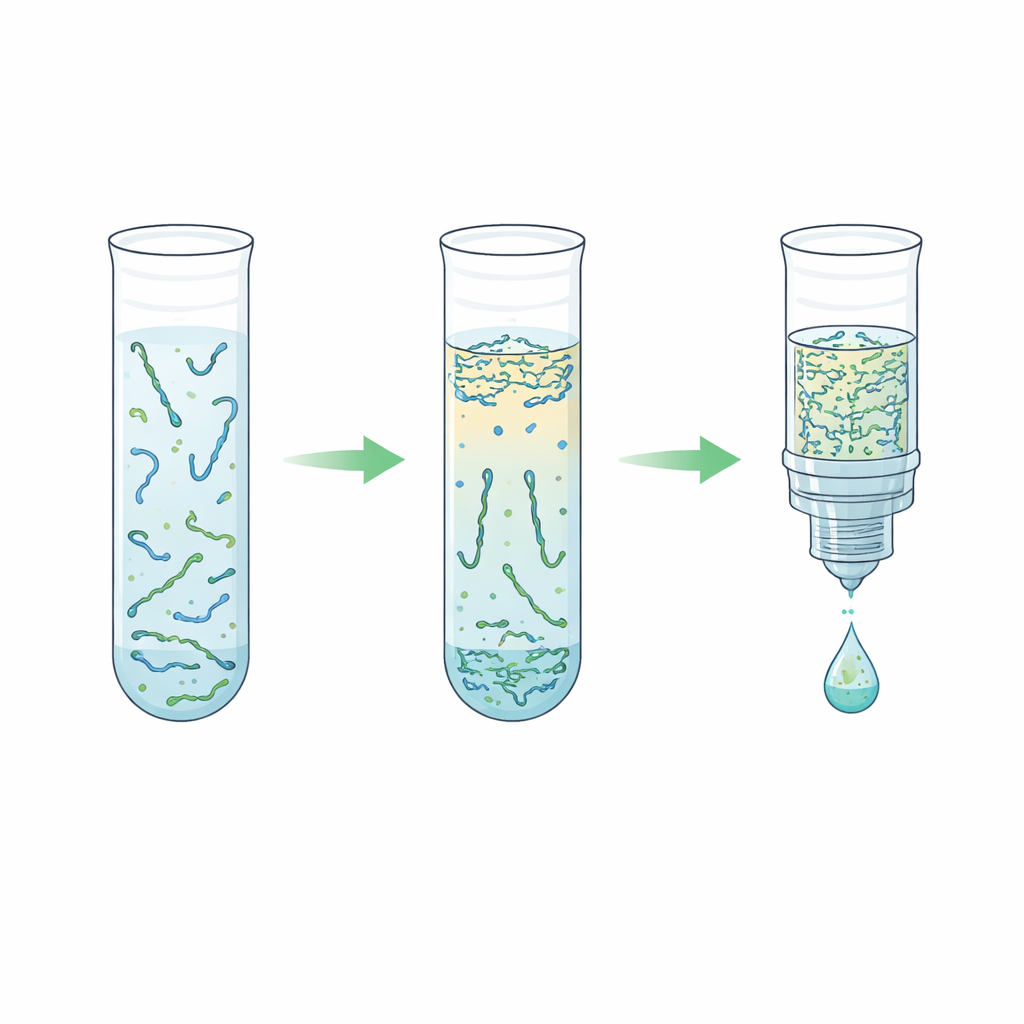
Zespół badał alternatywę opartą na „dwufazowym układzie wodnym” — mówiąc prościej, dwóch ciekłych faz bogatych w wodę, które nie mieszają się całkowicie, jak oliwa i ocet, ale obie złożone głównie z wody. Po zmieszaniu osocza z polimerem o nazwie poli(etylenoglikol) oraz prostymi solami fosforanowymi mieszanina naturalnie rozdzielała się na warstwę górną i dolną. Co niezwykłe, krótkie fragmenty DNA wyraźnie preferowały bogatą w sól dolną warstwę, podczas gdy większość białek krwi i długie nici DNA pozostawały w warstwie górnej lub na interfejsie. Badacze precyzyjnie dostroili skład, tak aby dolna warstwa była na tyle mała, by skoncentrować DNA, ale na tyle łagodna, by go nie uszkodzić. Następnie połączyli ten krok z „odwrotną elucją”, przez którą słona dolna warstwa była przepychana przez porowatą matrycę w celu usunięcia soli i zmniejszenia końcowej objętości, kończąc na czystszym i bardziej skoncentrowanym roztworze DNA.
Udoskonalanie procesu do zastosowań praktycznych
Wielokrotnymi testami autorzy dopracowali proporcje polimeru i soli, prędkości wirowania, objętości oraz opcjonalne kroki lizy rozbijające kompleksy białko–DNA. Stwierdzili, że zwiększenie zawartości polimeru wzdłuż pewnych linii składu podwajało koncentrację DNA bez pogorszenia wydajności, a silniejsze kondycjonowanie w kroku odwrotnej elucji mniej więcej czterokrotnie zwiększyło koncentrację w porównaniu z wcześniejszymi pracami. Zaskakująco, okazało się, że rezygnacja z agresywnej lizy przed separacją dwuwarstwową często dawała najlepsze wyniki; lizowanie miało tendencję do zaburzania faz i obniżania wydajności. Uproszczony, w dużej mierze pozbawiony lizy schemat usunął około 99,7% białek z osocza, odzyskując do około dwóch trzecich krótkiego DNA wejściowego w czterokrotnie mniejszej objętości, wszystko to w około dziesięć minut czasu całkowitego przetwarzania i zaledwie kilku minut obsługi manualnej.
Jak nowa metoda wypada w porównaniu
Badacze porównali swoje podejście z powszechnie używanym komercyjnym zestawem krzemionkowym. Standardowy zestaw dał nieco wyższe całkowite plony DNA i silniejszą koncentrację, ponieważ eluuje do bardzo małych objętości. Jednak metoda dwufazowa wykazała spójne odzyski powyżej 60% w szerokim zakresie wejść DNA, nawet przy bardzo małych ilościach, i wymagała znacznie mniej ręcznych kroków oraz mniejszej liczby urządzeń. Co istotne, nowy proces działał jak wbudowany filtr pod względem długości fragmentów: wzbogacał krótkie, przypominające DNA wolne od komórek fragmenty, jednocześnie w dużej mierze wykluczając długie nici pochodzące z uszkodzonych komórek krwi. Testy z użyciem ilościowego PCR wykazały, że oczyszczone ekstrakty nie hamują dalszej amplifikacji. Gdy zespół użył komercyjnej próbki odniesienia zawierającej znane mutacje związane z rakiem, odzyskane DNA dało się przygotować do bibliotek sekwencjonowania, uruchomić na wysokoprzepustowym sekwenserze i wykorzystać do wykrycia wszystkich oczekiwanych wariantów w odpowiednich częstościach.
Co to może oznaczać dla przyszłych testów krwi
Mówiąc wprost, praca ta pokazuje, że stosunkowo prosta, wodna separacja może zastąpić bardziej złożoną chemię powierzchni stałych w przygotowaniu DNA wolnego od komórek z osocza. Chociaż nowa metoda obecnie daje nieco mniejsze plony niż najlepsze komercyjne zestawy, oferuje szybkie przetwarzanie, skuteczne usuwanie niepożądanych białek i długiego DNA oraz dobrą kompatybilność z PCR i sekwencjonowaniem następnej generacji. Jeśli zostanie dodatkowo zwalidowana na próbkach od pacjentów i dopracowana pod kątem automatyzacji, podejście to mogłoby obniżyć koszty i uprościć pracę laboratoryjną, pomagając w szerszym wdrożeniu precyzyjnych, opartych na genetyce testów krwi dla raka, transplantologii i innych schorzeń.
Cytowanie: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Słowa kluczowe: biopsja płynna, DNA wolne od komórek, test krwi na raka, izolacja DNA, sekwencjonowanie następnej generacji